よむ、つかう、まなぶ。
資料2-2-1 MID-NET・NDB の行政利活用の調査実施状況について[2.4MB] (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_70725.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和7年度第4回 3/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
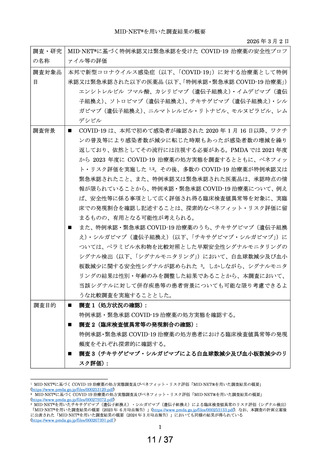
調査 3(チキサゲビマブ・シルガビマブによる白血球数減少及び血小板数減少のリ
スク評価)
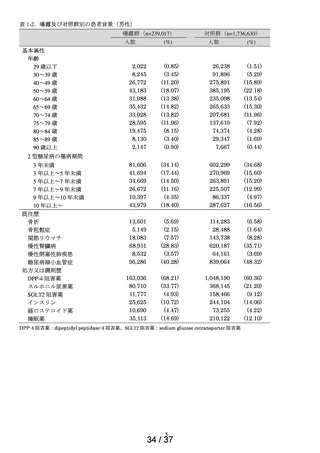
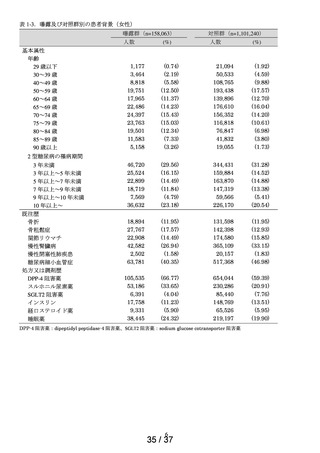
2014 年 1 月 1 日から 2023 年 12 月 31 日までの期間において、チキサゲビマブ・
シルガビマブ又はペラミビル水和物の処方がある患者を特定し、この期間における
処方日のうち最も早い日を t0 とした。このうち、データ期間中の最初の医療記録日
が t0 の 180 日以上前にあり、除外基準※1 に該当しない患者を調査の対象集団と
し、t0 時点で処方された薬剤がチキサゲビマブ・シルガビマブである患者を曝露群、
ペラミビル水和物である患者を対照群※2 に分類した。
※1 除外基準
① t0 時点でチキサゲビマブ・シルガビマブとペラミビルの両方が処方されている
② t0 時点で追跡期間終了の条件に該当している
③ t0-180 日から t0 日までの期間(t0-180 日及び t0 を含む)を Look back 期間とし、Look back 期間に
CTCAE Grade 1 以上の着目する臨床検査値異常がある
④ Look back 期間に着目する臨床検査値を持たない(欠測)
。
⑤ 観察期間の開始日が t0-364 日から t0-180 日の間にある
⑥ 観察期間の開始日から t0 までの期間に、ペラミビルの処方がある。
※2 対照群
チキサゲビマブ・シルガビマブは一般流通がなく、国からの供給は発症抑制目的での投与に限定されて
・イムデビマブ(遺
おり 5、他に発症抑制を効能効果に有する薬剤には、カシリビマブ(遺伝子組換え)
伝子組換え)
(以下、
「カシリビマブ・イムデビマブ」
)がある。本調査の契機となったチキサゲビマブ・
シルガビマブのシグナルモニタリングはペラミビル水和物以外にカシリビマブ・イムデビマブも比較
対照として行ったが、カシリビマブ・イムデビマブはチキサゲビマブ・シルガビマブに比べて、MIDNET における処方患者数が 1/10 程度と少なく 6、患者背景を可能な限り調整する解析を行うにあたり
対象者数の観点で限界がある等の課題が考えられた。一方、ペラミビル水和物はインフルエンザウイル
ス感染症に対する医薬品で効能効果は異なるものの、一定の使用実績があり既に白血球数減少及び血
小板数減少のリスクが知られていることから、本調査でも引き続きペラミビル水和物を対照群に設定
した。
追跡期間の定義
<追跡期間の開始日>t0 の翌日
<追跡期間の終了日>
調査 2-1 では以下の①~⑤、調査 2-2 及び調査 3 では以下の①、④~⑥
のいずれか早い日とした。
①
処方期間※1 の終了日
②
他の群に属する特例承認・緊急承認 COVID-19 治療薬又はデキサメタゾ
ン、トシリズマブ、バリシチニブ、ファビピラビル※2 の追加もしくは切
替え日の前日※3
③
退院日
④
観察期間終了日
⑤
アウトカムの発現日
⑥
他の群に属する医薬品の追加もしくは切替え日の前日※3
※1 処方期間の特定方法
処方日に処方日数を加えた日と後続の処方日が連日の場合に、処方が継続しているとみなし、最後の処
方日に処方日数と 30 日を加えた日を処方期間の終了日とした。
5「新型コロナウイルス感染症における中和抗体薬「チキサゲビマブ及びシルガビマブ」の医療機関への配分について」事務連絡令和 4 年 9 月
1 日(令和 6 年 5 月 24 日最終改正)
6 MID-NET®を用いたチキサゲビマブ(遺伝子組換え)・シルガビマブ(遺伝子組換え)による臨床検査値異常のリスク評価(シグナル検
出)「MID-NET®を用いた調査結果の概要(2023 年 6 月時点報告)」(https://www.pmda.go.jp/files/000253134.pdf) なお、本調査の計画
立案後に 公表された「MID-NET®を用いた調査結果の概要(2024 年 3 月時点報告)」(https://www.pmda.go.jp/files/000267390.pdf) に
おいても同様の結果が得られている
3
13 / 37
調査 3(チキサゲビマブ・シルガビマブによる白血球数減少及び血小板数減少のリ
スク評価)
2014 年 1 月 1 日から 2023 年 12 月 31 日までの期間において、チキサゲビマブ・
シルガビマブ又はペラミビル水和物の処方がある患者を特定し、この期間における
処方日のうち最も早い日を t0 とした。このうち、データ期間中の最初の医療記録日
が t0 の 180 日以上前にあり、除外基準※1 に該当しない患者を調査の対象集団と
し、t0 時点で処方された薬剤がチキサゲビマブ・シルガビマブである患者を曝露群、
ペラミビル水和物である患者を対照群※2 に分類した。
※1 除外基準
① t0 時点でチキサゲビマブ・シルガビマブとペラミビルの両方が処方されている
② t0 時点で追跡期間終了の条件に該当している
③ t0-180 日から t0 日までの期間(t0-180 日及び t0 を含む)を Look back 期間とし、Look back 期間に
CTCAE Grade 1 以上の着目する臨床検査値異常がある
④ Look back 期間に着目する臨床検査値を持たない(欠測)
。
⑤ 観察期間の開始日が t0-364 日から t0-180 日の間にある
⑥ 観察期間の開始日から t0 までの期間に、ペラミビルの処方がある。
※2 対照群
チキサゲビマブ・シルガビマブは一般流通がなく、国からの供給は発症抑制目的での投与に限定されて
・イムデビマブ(遺
おり 5、他に発症抑制を効能効果に有する薬剤には、カシリビマブ(遺伝子組換え)
伝子組換え)
(以下、
「カシリビマブ・イムデビマブ」
)がある。本調査の契機となったチキサゲビマブ・
シルガビマブのシグナルモニタリングはペラミビル水和物以外にカシリビマブ・イムデビマブも比較
対照として行ったが、カシリビマブ・イムデビマブはチキサゲビマブ・シルガビマブに比べて、MIDNET における処方患者数が 1/10 程度と少なく 6、患者背景を可能な限り調整する解析を行うにあたり
対象者数の観点で限界がある等の課題が考えられた。一方、ペラミビル水和物はインフルエンザウイル
ス感染症に対する医薬品で効能効果は異なるものの、一定の使用実績があり既に白血球数減少及び血
小板数減少のリスクが知られていることから、本調査でも引き続きペラミビル水和物を対照群に設定
した。
追跡期間の定義
<追跡期間の開始日>t0 の翌日
<追跡期間の終了日>
調査 2-1 では以下の①~⑤、調査 2-2 及び調査 3 では以下の①、④~⑥
のいずれか早い日とした。
①
処方期間※1 の終了日
②
他の群に属する特例承認・緊急承認 COVID-19 治療薬又はデキサメタゾ
ン、トシリズマブ、バリシチニブ、ファビピラビル※2 の追加もしくは切
替え日の前日※3
③
退院日
④
観察期間終了日
⑤
アウトカムの発現日
⑥
他の群に属する医薬品の追加もしくは切替え日の前日※3
※1 処方期間の特定方法
処方日に処方日数を加えた日と後続の処方日が連日の場合に、処方が継続しているとみなし、最後の処
方日に処方日数と 30 日を加えた日を処方期間の終了日とした。
5「新型コロナウイルス感染症における中和抗体薬「チキサゲビマブ及びシルガビマブ」の医療機関への配分について」事務連絡令和 4 年 9 月
1 日(令和 6 年 5 月 24 日最終改正)
6 MID-NET®を用いたチキサゲビマブ(遺伝子組換え)・シルガビマブ(遺伝子組換え)による臨床検査値異常のリスク評価(シグナル検
出)「MID-NET®を用いた調査結果の概要(2023 年 6 月時点報告)」(https://www.pmda.go.jp/files/000253134.pdf) なお、本調査の計画
立案後に 公表された「MID-NET®を用いた調査結果の概要(2024 年 3 月時点報告)」(https://www.pmda.go.jp/files/000267390.pdf) に
おいても同様の結果が得られている
3
13 / 37