会議資料 (35 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00043.html |
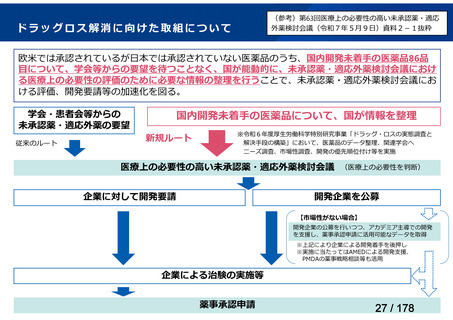
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第65回 9/29)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
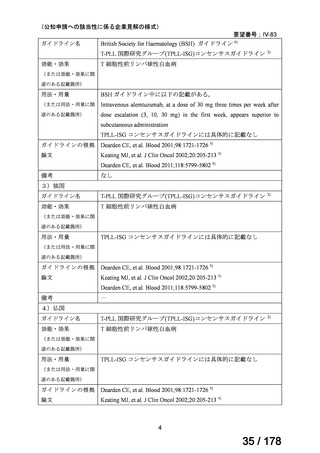
要望番号;IV-83
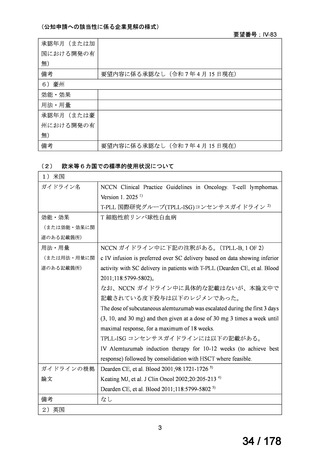
ガイドライン名
British Society for Haematology (BSH) ガイドライン 6)
T-PLL 国際研究グループ(TPLL-ISG)コンセンサスガイドライン 2)
効能・効果
T 細胞性前リンパ球性白血病
(または効能・効果に関
連のある記載箇所)
用法・用量
BSH ガイドライン中に以下の記載がある。
(または用法・用量に関
Intravenous alemtuzumab, at a dose of 30 mg three times per week after
連のある記載箇所)
dose escalation (3, 10, 30 mg) in the first week, appears superior to
subcutaneous administration
TPLL-ISG コンセンサスガイドラインには具体的に記載なし
ガイドラインの根拠
Dearden CE, et al. Blood 2001;98:1721-1726 3)
論文
Keating MJ, et al. J Clin Oncol 2002;20:205-213 4)
Dearden CE, et al. Blood 2011;118:5799-5802 5)
備考
なし
3)独国
ガイドライン名
T-PLL 国際研究グループ(TPLL-ISG)コンセンサスガイドライン 2)
効能・効果
T 細胞性前リンパ球性白血病
(または効能・効果に関
連のある記載箇所)
用法・用量
TPLL-ISG コンセンサスガイドラインには具体的に記載なし
(または用法・用量に関
連のある記載箇所)
ガイドラインの根拠
Dearden CE, et al. Blood 2001;98:1721-1726 3)
論文
Keating MJ, et al. J Clin Oncol 2002;20:205-213 4)
Dearden CE, et al. Blood 2011;118:5799-5802 5)
備考
-
4)仏国
ガイドライン名
T-PLL 国際研究グループ(TPLL-ISG)コンセンサスガイドライン 2)
効能・効果
T 細胞性前リンパ球性白血病
(または効能・効果に関
連のある記載箇所)
用法・用量
TPLL-ISG コンセンサスガイドラインには具体的に記載なし
(または用法・用量に関
連のある記載箇所)
ガイドラインの根拠
Dearden CE, et al. Blood 2001;98:1721-1726 3)
論文
Keating MJ, et al. J Clin Oncol 2002;20:205-213 4)
4
35 / 178