よむ、つかう、まなぶ。
【参考1】新型コロナウイルス感染症COVID-19診療の手引き 第10.0版 (40 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000121431_00416.html |
| 出典情報 | 「新型コロナウイルス感染症(COVID-19)診療の手引き・第 10.0 版」の 周知について(8/21付 事務連絡)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
●新型コロナウイルス感染症(COVID-19) 診療の手引き・第 10.0 版 ●5 薬物療法
ニルマトレルビル/リトナビル
商品名:パキロビッドパック
プロテアーゼ阻害薬
2022.2.10 特例承認,2023.3.15 保険適用,2023.3.22 一般流通開始
禁忌 ①本剤の成分に対し過敏症の既往歴のある患者
②特定の薬剤を投与中の患者(最新の添付文書を参照)
③腎機能または肝機能障害のある患者で,コルヒチンを投与中の患者
☞ ニルマトレルビル/リトナビル(医薬品医療機器総合機構 HP)
ニルマトレルビルは,SARS-CoV-2 のメイン(3CL)プロテアーゼに作用し,その働きを
阻害することによりウイルスの増殖を阻害する.リトナビルは,ニルマトレルビルの代謝を遅
らせ,体内濃度をウイルスに作用する濃度に維持する目的で併用される.
国内外で実施された多施設共同,プラセボ対照,ランダム化二重盲検試験において,重症
化リスクのある非入院 COVID-19 患者の外来治療を対象にニルマトレルビル 300 mg /リ
トナビル 100 mg またはプラセボを 1 日 2 回,5 日間経口投与する群に 1 対 1 で無作為割付
した.主要有効性解析集団とされた mITT 集団(無作為化され,治験薬が 1 回以上投与され,
ベースライン後から無作為化 28 日目までに少なくとも 1 回の受診があり,ベースライン時
点で COVID-19 に対するモノクローナル抗体が投与されておらず投与の予定もなく,かつ,
COVID-19 の症状発現から 3 日以内に治験薬が投与された被験者)の 45%が投与 28 日目を
完了した時点で行うよう事前に計画されていた中間解析において,mITT 集団のうちプラセボ
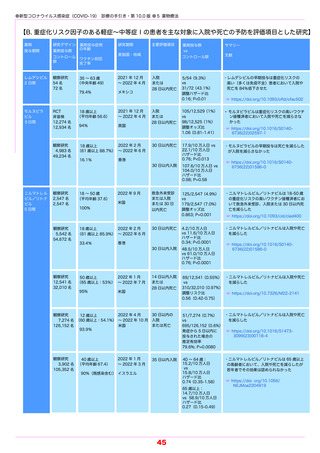
群(385 名)の 28 日目までの入院または死亡 27 名(7.0%)に対し,治療群(389 名)で
は 3 名(0.8%)と相対リスクが 89%減少した(p<0.0001)
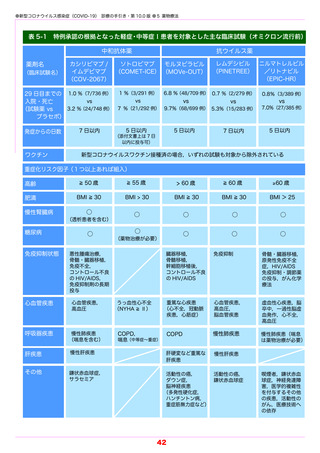
(表 5-1)
.
この結果を受け,中間解析以降の被験者登録が中止されたが,被験者登録が中止されるまで
に組み入れられたすべての被験者(2,246 名)を対象とした解析の結果においては,mITT 集
団のうちプラセボ群(682 名)の 28 日目までの入院または死亡が 44 名(6.5%)に対し,治
療群(697 名)では 5 名(0.7%)と,相対リスクが 89%減少となった.
また,副次有効性解析集団とされた mITT1 集団(無作為化され,治験薬が 1 回以上投与さ
れ,ベースライン後から無作為化 28 日目までに少なくとも 1 回の受診があり,ベースライン
時点で COVID-19 に対するモノクローナル抗体が投与されておらず投与の予定もなく,かつ,
COVID-19 の症状発現から 5 日以内に治験薬が投与された被験者)における,被験者登録が中
止されるまでに組み入れられたすべての被験者を対象とした解析の結果では,mITT1 集団のう
ちプラセボ群(1,046 名)の 28 日目までの入院または死亡が 66 名(6.3%)に対し,治療群
(1,039 名)では 8 名(0.8%)と,相対リスクが 88%減少した.
投与方法(用法・用量)
〔成人および 12 歳以上かつ体重 40 kg 以上の小児〕ニルマトレルビルとして,1回 300 mg
およびリトナビルとして1回 100 mg を同時に1日2回,5日間経口投与する.
40
ニルマトレルビル/リトナビル
商品名:パキロビッドパック
プロテアーゼ阻害薬
2022.2.10 特例承認,2023.3.15 保険適用,2023.3.22 一般流通開始
禁忌 ①本剤の成分に対し過敏症の既往歴のある患者
②特定の薬剤を投与中の患者(最新の添付文書を参照)
③腎機能または肝機能障害のある患者で,コルヒチンを投与中の患者
☞ ニルマトレルビル/リトナビル(医薬品医療機器総合機構 HP)
ニルマトレルビルは,SARS-CoV-2 のメイン(3CL)プロテアーゼに作用し,その働きを
阻害することによりウイルスの増殖を阻害する.リトナビルは,ニルマトレルビルの代謝を遅
らせ,体内濃度をウイルスに作用する濃度に維持する目的で併用される.
国内外で実施された多施設共同,プラセボ対照,ランダム化二重盲検試験において,重症
化リスクのある非入院 COVID-19 患者の外来治療を対象にニルマトレルビル 300 mg /リ
トナビル 100 mg またはプラセボを 1 日 2 回,5 日間経口投与する群に 1 対 1 で無作為割付
した.主要有効性解析集団とされた mITT 集団(無作為化され,治験薬が 1 回以上投与され,
ベースライン後から無作為化 28 日目までに少なくとも 1 回の受診があり,ベースライン時
点で COVID-19 に対するモノクローナル抗体が投与されておらず投与の予定もなく,かつ,
COVID-19 の症状発現から 3 日以内に治験薬が投与された被験者)の 45%が投与 28 日目を
完了した時点で行うよう事前に計画されていた中間解析において,mITT 集団のうちプラセボ
群(385 名)の 28 日目までの入院または死亡 27 名(7.0%)に対し,治療群(389 名)で
は 3 名(0.8%)と相対リスクが 89%減少した(p<0.0001)
(表 5-1)
.
この結果を受け,中間解析以降の被験者登録が中止されたが,被験者登録が中止されるまで
に組み入れられたすべての被験者(2,246 名)を対象とした解析の結果においては,mITT 集
団のうちプラセボ群(682 名)の 28 日目までの入院または死亡が 44 名(6.5%)に対し,治
療群(697 名)では 5 名(0.7%)と,相対リスクが 89%減少となった.
また,副次有効性解析集団とされた mITT1 集団(無作為化され,治験薬が 1 回以上投与さ
れ,ベースライン後から無作為化 28 日目までに少なくとも 1 回の受診があり,ベースライン
時点で COVID-19 に対するモノクローナル抗体が投与されておらず投与の予定もなく,かつ,
COVID-19 の症状発現から 5 日以内に治験薬が投与された被験者)における,被験者登録が中
止されるまでに組み入れられたすべての被験者を対象とした解析の結果では,mITT1 集団のう
ちプラセボ群(1,046 名)の 28 日目までの入院または死亡が 66 名(6.3%)に対し,治療群
(1,039 名)では 8 名(0.8%)と,相対リスクが 88%減少した.
投与方法(用法・用量)
〔成人および 12 歳以上かつ体重 40 kg 以上の小児〕ニルマトレルビルとして,1回 300 mg
およびリトナビルとして1回 100 mg を同時に1日2回,5日間経口投与する.
40