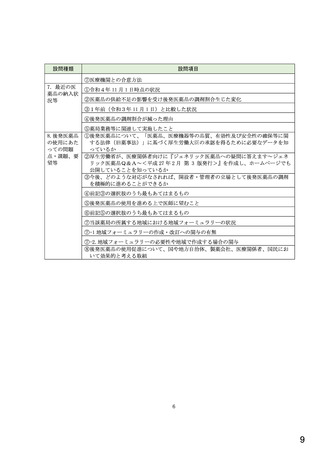
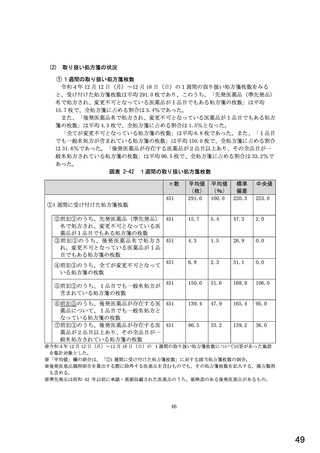
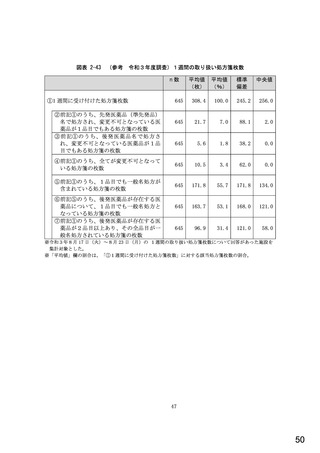
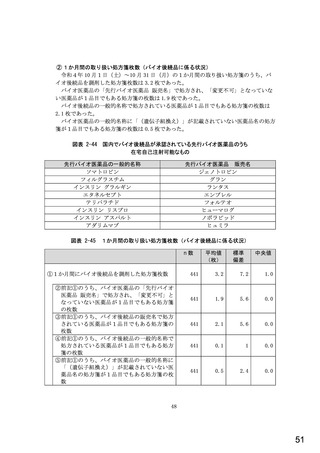
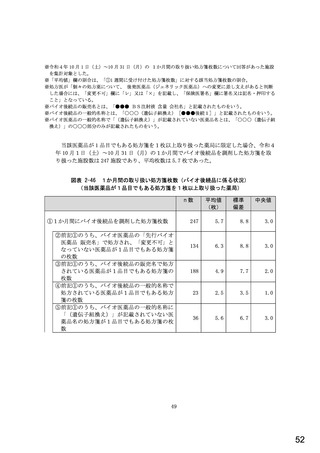
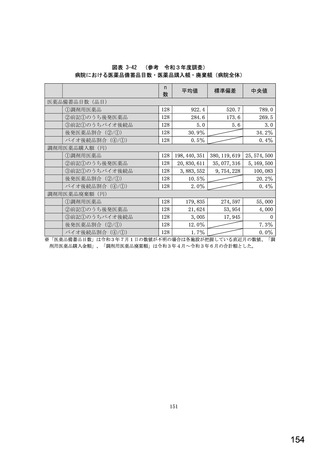
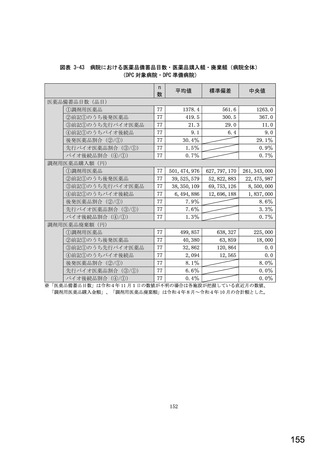
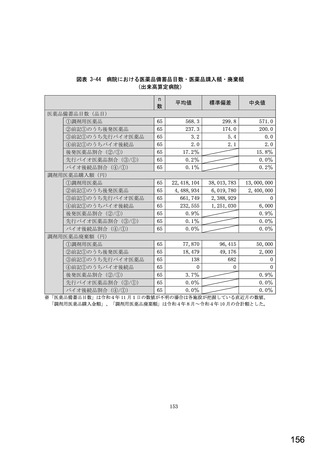
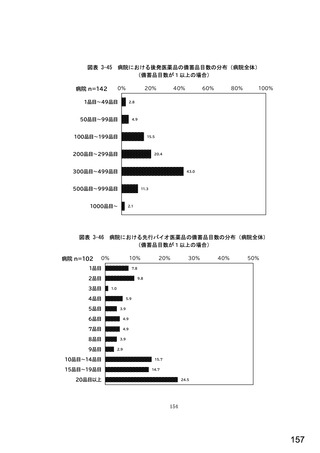
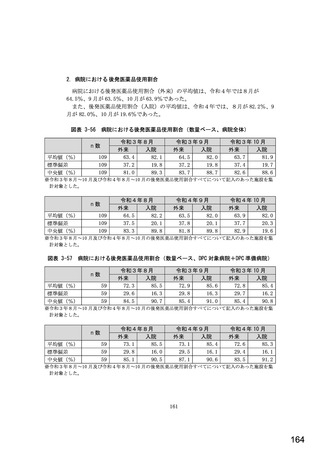
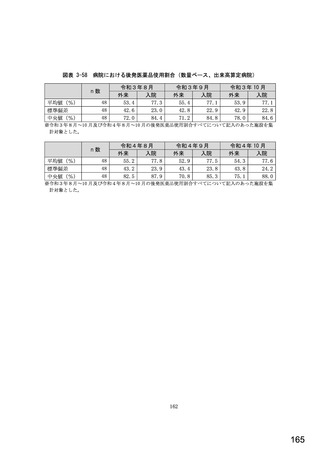
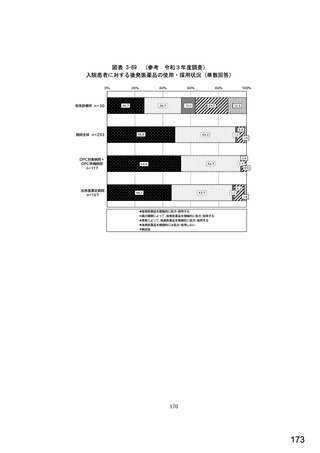
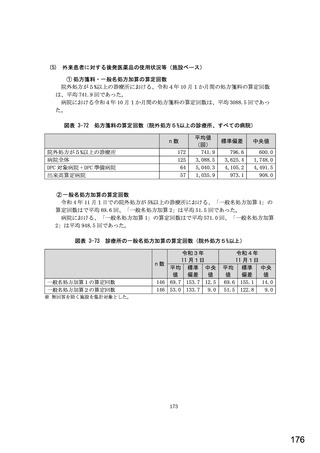
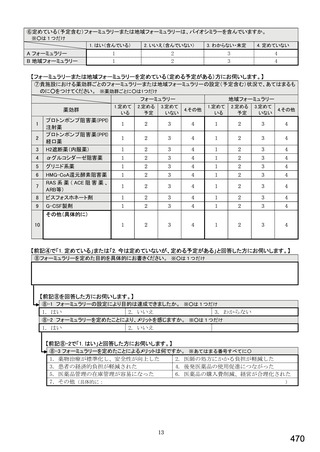
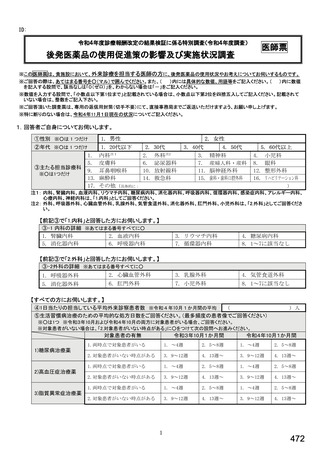
総-5-2○診療報酬改定結果検証部会からの報告について (77 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212500_00179.html |
| 出典情報 | 中央社会保険医療協議会 総会(第542回 3/22)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
0%
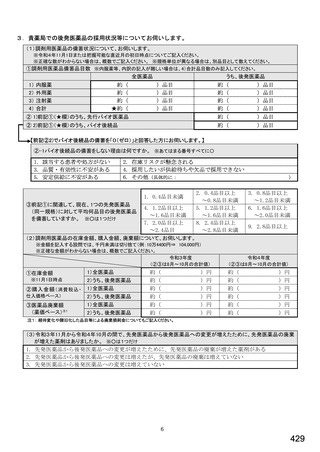
★後発医薬品メーカーが原薬、添加剤の製造国・製
造場所を公開していること
★後発医薬品メーカーが共同開発についての情報
を公開していること
★GMP(医薬品の製造管理及び品質管理の基準)
上、問題のないメーカーの製品であること
メーカー・卸からの情報提供が頻繁にあること
他の後発医薬品よりも薬価が安価であること
大病院で採用されていること
10% 20% 30% 40% 50% 60% 70%
11.7
1.0
4.9
0.0
26.2
3.3
32.9
2.0
17.9
1.4
10.4
0.0
近隣の保険医療機関(病院・診療所)で採用されて
いる処方銘柄であること
後発医薬品の適応症が先発医薬品と同一であるこ
と
納品までの時間が短いこと
29.8
5.1
49.3
2.9
31.3
1.6
61.8
★欠品(品切れ)のない会社の製品であること
10.3
47.5
★出荷調整のない会社の製品であること
4.8
★供給停止や回収等の問題事例のない会社の製品
であること
患者からの評判が良いこと
調剤がしやすい(例:容易に半割ができる、一包化
調剤がしやすい)こと
患者が使用しやすいよう医薬品に工夫がなされて
いること(例:味が良い、かぶれにくいなど)
先発医薬品メーカー・その子会社が扱う後発医薬品
であること
42.8
5.5
10.7
0.7
29.4
0.9
29.4
1.9
20.4
0.6
信頼のおける後発医薬品メーカーが扱う後発医薬
品であること
42.0
6.2
47.0
オーソライズドジェネリックであること
13.7
40.1
本社の方針・指示があった後発医薬品であること
共同購入先(同一グループの薬局を除く)で採用さ
れていること
21.1
6.8
1.3
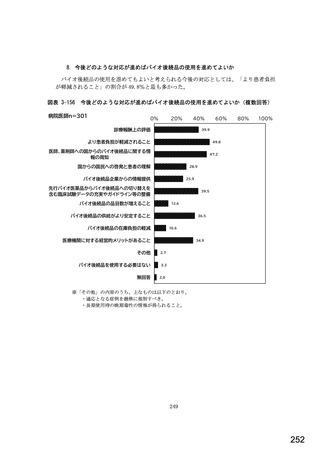
後発医薬品の採用基準 n=691
その他
令和2年度調査と選択肢項目の内容が異
なる場合、選択肢項目の先頭に★印。
無回答
3.0
1.3
採用基準で最も重視するもの n=691
0.6
14.3
73
76