よむ、つかう、まなぶ。
(別紙1)[2.8MB] (18 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00174.html |
| 出典情報 | 先進医療会議(第153回 4/9)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
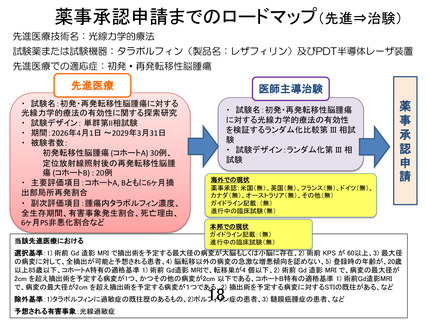
薬事承認申請までのロードマップ(先進⇒治験)
先進医療技術名:光線力学的療法
試験薬または試験機器:タラポルフィン(製品名:レザフィリン)及びPDT半導体レーザ装置
先進医療での適応症:初発・再発転移性脳腫瘍
先進医療
・ 試験名:初発・再発転移性脳腫瘍に対する
光線力学的療法の有効性に関する探索研究
・ 試験デザイン: 単群第II相試験
・ 期間:2026年4月1日 ~2029年3月31日
・ 被験者数:
初発転移性脳腫瘍 (コホートA) 30例、
定位放射線照射後の再発転移性脳腫
瘍 (コホートB) : 20例
・ 主要評価項目:コホートA, Bともに6ヶ月摘
出部局所再発割合
・ 副次評価項目:腫瘍内タラポルフィン濃度、
全生存期間、有害事象発生割合、死亡理由、
6ヶ月PS非悪化割合など
当該先進医療における
医師主導治験
・ 試験名:初発・再発転移性脳腫瘍
に対する光線力学的療法の有効性
を検証するランダム化比較第 III 相試
験
・ 試験デザイン:ランダム化第 III 相
試験
海外での現状
薬事承認:米国(無)、英国(無)、フランス(無)、ドイツ(無)、
カナダ(無)、オーストラリア(無)、その他(無)
ガイドライン記載:(無)
進行中の臨床試験(無)
薬
事
承
認
申
請
本邦での現状
ガイドライン記載:(無)
進行中の臨床試験(無)
選択基準:1) 術前 Gd 造影 MRI で摘出術を予定する最大径の病変が大脳もしくは小脳に存在、2) 術前 KPS が 60以上、3) 最大径
の病変に対して、全摘出が可能と予想される患者、4) 脳転移以外の病変の急激な増悪傾向を認めない、5) 登録時の年齢が、20歳
以上85歳以下、コホートA特有の適格基準 1) 術前 Gd造影 MRIで、転移巣が4 個以下、2) 術前 Gd 造影 MRI で、病変の最大径が
2cm を超え摘出術を予定する病変が1つ、かつその他の病変が2cm 以下である、コホートB特有の適格基準 1) 術前Gd造影MRI
で、病変の最大径が2cm を超え摘出術を予定する病変が1つである、2) 摘出術を予定する病変に対するSTIの既往がある、など
18
除外基準:1)タラポルフィンに過敏症の既往歴のあるもの、2)ポルフィリン症の患者、3) 髄膜癌腫症の患者、など
予想される有害事象:光線過敏症
先進医療技術名:光線力学的療法
試験薬または試験機器:タラポルフィン(製品名:レザフィリン)及びPDT半導体レーザ装置
先進医療での適応症:初発・再発転移性脳腫瘍
先進医療
・ 試験名:初発・再発転移性脳腫瘍に対する
光線力学的療法の有効性に関する探索研究
・ 試験デザイン: 単群第II相試験
・ 期間:2026年4月1日 ~2029年3月31日
・ 被験者数:
初発転移性脳腫瘍 (コホートA) 30例、
定位放射線照射後の再発転移性脳腫
瘍 (コホートB) : 20例
・ 主要評価項目:コホートA, Bともに6ヶ月摘
出部局所再発割合
・ 副次評価項目:腫瘍内タラポルフィン濃度、
全生存期間、有害事象発生割合、死亡理由、
6ヶ月PS非悪化割合など
当該先進医療における
医師主導治験
・ 試験名:初発・再発転移性脳腫瘍
に対する光線力学的療法の有効性
を検証するランダム化比較第 III 相試
験
・ 試験デザイン:ランダム化第 III 相
試験
海外での現状
薬事承認:米国(無)、英国(無)、フランス(無)、ドイツ(無)、
カナダ(無)、オーストラリア(無)、その他(無)
ガイドライン記載:(無)
進行中の臨床試験(無)
薬
事
承
認
申
請
本邦での現状
ガイドライン記載:(無)
進行中の臨床試験(無)
選択基準:1) 術前 Gd 造影 MRI で摘出術を予定する最大径の病変が大脳もしくは小脳に存在、2) 術前 KPS が 60以上、3) 最大径
の病変に対して、全摘出が可能と予想される患者、4) 脳転移以外の病変の急激な増悪傾向を認めない、5) 登録時の年齢が、20歳
以上85歳以下、コホートA特有の適格基準 1) 術前 Gd造影 MRIで、転移巣が4 個以下、2) 術前 Gd 造影 MRI で、病変の最大径が
2cm を超え摘出術を予定する病変が1つ、かつその他の病変が2cm 以下である、コホートB特有の適格基準 1) 術前Gd造影MRI
で、病変の最大径が2cm を超え摘出術を予定する病変が1つである、2) 摘出術を予定する病変に対するSTIの既往がある、など
18
除外基準:1)タラポルフィンに過敏症の既往歴のあるもの、2)ポルフィリン症の患者、3) 髄膜癌腫症の患者、など
予想される有害事象:光線過敏症