よむ、つかう、まなぶ。
(別紙1)[2.8MB] (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00174.html |
| 出典情報 | 先進医療会議(第153回 4/9)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
別紙1
先進医療 B
評価委員
主担当:
副担当:
坂井
掛江
実施計画等評価表(番号 B152)
副担当: 上村
先進医療の名称
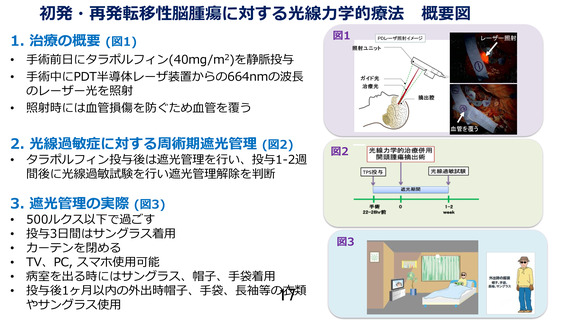
初発・再発転移性脳腫瘍に対する光線力学的療法
申請医療機関
国立がん研究センター中央病院
医療技術の概要
転移性脳腫瘍は進行癌患者の 10〜40%に発生し、手術や放射
線治療を主体とする現行治療では局所再発や放射線壊死が課題
である。本研究は、国産アカデミア発の光感受性物質タラポル
フィンを用いた PDT を開頭腫瘍摘出術を要する初発および再発
転移性脳腫瘍に適応拡大を目指す探索的臨床試験である。開頭
腫瘍摘出後にレーザ光を照射し、タラポルフィンを取り込んだ
腫瘍細胞を選択的に破壊することで局所再発リスクを低減し、
放射線治療を回避できる可能性がある。主要評価項目は術後 6
か月の局所再発割合、副次評価項目として腫瘍内タラポルフィ
ンの集積の有無を検討する。本試験により PDT の proof of
concept を確立し、将来的な比較試験への基盤確立を行う。
○主要評価項目:術後 6 ヶ月後の摘出部局所再発割合
○副次評価項目:有効性評価項目:全生存期間、髄膜播種再発
期間、脳内遠隔再発期間、脳内再発期間、脳内無再発生存期間、
登録後 2, 6 ヶ月の MMSE 非悪化割合、登録後 6 ヶ月の KPS 非悪
化割合
安全性評価項目:腫瘍内タラポルフィン濃度、有害事象発生割合、
重篤な有害事象発生割合
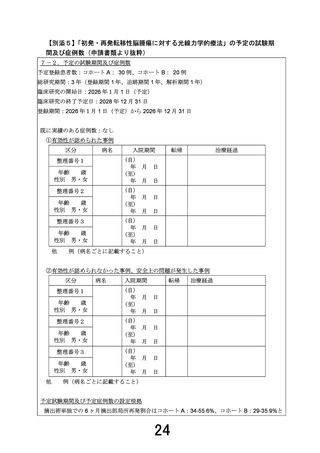
○予定試験期間:jRCT 公開日~2028 年 12 月 31 日
○目標症例数
コホート A(初発転移脳腫瘍): 30 例
コホート B(定位放射線照射後の再発転移性脳腫瘍): 20 例
1
先進医療 B
評価委員
主担当:
副担当:
坂井
掛江
実施計画等評価表(番号 B152)
副担当: 上村
先進医療の名称
初発・再発転移性脳腫瘍に対する光線力学的療法
申請医療機関
国立がん研究センター中央病院
医療技術の概要
転移性脳腫瘍は進行癌患者の 10〜40%に発生し、手術や放射
線治療を主体とする現行治療では局所再発や放射線壊死が課題
である。本研究は、国産アカデミア発の光感受性物質タラポル
フィンを用いた PDT を開頭腫瘍摘出術を要する初発および再発
転移性脳腫瘍に適応拡大を目指す探索的臨床試験である。開頭
腫瘍摘出後にレーザ光を照射し、タラポルフィンを取り込んだ
腫瘍細胞を選択的に破壊することで局所再発リスクを低減し、
放射線治療を回避できる可能性がある。主要評価項目は術後 6
か月の局所再発割合、副次評価項目として腫瘍内タラポルフィ
ンの集積の有無を検討する。本試験により PDT の proof of
concept を確立し、将来的な比較試験への基盤確立を行う。
○主要評価項目:術後 6 ヶ月後の摘出部局所再発割合
○副次評価項目:有効性評価項目:全生存期間、髄膜播種再発
期間、脳内遠隔再発期間、脳内再発期間、脳内無再発生存期間、
登録後 2, 6 ヶ月の MMSE 非悪化割合、登録後 6 ヶ月の KPS 非悪
化割合
安全性評価項目:腫瘍内タラポルフィン濃度、有害事象発生割合、
重篤な有害事象発生割合
○予定試験期間:jRCT 公開日~2028 年 12 月 31 日
○目標症例数
コホート A(初発転移脳腫瘍): 30 例
コホート B(定位放射線照射後の再発転移性脳腫瘍): 20 例
1