よむ、つかう、まなぶ。
材-4体外診断用医薬品 (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_62378.html |
| 出典情報 | 中央社会保険医療協議会 保険医療材料専門部会(第130回 8/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
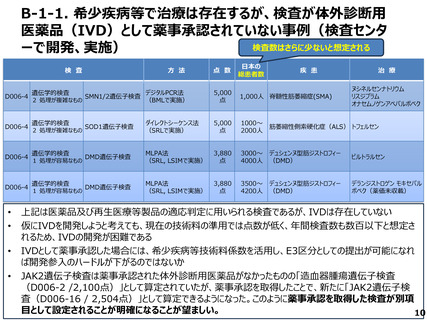
B-1-1.市場性評価(希少疾病等の検査)
検査回数:検査数が少なく、医技評経由で増点いただいた事例
対象患者数が少ない検査について、令和2年改定時に、日本臨床検査専門医会から医療技術再評価提案書が提出
された
対象疾患
患者数
検査
改定前
改定後
血栓性血小板減少
性紫斑病
約500人
ADAMTS13活性
400点
400点
ADAMTS13インヒビター
600点
1000点
•
•
上記検査の対象疾患である血栓性血小板減少性紫斑病の治療薬(リツキサンとアジンマ)は希少疾病用医薬
品の指定を受けている
医技評での要望においては、増点後2000回を想定している(B-1参考資料 参照)
≪提 案≫
◆ 希少疾病等の検査に用いるものとして配慮が必要な体外診断用医薬品(IVD)について、再生医療
を含む治療法等が発見された場合など新たにIVDを開発した場合に適用される仕組みとできないか
• LDT(薬事承認されていない検査等)が保険適用されている場合においても、IVDとして薬事承認された場合には、
E3区分としての提出が可能であることを明確化していただけないか
• 患者数が少なく、既存検査の準用ではIVDの開発が困難である場合がある。希少疾病等技術料係数を活用し、希
少疾患を対象とした検査の充実化に繋げられないか
◆ 現在規定されている年間検査回数については、開発そのものを躊躇する件数である。回数を緩和いた
だけないか
11
検査回数:検査数が少なく、医技評経由で増点いただいた事例
対象患者数が少ない検査について、令和2年改定時に、日本臨床検査専門医会から医療技術再評価提案書が提出
された
対象疾患
患者数
検査
改定前
改定後
血栓性血小板減少
性紫斑病
約500人
ADAMTS13活性
400点
400点
ADAMTS13インヒビター
600点
1000点
•
•
上記検査の対象疾患である血栓性血小板減少性紫斑病の治療薬(リツキサンとアジンマ)は希少疾病用医薬
品の指定を受けている
医技評での要望においては、増点後2000回を想定している(B-1参考資料 参照)
≪提 案≫
◆ 希少疾病等の検査に用いるものとして配慮が必要な体外診断用医薬品(IVD)について、再生医療
を含む治療法等が発見された場合など新たにIVDを開発した場合に適用される仕組みとできないか
• LDT(薬事承認されていない検査等)が保険適用されている場合においても、IVDとして薬事承認された場合には、
E3区分としての提出が可能であることを明確化していただけないか
• 患者数が少なく、既存検査の準用ではIVDの開発が困難である場合がある。希少疾病等技術料係数を活用し、希
少疾患を対象とした検査の充実化に繋げられないか
◆ 現在規定されている年間検査回数については、開発そのものを躊躇する件数である。回数を緩和いた
だけないか
11