よむ、つかう、まなぶ。
材-4体外診断用医薬品 (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_62378.html |
| 出典情報 | 中央社会保険医療協議会 保険医療材料専門部会(第130回 8/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
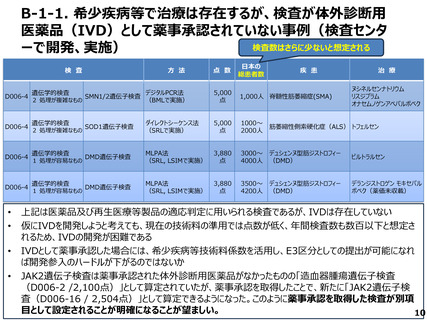
B-1-1. 希少疾病等で治療は存在するが、検査が体外診断用
医薬品(IVD)として薬事承認されていない事例(検査センタ
検査数はさらに少ないと想定される
ーで開発、実施)
方 法
点 数
日本の
総患者数
SMN1/2遺伝子検査
デジタルPCR法
(BMLで実施)
5,000
点
1,000人 脊髄性筋萎縮症(SMA)
SOD1遺伝子検査
ダイレクトシーケンス法
(SRLで実施)
5,000
点
1000~
2000人
筋萎縮性側索硬化症(ALS) トフェルセン
DMD遺伝子検査
MLPA法
(SRL, LSIMで実施)
3,880
点
3000~
4000人
デュシェンヌ型筋ジストロフィー
(DMD)
ビルトラルセン
DMD遺伝子検査
MLPA法
(SRL, LSIMで実施)
3,880
点
3500~
4200人
デュシェンヌ型筋ジストロフィー
(DMD)
デランジストロゲン モキセパル
ボベク(薬価未収載)
検 査
D006-4
D006-4
D006-4
D006-4
•
•
•
•
遺伝学的検査
2 処理が複雑なもの
遺伝学的検査
2 処理が複雑なもの
遺伝学的検査
1 処理が容易なもの
遺伝学的検査
1 処理が容易なもの
疾 患
治 療
ヌシネルセンナトリウム
リスジプラム
オナセムノゲンアベパルボベク
上記は医薬品及び再生医療等製品の適応判定に用いられる検査であるが、IVDは存在していない
仮にIVDを開発しようと考えても、現在の技術料の準用では点数が低く、年間検査数も数百以下と想定さ
れるため、IVDの開発が困難である
IVDとして薬事承認した場合には、希少疾病等技術料係数を活用し、E3区分としての提出が可能になれ
ば開発参入のハードルが下がるのではないか
JAK2遺伝子検査は薬事承認された体外診断用医薬品がなかったものの「造血器腫瘍遺伝子検査
(D006-2 /2,100点)」として算定されていたが、薬事承認を取得したことで、新たに「JAK2遺伝子検
査(D006-16 / 2,504点)」として算定できるようになった。このように薬事承認を取得した検査が別項
目として設定されることが明確になることが望ましい。
10
医薬品(IVD)として薬事承認されていない事例(検査センタ
検査数はさらに少ないと想定される
ーで開発、実施)
方 法
点 数
日本の
総患者数
SMN1/2遺伝子検査
デジタルPCR法
(BMLで実施)
5,000
点
1,000人 脊髄性筋萎縮症(SMA)
SOD1遺伝子検査
ダイレクトシーケンス法
(SRLで実施)
5,000
点
1000~
2000人
筋萎縮性側索硬化症(ALS) トフェルセン
DMD遺伝子検査
MLPA法
(SRL, LSIMで実施)
3,880
点
3000~
4000人
デュシェンヌ型筋ジストロフィー
(DMD)
ビルトラルセン
DMD遺伝子検査
MLPA法
(SRL, LSIMで実施)
3,880
点
3500~
4200人
デュシェンヌ型筋ジストロフィー
(DMD)
デランジストロゲン モキセパル
ボベク(薬価未収載)
検 査
D006-4
D006-4
D006-4
D006-4
•
•
•
•
遺伝学的検査
2 処理が複雑なもの
遺伝学的検査
2 処理が複雑なもの
遺伝学的検査
1 処理が容易なもの
遺伝学的検査
1 処理が容易なもの
疾 患
治 療
ヌシネルセンナトリウム
リスジプラム
オナセムノゲンアベパルボベク
上記は医薬品及び再生医療等製品の適応判定に用いられる検査であるが、IVDは存在していない
仮にIVDを開発しようと考えても、現在の技術料の準用では点数が低く、年間検査数も数百以下と想定さ
れるため、IVDの開発が困難である
IVDとして薬事承認した場合には、希少疾病等技術料係数を活用し、E3区分としての提出が可能になれ
ば開発参入のハードルが下がるのではないか
JAK2遺伝子検査は薬事承認された体外診断用医薬品がなかったものの「造血器腫瘍遺伝子検査
(D006-2 /2,100点)」として算定されていたが、薬事承認を取得したことで、新たに「JAK2遺伝子検
査(D006-16 / 2,504点)」として算定できるようになった。このように薬事承認を取得した検査が別項
目として設定されることが明確になることが望ましい。
10