よむ、つかう、まなぶ。
07資料2-3小児におけるRSウイルス感染症の予防について (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_64997.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会 ワクチン評価に関する小委員会(第32回 10/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
小児におけるRSウイルス感染症の予防に係るこれまでの経緯
平成14年(2002年)1月
モノクローナル抗体製剤パリビズマブが早産児等のRSウイルス感染症予防について薬事承認。
平成15年(2003年)10月
RSウイルス感染症が5類感染症の定点把握対象疾患(小児科定点)に追加。
平成25年(2013年)10月
第5回研究開発及び生産・流通部会(以下「生産・流通部会」)において、「RSウイルスワクチン」が
開発優先度の高いワクチンの一つに定められた。
12月
日本ワクチン産業協会の会員企業に対し、RSウイルスワクチン等の開発要請を行った。
令和6年(2024年)1月
母子免疫による新生児・乳児の予防を目的とするファイザー社の組換えRSウイルスワクチンが薬事承認。
3月
薬事・食品衛生審議会 医薬品第二部会において、以下の事項が了承された。
・効果の持続期間が長いモノクローナル抗体製剤であるニルセビマブ(nirsevimab)の、重症化リスク
の高い児のほか、生後初回のRSウイルス流行期のすべての新生児及び乳幼児等を対象とした承認。
・モノクローナル抗体製剤パリビズマブの適応に、肺低形成等の重症化リスクの高い5疾患を伴う24か月
齢以下の児を追加。
3月14日
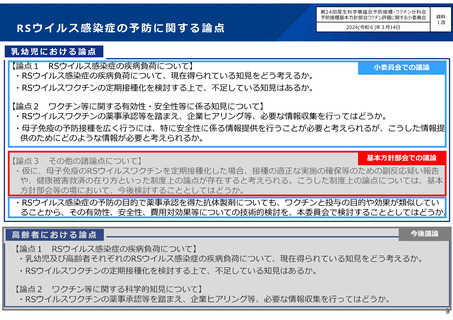
第24回ワクチン評価小委員会においてRSウイルスワクチンの議論を開始。
・母子免疫について、疾病負荷は一定程度明らかであるが、安全性についての情報収集や、抗体製剤(ニ
ルセビマブ)の扱いが論点とされた。
・企業からのヒアリングを含め、各論点について検討を進める方針。
9月4日
第27回ワクチン評価小委員会にて母子免疫ワクチン・抗体製剤の企業ヒアリングを実施。
・乳幼児におけるRSウイルスの予防について、疾病負荷や母子免疫ワクチンおよび抗体製剤の有効性に
ついては一定の知見があるとされた。
・一方、ワクチン等の安全性については国内の知見が限定的であり、企業による安全性情報の収集が予定
されていることから引き続き国内の安全性に係る知見を収集し、ワクチン等の評価に必要な情報が一定
程度集積した段階でファクトシートの作成に進むこととされた。
11月21日
第28回ワクチン評価小委員会において、知見の一定の集積を踏まえ、疾病負荷、母子免疫ワクチン及び抗
体製剤の有効性・安全性、費用対効果について、ファクトシートの作成を国立感染症研究所に依頼し、そ
れを踏まえて再度議論を行うこととされた。
4
平成14年(2002年)1月
モノクローナル抗体製剤パリビズマブが早産児等のRSウイルス感染症予防について薬事承認。
平成15年(2003年)10月
RSウイルス感染症が5類感染症の定点把握対象疾患(小児科定点)に追加。
平成25年(2013年)10月
第5回研究開発及び生産・流通部会(以下「生産・流通部会」)において、「RSウイルスワクチン」が
開発優先度の高いワクチンの一つに定められた。
12月
日本ワクチン産業協会の会員企業に対し、RSウイルスワクチン等の開発要請を行った。
令和6年(2024年)1月
母子免疫による新生児・乳児の予防を目的とするファイザー社の組換えRSウイルスワクチンが薬事承認。
3月
薬事・食品衛生審議会 医薬品第二部会において、以下の事項が了承された。
・効果の持続期間が長いモノクローナル抗体製剤であるニルセビマブ(nirsevimab)の、重症化リスク
の高い児のほか、生後初回のRSウイルス流行期のすべての新生児及び乳幼児等を対象とした承認。
・モノクローナル抗体製剤パリビズマブの適応に、肺低形成等の重症化リスクの高い5疾患を伴う24か月
齢以下の児を追加。
3月14日
第24回ワクチン評価小委員会においてRSウイルスワクチンの議論を開始。
・母子免疫について、疾病負荷は一定程度明らかであるが、安全性についての情報収集や、抗体製剤(ニ
ルセビマブ)の扱いが論点とされた。
・企業からのヒアリングを含め、各論点について検討を進める方針。
9月4日
第27回ワクチン評価小委員会にて母子免疫ワクチン・抗体製剤の企業ヒアリングを実施。
・乳幼児におけるRSウイルスの予防について、疾病負荷や母子免疫ワクチンおよび抗体製剤の有効性に
ついては一定の知見があるとされた。
・一方、ワクチン等の安全性については国内の知見が限定的であり、企業による安全性情報の収集が予定
されていることから引き続き国内の安全性に係る知見を収集し、ワクチン等の評価に必要な情報が一定
程度集積した段階でファクトシートの作成に進むこととされた。
11月21日
第28回ワクチン評価小委員会において、知見の一定の集積を踏まえ、疾病負荷、母子免疫ワクチン及び抗
体製剤の有効性・安全性、費用対効果について、ファクトシートの作成を国立感染症研究所に依頼し、そ
れを踏まえて再度議論を行うこととされた。
4