よむ、つかう、まなぶ。
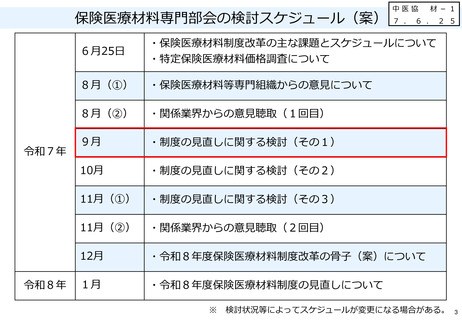
材ー1保険医療材料制度の見直しに関する検討(その1) (8 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_63930.html |
| 出典情報 | 中央社会保険医療協議会 保険医療材料専門部会(第131回 9/26)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
チャレンジ申請に関する累次の改定での対応
H30
R2
R4
R6
•
特定保険医療材料として評価される医療機器等を対象に、製品導入時には評価できなかった部分につ
いて、保険収載後に使用実績を踏まえて新規機能区分の該当性に係る再評価を行うことができる仕組
みとして「チャレンジ申請」を新設。
•
•
B1(既存機能区分)、B2(既存機能区分・変更あり)に対象を拡大。
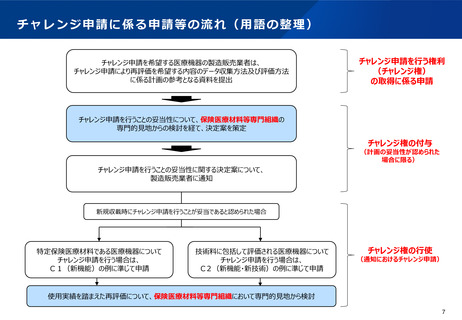
製造販売業者がチャレンジ権の付与を希望する場合には、保険収載後のデータ収集及び評価方法に係
る計画を具体的に提示することを求める。
チャレンジ権が付与された製品については、データ収集の進捗状況等について定期的な報告を求める。
データ収集が困難等の正当な理由がある場合は、チャレンジ権の放棄も可能とする。
保険収載時の評価を下回る結果が得られた場合には評価の見直しを検討する。
•
•
•
•
•
技術料に一体として包括して評価される医療機器等に対象を拡大。
チャレンジ権の付与を希望する際に希望書に記載するべき具体的な内容(データ収集及びその評価の
計画等)について明確化。
•
•
チャレンジ権の付与を希望する場合は、保険適用後1年間は申請可能とする。
チャレンジ申請による再評価は、チャレンジ申請を行うことが妥当であると判断された後に、製造販
売業者が関与の上で、前向きに収集したデータに基づくものに限られることとする。
体外診断用医薬品に対象を拡大。
•
8
H30
R2
R4
R6
•
特定保険医療材料として評価される医療機器等を対象に、製品導入時には評価できなかった部分につ
いて、保険収載後に使用実績を踏まえて新規機能区分の該当性に係る再評価を行うことができる仕組
みとして「チャレンジ申請」を新設。
•
•
B1(既存機能区分)、B2(既存機能区分・変更あり)に対象を拡大。
製造販売業者がチャレンジ権の付与を希望する場合には、保険収載後のデータ収集及び評価方法に係
る計画を具体的に提示することを求める。
チャレンジ権が付与された製品については、データ収集の進捗状況等について定期的な報告を求める。
データ収集が困難等の正当な理由がある場合は、チャレンジ権の放棄も可能とする。
保険収載時の評価を下回る結果が得られた場合には評価の見直しを検討する。
•
•
•
•
•
技術料に一体として包括して評価される医療機器等に対象を拡大。
チャレンジ権の付与を希望する際に希望書に記載するべき具体的な内容(データ収集及びその評価の
計画等)について明確化。
•
•
チャレンジ権の付与を希望する場合は、保険適用後1年間は申請可能とする。
チャレンジ申請による再評価は、チャレンジ申請を行うことが妥当であると判断された後に、製造販
売業者が関与の上で、前向きに収集したデータに基づくものに限られることとする。
体外診断用医薬品に対象を拡大。
•
8