よむ、つかう、まなぶ。
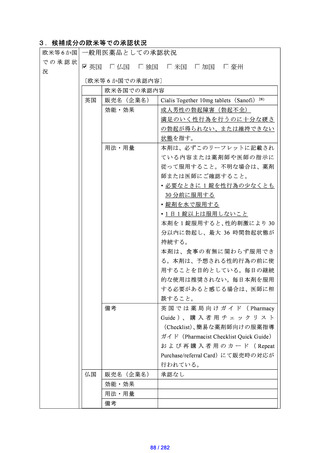
【資料2-1】成分情報等 (25 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_58149.html |
| 出典情報 | 医療用から要指導・一般用への転用に関する評価検討会議(第32回 5/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
27)Forgue ST, et al .:Br J Clin Pharmacol. 2007; 63(1): 24-35
28)社内資料:リトナビルとの薬物相互作用(2007年7月31日承認、
CTD 2.7.2.2.2.3.3)
29)社内資料:制酸剤及びH2受容体拮抗剤との薬物相互作用(2007年
7月31日承認、CTD 2.7.2.2.2.3.8)
30)社内資料:ミダゾラムとの薬物相互作用(2007年7月31日承認、
CTD 2.7.2.2.2.3.5)
31)社内資料:テオフィリンとの薬物相互作用(2007年7月31日承認、
CTD 2.7.2.2.2.3.7)
32)社内資料:ワルファリンとの薬物相互作用(タダラフィル10mg)
(2007年7月31日承認、CTD 2.7.2.2.2.3.6)
33)社内資料:ワルファリンとの薬物相互作用(タダラフィル20mg)
(2007年7月31日承認、CTD 2.7.2.2.2.3.6)
34)社内資料:アムロジピンとの薬物相互作用(2007年7月31日承認、
CTD 2.7.2.2.2.3.10)
35)Nagao K, et al .:Urology. 2006; 68(4): 845-851
36)Saenz de Tejada I, et al .:Int J Impot Res. 2002; 14(Suppl
4): S20
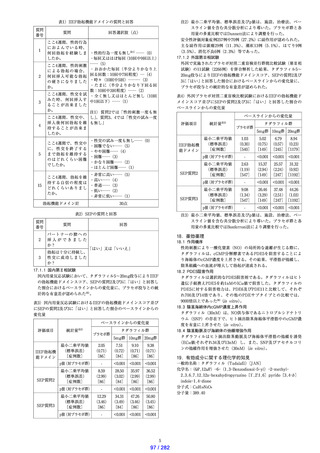
化学構造式:
性状:白色の粉末である。
ジメチルスルホキシドに溶けやすく、アセトニトリルにやや溶けに
くく、エタノール(99.5)に溶けにくく、水にほとんど溶けない。
分配係数:2.89(1-オクタノール/水系)
22. 包装
医療保険適用品
〈シアリス錠5mg〉
20錠[10錠(PTP)×2]
〈シアリス錠10mg〉
20錠[10錠(PTP)×2]
〈シアリス錠20mg〉
20錠[10錠(PTP)×2]
薬価基準未収載品
〈シアリス錠5mg〉
20錠[10錠(PTP)×2]
〈シアリス錠10mg〉
20錠[10錠(PTP)×2]、40錠[10錠(PTP)×4]
〈シアリス錠20mg〉
20錠[10錠(PTP)×2]、40錠[10錠(PTP)×4]
24. 文献請求先及び問い合わせ先
日本新薬株式会社 製品情報担当
〒601-8550 京都市南区吉祥院西ノ庄門口町14
フリーダイヤル0120-321-372
TEL 075-321-9064
FAX 075-321-9061
25. 保険給付上の注意
本製剤が「勃起不全による男性不妊」の治療目的で処方された場合
にのみ、保険給付の対象とする。
23. 主要文献
1)Kloner RA, et al .: Am J Cardiol. 2003; 92(Suppl):
37M-46M
2)Patterson D, et al .: Br J Clin Pharmacol. 2005; 60(5):
459-468
3)Kloner RA, et al .: J Am Coll Cardiol. 2003; 42(10):
1855-1860
4)社内資料:リトナビル及びケトコナゾールとの薬物相互作用
(2007年7月31日承認、CTD 2.7.2.2.2.3.2)
5)社内資料:リファンピシン及びケトコナゾールとの薬物相互作用
(2007年7月31日承認、CTD 2.7.2.2.2.3.1)
6)Kloner RA, et al .:J Urol. 2004; 172(5 Pt 1): 1935-1940
7)Kloner RA, et al .:Am J Cardiol. 2003; 92(Suppl): 47M-57M
8)Carson CC, et al .:BJU Int. 2004; 93(9): 1276-1281
9)Young JM, et al .:J Androl. 2005; 26(3): 310-318
10)Porst H, et al .:Urology. 2003; 62(1): 121-125
11)Pomeranz HD, et al .:J Neuroophthalmol. 2005; 25(1): 9-13
12)Lee AG, et al .:Am J Ophthalmol. 2005; 140(4): 707-708
13)Campbell UB, et al .:J Sex Med. 2015; 12(1): 139-151
14)Gilad R, et al .:BMJ. 2002; 325(7369): 869
15)Striano P, et al .:BMJ. 2006; 333(7572): 785
16)社内資料:アルコールとの薬物相互作用(タダラフィル
10mg)(2007年7月31日承認、CTD 2.7.2.2.2.3.9、CTD
2.7.2.2.2.4.7)
17)社内資料:アルコールとの薬物相互作用(タダラフィル
20mg)(2007年7月31日承認、CTD 2.7.2.2.2.3.9、CTD
2.7.2.2.2.4.7)
18)Hellstrom WJG, et al .:J Urol. 2003; 170(3): 887-891
19)社内資料:精液特性に及ぼす影響(2007年7月31日承認、CTD
2.7.4.4.3)
20)社内資料:健康成人における薬物動態(単回投与)(2007年7月31
日承認、CTD 2.7.2.2.2.1.1)
21)社内資料:健康成人における薬物動態(反復投与)(2007年7月31
日承認、CTD 2.7.2.2.2.1.2)
22)社内資料:食事の影響(2007年7月31日承認、CTD 2.7.1.3.2)
23)社内資料:蛋白結合(in vitro ;ラット、イヌ及びヒト血漿)(2007
年7月31日承認、CTD 2.6.4.4.3)
24)社内資料:蛋白結合(in vitro ;ヒト血漿蛋白)(2007年7月31日承
認、CTD 2.7.2.2.1.1)
25)社内資料:放射性標識体投与時の薬物動態(代謝)(2007年7月31
日承認、CTD 2.7.2.3.1.3)
26)社内資料:放射性標識体投与時の薬物動態(排泄)(2007年7月31
日承認、CTD 2.7.2.3.1.4)
26. 製造販売業者等
26.1 製造販売元
日本新薬株式会社
京都市南区吉祥院西ノ庄門口町14
シアリスⓇ及びCialisⓇは、米国イーライリリー・アンド・カンパニー
の登録商標です。
6
98 / 282
28)社内資料:リトナビルとの薬物相互作用(2007年7月31日承認、
CTD 2.7.2.2.2.3.3)
29)社内資料:制酸剤及びH2受容体拮抗剤との薬物相互作用(2007年
7月31日承認、CTD 2.7.2.2.2.3.8)
30)社内資料:ミダゾラムとの薬物相互作用(2007年7月31日承認、
CTD 2.7.2.2.2.3.5)
31)社内資料:テオフィリンとの薬物相互作用(2007年7月31日承認、
CTD 2.7.2.2.2.3.7)
32)社内資料:ワルファリンとの薬物相互作用(タダラフィル10mg)
(2007年7月31日承認、CTD 2.7.2.2.2.3.6)
33)社内資料:ワルファリンとの薬物相互作用(タダラフィル20mg)
(2007年7月31日承認、CTD 2.7.2.2.2.3.6)
34)社内資料:アムロジピンとの薬物相互作用(2007年7月31日承認、
CTD 2.7.2.2.2.3.10)
35)Nagao K, et al .:Urology. 2006; 68(4): 845-851
36)Saenz de Tejada I, et al .:Int J Impot Res. 2002; 14(Suppl
4): S20
化学構造式:
性状:白色の粉末である。
ジメチルスルホキシドに溶けやすく、アセトニトリルにやや溶けに
くく、エタノール(99.5)に溶けにくく、水にほとんど溶けない。
分配係数:2.89(1-オクタノール/水系)
22. 包装
医療保険適用品
〈シアリス錠5mg〉
20錠[10錠(PTP)×2]
〈シアリス錠10mg〉
20錠[10錠(PTP)×2]
〈シアリス錠20mg〉
20錠[10錠(PTP)×2]
薬価基準未収載品
〈シアリス錠5mg〉
20錠[10錠(PTP)×2]
〈シアリス錠10mg〉
20錠[10錠(PTP)×2]、40錠[10錠(PTP)×4]
〈シアリス錠20mg〉
20錠[10錠(PTP)×2]、40錠[10錠(PTP)×4]
24. 文献請求先及び問い合わせ先
日本新薬株式会社 製品情報担当
〒601-8550 京都市南区吉祥院西ノ庄門口町14
フリーダイヤル0120-321-372
TEL 075-321-9064
FAX 075-321-9061
25. 保険給付上の注意
本製剤が「勃起不全による男性不妊」の治療目的で処方された場合
にのみ、保険給付の対象とする。
23. 主要文献
1)Kloner RA, et al .: Am J Cardiol. 2003; 92(Suppl):
37M-46M
2)Patterson D, et al .: Br J Clin Pharmacol. 2005; 60(5):
459-468
3)Kloner RA, et al .: J Am Coll Cardiol. 2003; 42(10):
1855-1860
4)社内資料:リトナビル及びケトコナゾールとの薬物相互作用
(2007年7月31日承認、CTD 2.7.2.2.2.3.2)
5)社内資料:リファンピシン及びケトコナゾールとの薬物相互作用
(2007年7月31日承認、CTD 2.7.2.2.2.3.1)
6)Kloner RA, et al .:J Urol. 2004; 172(5 Pt 1): 1935-1940
7)Kloner RA, et al .:Am J Cardiol. 2003; 92(Suppl): 47M-57M
8)Carson CC, et al .:BJU Int. 2004; 93(9): 1276-1281
9)Young JM, et al .:J Androl. 2005; 26(3): 310-318
10)Porst H, et al .:Urology. 2003; 62(1): 121-125
11)Pomeranz HD, et al .:J Neuroophthalmol. 2005; 25(1): 9-13
12)Lee AG, et al .:Am J Ophthalmol. 2005; 140(4): 707-708
13)Campbell UB, et al .:J Sex Med. 2015; 12(1): 139-151
14)Gilad R, et al .:BMJ. 2002; 325(7369): 869
15)Striano P, et al .:BMJ. 2006; 333(7572): 785
16)社内資料:アルコールとの薬物相互作用(タダラフィル
10mg)(2007年7月31日承認、CTD 2.7.2.2.2.3.9、CTD
2.7.2.2.2.4.7)
17)社内資料:アルコールとの薬物相互作用(タダラフィル
20mg)(2007年7月31日承認、CTD 2.7.2.2.2.3.9、CTD
2.7.2.2.2.4.7)
18)Hellstrom WJG, et al .:J Urol. 2003; 170(3): 887-891
19)社内資料:精液特性に及ぼす影響(2007年7月31日承認、CTD
2.7.4.4.3)
20)社内資料:健康成人における薬物動態(単回投与)(2007年7月31
日承認、CTD 2.7.2.2.2.1.1)
21)社内資料:健康成人における薬物動態(反復投与)(2007年7月31
日承認、CTD 2.7.2.2.2.1.2)
22)社内資料:食事の影響(2007年7月31日承認、CTD 2.7.1.3.2)
23)社内資料:蛋白結合(in vitro ;ラット、イヌ及びヒト血漿)(2007
年7月31日承認、CTD 2.6.4.4.3)
24)社内資料:蛋白結合(in vitro ;ヒト血漿蛋白)(2007年7月31日承
認、CTD 2.7.2.2.1.1)
25)社内資料:放射性標識体投与時の薬物動態(代謝)(2007年7月31
日承認、CTD 2.7.2.3.1.3)
26)社内資料:放射性標識体投与時の薬物動態(排泄)(2007年7月31
日承認、CTD 2.7.2.3.1.4)
26. 製造販売業者等
26.1 製造販売元
日本新薬株式会社
京都市南区吉祥院西ノ庄門口町14
シアリスⓇ及びCialisⓇは、米国イーライリリー・アンド・カンパニー
の登録商標です。
6
98 / 282