よむ、つかう、まなぶ。
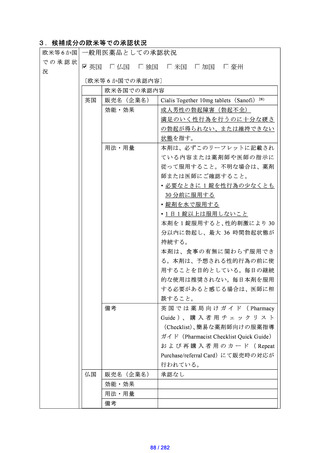
【資料2-1】成分情報等 (20 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_58149.html |
| 出典情報 | 医療用から要指導・一般用への転用に関する評価検討会議(第32回 5/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
**2024年11月改訂(第4版)
*2024年5月改訂(第3版)
貯法:室温保存
有効期間:3年
日本標準商品分類番号
87259
勃起不全治療剤
処方箋医薬品注)
タダラフィル錠
シアリス錠5mg シアリス錠10mg シアリス錠20mg
承認番号 21900AMX01084000 21900AMX01085000 21900AMX01086000
販売開始
2007年9月
2007年9月
2007年9月
Cialis® Tablets
注)注意-医師等の処方箋により使用すること
Z7
3.2 製剤の性状
1. 警告
1.1 本剤と硝酸剤又は一酸化窒素(NO)供与剤(ニトロ
グリセリン、亜硝酸アミル、硝酸イソソルビド、ニコラ
ンジル等)との併用により降圧作用が増強し、過度に血
圧を下降させることがあるので、本剤投与の前に、硝酸
剤又は一酸化窒素(NO)供与剤が投与されていないこ
とを十分確認し、本剤投与中及び投与後においても硝酸
剤又は一酸化窒素(NO)供与剤が投与されないよう十
分注意すること。[2.2、10.1参照]
1.2 死亡例を含む心筋梗塞等の重篤な心血管系等の有害事
象が報告されているので、本剤投与の前に、心血管系障
害の有無等を十分確認すること。
[2.4-2.8、8.1、11.2参照]
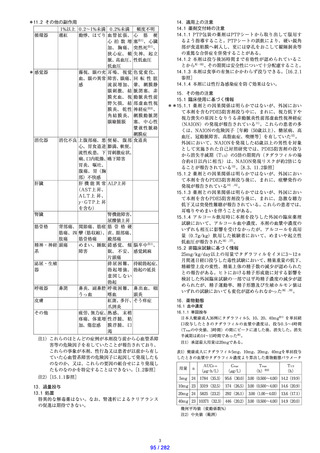
販売名
性状・剤形
外形
有効成分
添加剤
くすんだ黄色のフィルムコート錠
裏面
側面
寸法・重量
長径:約9.7mm
短径:約6.0mm
厚さ:約4.0mm
重量:約0.18g
長径:約11.0mm 長径:約12.3mm
短径:約6.8mm 短径:約7.6mm
厚さ:約4.5mm 厚さ:約5.0mm
重量:約0.26g
重量:約0.36g
識別コード
4. 効能又は効果
勃起不全(満足な性行為を行うに十分な勃起とその維持が
出来ない患者)
5. 効能又は効果に関連する注意
5.1 投与に際しては、勃起不全及びその基礎疾患の診断のた
め、既往歴の調査や諸検査を行い、客観的な診断に基づき
臨床上治療が必要とされる患者に限定すること。
5.2 本剤は催淫剤又は性欲増進剤ではない。
6. 用法及び用量
通常、成人には1日1回タダラフィルとして10mgを性行為
の約1時間前に経口投与する。10mgの投与で十分な効果が
得られず、忍容性が良好と判断された器質性又は混合型勃
起不全患者に対しては、20mgに増量することができる。
軽度又は中等度の肝障害のある患者では10mgを超えない
こと。なお、いずれの場合も1日の投与は1回とし、投与間
隔は24時間以上とすること。
中等度又は重度の腎障害のある患者では、5mgから開始
し、投与間隔は24時間以上とすること。なお、中等度の腎
障害のある患者では最高用量は10mgを超えないこととし、
10mgを投与する場合には投与間隔を48時間以上とするこ
と。重度の腎障害のある患者では5mgを超えないこと。
3. 組成・性状
3.1 組成
シアリス錠5mg
シアリス錠10mg シアリス錠20mg
表面
2. 禁忌(次の患者には投与しないこと)
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 硝酸剤又は一酸化窒素(NO)供与剤(ニトログリセ
リン、亜硝酸アミル、硝酸イソソルビド、ニコランジル
等)を投与中の患者[1.1、10.1参照]
2.3 可溶性グアニル酸シクラーゼ(sGC)刺激剤(リオシ
グアト)を投与中の患者[10.1参照]
2.4 心血管系障害を有するなど性行為が不適当と考えられ
る患者[1.2、8.1参照]
2.5 不安定狭心症のある患者又は性交中に狭心症を発現し
たことのある患者[1.2、8.1参照]
2.6 コ ン ト ロール 不 良 の 不 整 脈、 低 血 圧(血 圧<90/50
mmHg)又はコントロール不良の高血圧(安静時血圧
>170/100 mmHg)のある患者[1.2、8.1参照]
2.7 心筋梗塞の既往歴が最近3ヵ月以内にある患者[1.2、
8.1参照]
2.8 脳梗塞・脳出血の既往歴が最近6ヵ月以内にある患者
[1.2、8.1参照]
2.9 重度の肝障害のある患者[9.3.1参照]
2.10 網膜色素変性症患者[網膜色素変性症の患者にはホ
スホジエステラーゼ(PDE)の遺伝的障害を持つ症例
が少数認められる。]
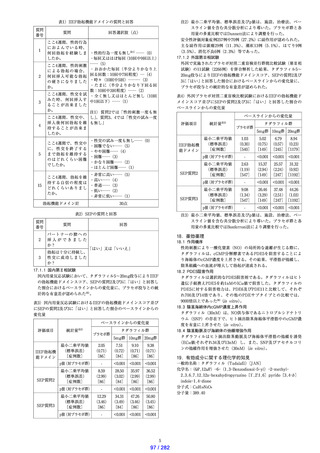
販売名
シアリス錠5mg
7. 用法及び用量に関連する注意
チトクロームP450 3A4(CYP3A4) を強く阻害する薬剤
を投与中の患者では、本剤の血漿中濃度が上昇することが
認められているので、低用量(5mg)から開始し、投与間
隔を十分にあける(10mgを投与する場合は投与間隔を48
時間以上) など注意して投与すること。 なお、 投与量は
10mgを超えないこと。[10.2参照]
シアリス錠10mg シアリス錠20mg
1錠中
1錠中
1錠中
タ ダ ラ フィル タ ダ ラ フィル タ ダ ラ フィル
5mg
10mg
20mg
乳糖水和物、結晶セルロース、クロスカルメロースナ
トリウム、ヒドロキシプロピルセルロース、ラウリル
硫酸ナトリウム、ステアリン酸マグネシウム、ヒプロ
メロース、酸化チタン、黄色三二酸化鉄、トリアセチ
ン、タルク
8. 重要な基本的注意
8.1 性行為は心臓へのリスクを伴うため勃起不全の治療を開
始する前に心血管系の状態に注意をはらうこと。[1.2、
2.4-2.8参照]
1
93 / 282
*2024年5月改訂(第3版)
貯法:室温保存
有効期間:3年
日本標準商品分類番号
87259
勃起不全治療剤
処方箋医薬品注)
タダラフィル錠
シアリス錠5mg シアリス錠10mg シアリス錠20mg
承認番号 21900AMX01084000 21900AMX01085000 21900AMX01086000
販売開始
2007年9月
2007年9月
2007年9月
Cialis® Tablets
注)注意-医師等の処方箋により使用すること
Z7
3.2 製剤の性状
1. 警告
1.1 本剤と硝酸剤又は一酸化窒素(NO)供与剤(ニトロ
グリセリン、亜硝酸アミル、硝酸イソソルビド、ニコラ
ンジル等)との併用により降圧作用が増強し、過度に血
圧を下降させることがあるので、本剤投与の前に、硝酸
剤又は一酸化窒素(NO)供与剤が投与されていないこ
とを十分確認し、本剤投与中及び投与後においても硝酸
剤又は一酸化窒素(NO)供与剤が投与されないよう十
分注意すること。[2.2、10.1参照]
1.2 死亡例を含む心筋梗塞等の重篤な心血管系等の有害事
象が報告されているので、本剤投与の前に、心血管系障
害の有無等を十分確認すること。
[2.4-2.8、8.1、11.2参照]
販売名
性状・剤形
外形
有効成分
添加剤
くすんだ黄色のフィルムコート錠
裏面
側面
寸法・重量
長径:約9.7mm
短径:約6.0mm
厚さ:約4.0mm
重量:約0.18g
長径:約11.0mm 長径:約12.3mm
短径:約6.8mm 短径:約7.6mm
厚さ:約4.5mm 厚さ:約5.0mm
重量:約0.26g
重量:約0.36g
識別コード
4. 効能又は効果
勃起不全(満足な性行為を行うに十分な勃起とその維持が
出来ない患者)
5. 効能又は効果に関連する注意
5.1 投与に際しては、勃起不全及びその基礎疾患の診断のた
め、既往歴の調査や諸検査を行い、客観的な診断に基づき
臨床上治療が必要とされる患者に限定すること。
5.2 本剤は催淫剤又は性欲増進剤ではない。
6. 用法及び用量
通常、成人には1日1回タダラフィルとして10mgを性行為
の約1時間前に経口投与する。10mgの投与で十分な効果が
得られず、忍容性が良好と判断された器質性又は混合型勃
起不全患者に対しては、20mgに増量することができる。
軽度又は中等度の肝障害のある患者では10mgを超えない
こと。なお、いずれの場合も1日の投与は1回とし、投与間
隔は24時間以上とすること。
中等度又は重度の腎障害のある患者では、5mgから開始
し、投与間隔は24時間以上とすること。なお、中等度の腎
障害のある患者では最高用量は10mgを超えないこととし、
10mgを投与する場合には投与間隔を48時間以上とするこ
と。重度の腎障害のある患者では5mgを超えないこと。
3. 組成・性状
3.1 組成
シアリス錠5mg
シアリス錠10mg シアリス錠20mg
表面
2. 禁忌(次の患者には投与しないこと)
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 硝酸剤又は一酸化窒素(NO)供与剤(ニトログリセ
リン、亜硝酸アミル、硝酸イソソルビド、ニコランジル
等)を投与中の患者[1.1、10.1参照]
2.3 可溶性グアニル酸シクラーゼ(sGC)刺激剤(リオシ
グアト)を投与中の患者[10.1参照]
2.4 心血管系障害を有するなど性行為が不適当と考えられ
る患者[1.2、8.1参照]
2.5 不安定狭心症のある患者又は性交中に狭心症を発現し
たことのある患者[1.2、8.1参照]
2.6 コ ン ト ロール 不 良 の 不 整 脈、 低 血 圧(血 圧<90/50
mmHg)又はコントロール不良の高血圧(安静時血圧
>170/100 mmHg)のある患者[1.2、8.1参照]
2.7 心筋梗塞の既往歴が最近3ヵ月以内にある患者[1.2、
8.1参照]
2.8 脳梗塞・脳出血の既往歴が最近6ヵ月以内にある患者
[1.2、8.1参照]
2.9 重度の肝障害のある患者[9.3.1参照]
2.10 網膜色素変性症患者[網膜色素変性症の患者にはホ
スホジエステラーゼ(PDE)の遺伝的障害を持つ症例
が少数認められる。]
販売名
シアリス錠5mg
7. 用法及び用量に関連する注意
チトクロームP450 3A4(CYP3A4) を強く阻害する薬剤
を投与中の患者では、本剤の血漿中濃度が上昇することが
認められているので、低用量(5mg)から開始し、投与間
隔を十分にあける(10mgを投与する場合は投与間隔を48
時間以上) など注意して投与すること。 なお、 投与量は
10mgを超えないこと。[10.2参照]
シアリス錠10mg シアリス錠20mg
1錠中
1錠中
1錠中
タ ダ ラ フィル タ ダ ラ フィル タ ダ ラ フィル
5mg
10mg
20mg
乳糖水和物、結晶セルロース、クロスカルメロースナ
トリウム、ヒドロキシプロピルセルロース、ラウリル
硫酸ナトリウム、ステアリン酸マグネシウム、ヒプロ
メロース、酸化チタン、黄色三二酸化鉄、トリアセチ
ン、タルク
8. 重要な基本的注意
8.1 性行為は心臓へのリスクを伴うため勃起不全の治療を開
始する前に心血管系の状態に注意をはらうこと。[1.2、
2.4-2.8参照]
1
93 / 282