よむ、つかう、まなぶ。
「医薬品等の副作用等の報告について」の一部改正について (36 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000190382_00010.html |
| 出典情報 | 薬事・食品衛生審議会 医療機器・再生医療等製品安全対策部会(令和3年度第2回 3/16)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
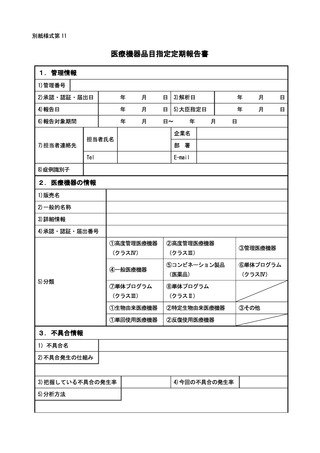
別紙様式第 11
医療機器品目指定定期報告書
1.管理情報
1)管理番号
2)承認・認証・届出日
年
月
日 3)解析日
年
月
日
4)報告日
年
月
日 5)大臣指定日
年
月
日
6)報告対象期間
年
月
日~
年
月
日
企業名
担当者氏名
7)担当者連絡先
部 署
Tel
E-mail
8)症例識別子
2.医療機器の情報
1)販売名
2)一般的名称
3)詳細情報
4)承認・認証・届出番号
①高度管理医療機器
②高度管理医療機器
(クラスⅣ)
(クラスⅢ)
④一般医療機器
5)分類
⑤コンビネーション製品
⑥単体プログラム
(医薬品)
(クラスⅣ)
⑦単体プログラム
⑧単体プログラム
(クラスⅢ)
(クラスⅡ)
①生物由来医療機器
②特定生物由来医療機器
①単回使用医療機器
②反復使用医療機器
3.不具合情報
1)不具合名
2)不具合発生の仕組み
3)把握している不具合の発生率
5)分析方法
③管理医療機器
4)今回の不具合の発生率
③その他
医療機器品目指定定期報告書
1.管理情報
1)管理番号
2)承認・認証・届出日
年
月
日 3)解析日
年
月
日
4)報告日
年
月
日 5)大臣指定日
年
月
日
6)報告対象期間
年
月
日~
年
月
日
企業名
担当者氏名
7)担当者連絡先
部 署
Tel
8)症例識別子
2.医療機器の情報
1)販売名
2)一般的名称
3)詳細情報
4)承認・認証・届出番号
①高度管理医療機器
②高度管理医療機器
(クラスⅣ)
(クラスⅢ)
④一般医療機器
5)分類
⑤コンビネーション製品
⑥単体プログラム
(医薬品)
(クラスⅣ)
⑦単体プログラム
⑧単体プログラム
(クラスⅢ)
(クラスⅡ)
①生物由来医療機器
②特定生物由来医療機器
①単回使用医療機器
②反復使用医療機器
3.不具合情報
1)不具合名
2)不具合発生の仕組み
3)把握している不具合の発生率
5)分析方法
③管理医療機器
4)今回の不具合の発生率
③その他