よむ、つかう、まなぶ。
資料2-3 外国での新たな措置の報告状況 (55 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_24331.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和3年度 第3回 3/11)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
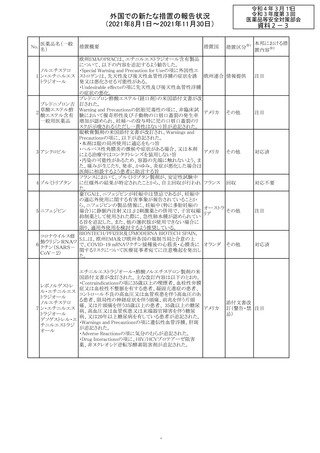
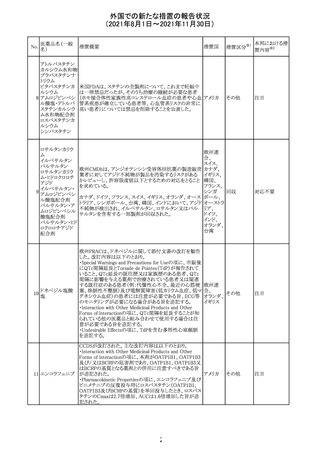
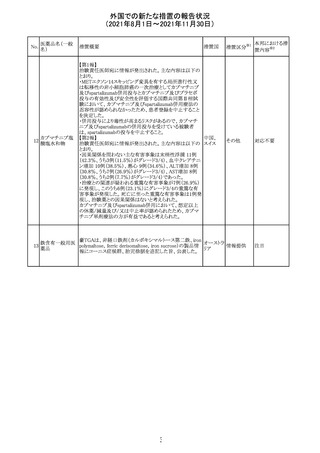
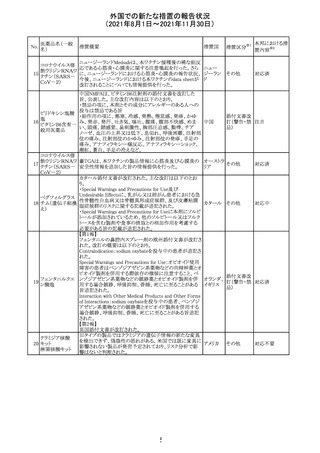
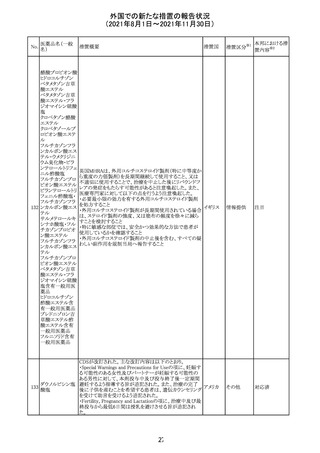
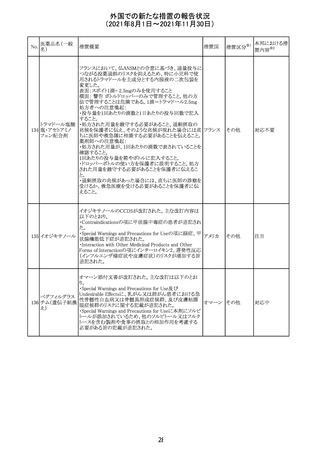
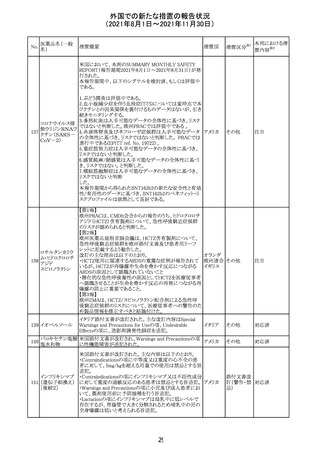
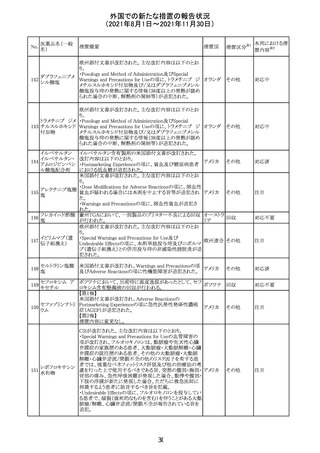
外国での新たな措置の報告状況
(2021年8月1日~2021年11月30日)
No.
291
292
本邦における措
※2
置内容
医薬品名(一般
名)
措置概要
タクロリムス水和
物
アイルランド添付文書が改訂された。主な内容は以下のと
おり。
・Special Warnings and Precautions for Useに、本剤が腎障
害を引き起こす可能性がある旨、腎障害のある患者では減
量が必要な可能性がある旨、適切なモニタリングが必要な
胸、腎毒性を持つ薬剤との併用は避けるべきであり、併用
する際は注意深いモニタリングが必要な旨が追記された。
・Special Warnings and Precautions for Use及びInteraction
with Other Medicinal Products and Other Forms of
Interactionsに、CYP3A4の強力な阻害剤又はCYP3A4の誘
導物質をタクロリムスと併用する場合の注意が追記された。
アイルラ
・Special Warnings and Precautions for Useの賦形剤の項
ンド
に、乳糖が含まれているため、ガラクトース不耐症、総ラク
ターゼ欠乏症、又はブドウ糖-ガラクトース吸収不良などの
まれな遺伝性の問題がある患者では注意が必要な旨が追
記された。
・Special Warnings and Precautions for Useの賦形剤の項
に、含まれるエタノール含有量が記載された。
・Undesirable Effectsに、可逆性高白質脳症症候群が追記
された。
・Special Precautions for Disposalに本剤の調整中の皮膚、
粘膜、吸入暴露を避ける必要があり、そのような曝露があっ
た場合は洗い流す必要がある旨が追記された。
その他
注目
タクロリムス水和
物
欧州添付文書が改訂された。主な内容は以下のとおり。
・Special Warnings and Precautions for Useに、本剤が腎障
害を引き起こす可能性がある旨、腎障害のある患者では減
量が必要な可能性がある旨、適切なモニタリングが必要な
胸、腎毒性を持つ薬剤との併用は避けるべきであり、併用
する際は注意深いモニタリングが必要な旨が追記された。
・Special Warnings and Precautions for Use及びInteraction
with Other Medicinal Products and Other Forms of
Interactionsに、CYP3A4の強力な阻害剤又はCYP3A4の誘
導物質をタクロリムスと併用する場合の注意が追記された。
・Special Warnings and Precautions for Useの賦形剤の項
欧州連合 その他
に、乳糖が含まれているため、ガラクトース不耐症、総ラク
ターゼ欠乏症、又はブドウ糖-ガラクトース吸収不良などの
まれな遺伝性の問題がある患者では注意が必要な旨が追
記された。
・Special Warnings and Precautions for Useの賦形剤の項
に、含まれるエタノール含有量が記載された。
・Undesirable Effectsに、可逆性高白質脳症症候群が追記
された。
・Special Precautions for Disposal に本剤の調整中の皮
膚、粘膜、吸入暴露を避ける必要があり、そのような曝露が
あった場合は洗い流す必要がある旨が追記された。
注目
措置国
措置区分
※1
製造販売後臨床試験の成績が得られたことに伴い、CDS
ゲムツズマブオゾ のUndesirable Effects(静脈閉塞性肝疾患、感染症、出血、
293 ガマイシン(遺伝 免疫原性)、
アメリカ
子組換え)
Pharmacodynamic Properties及びPharmacokinetic
Propertiesの項が更新された。
その他
サリチル酸メチル 米国FDAのSrLCにて、サリチル酸メチルを含有する製剤に
294 含有一般用医薬 ついて、妊娠中の女性は医師からの指示がない限り使用し アメリカ
品
ないことの記載に「妊娠20週以降」が追記された。
添付文書改
訂(警告・禁 対応不要
忌)
55
対応不要
(2021年8月1日~2021年11月30日)
No.
291
292
本邦における措
※2
置内容
医薬品名(一般
名)
措置概要
タクロリムス水和
物
アイルランド添付文書が改訂された。主な内容は以下のと
おり。
・Special Warnings and Precautions for Useに、本剤が腎障
害を引き起こす可能性がある旨、腎障害のある患者では減
量が必要な可能性がある旨、適切なモニタリングが必要な
胸、腎毒性を持つ薬剤との併用は避けるべきであり、併用
する際は注意深いモニタリングが必要な旨が追記された。
・Special Warnings and Precautions for Use及びInteraction
with Other Medicinal Products and Other Forms of
Interactionsに、CYP3A4の強力な阻害剤又はCYP3A4の誘
導物質をタクロリムスと併用する場合の注意が追記された。
アイルラ
・Special Warnings and Precautions for Useの賦形剤の項
ンド
に、乳糖が含まれているため、ガラクトース不耐症、総ラク
ターゼ欠乏症、又はブドウ糖-ガラクトース吸収不良などの
まれな遺伝性の問題がある患者では注意が必要な旨が追
記された。
・Special Warnings and Precautions for Useの賦形剤の項
に、含まれるエタノール含有量が記載された。
・Undesirable Effectsに、可逆性高白質脳症症候群が追記
された。
・Special Precautions for Disposalに本剤の調整中の皮膚、
粘膜、吸入暴露を避ける必要があり、そのような曝露があっ
た場合は洗い流す必要がある旨が追記された。
その他
注目
タクロリムス水和
物
欧州添付文書が改訂された。主な内容は以下のとおり。
・Special Warnings and Precautions for Useに、本剤が腎障
害を引き起こす可能性がある旨、腎障害のある患者では減
量が必要な可能性がある旨、適切なモニタリングが必要な
胸、腎毒性を持つ薬剤との併用は避けるべきであり、併用
する際は注意深いモニタリングが必要な旨が追記された。
・Special Warnings and Precautions for Use及びInteraction
with Other Medicinal Products and Other Forms of
Interactionsに、CYP3A4の強力な阻害剤又はCYP3A4の誘
導物質をタクロリムスと併用する場合の注意が追記された。
・Special Warnings and Precautions for Useの賦形剤の項
欧州連合 その他
に、乳糖が含まれているため、ガラクトース不耐症、総ラク
ターゼ欠乏症、又はブドウ糖-ガラクトース吸収不良などの
まれな遺伝性の問題がある患者では注意が必要な旨が追
記された。
・Special Warnings and Precautions for Useの賦形剤の項
に、含まれるエタノール含有量が記載された。
・Undesirable Effectsに、可逆性高白質脳症症候群が追記
された。
・Special Precautions for Disposal に本剤の調整中の皮
膚、粘膜、吸入暴露を避ける必要があり、そのような曝露が
あった場合は洗い流す必要がある旨が追記された。
注目
措置国
措置区分
※1
製造販売後臨床試験の成績が得られたことに伴い、CDS
ゲムツズマブオゾ のUndesirable Effects(静脈閉塞性肝疾患、感染症、出血、
293 ガマイシン(遺伝 免疫原性)、
アメリカ
子組換え)
Pharmacodynamic Properties及びPharmacokinetic
Propertiesの項が更新された。
その他
サリチル酸メチル 米国FDAのSrLCにて、サリチル酸メチルを含有する製剤に
294 含有一般用医薬 ついて、妊娠中の女性は医師からの指示がない限り使用し アメリカ
品
ないことの記載に「妊娠20週以降」が追記された。
添付文書改
訂(警告・禁 対応不要
忌)
55
対応不要