よむ、つかう、まなぶ。
参考資料3 RevMate Ver.6.2 (16 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_25755.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和4年度第4回 5/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
※1
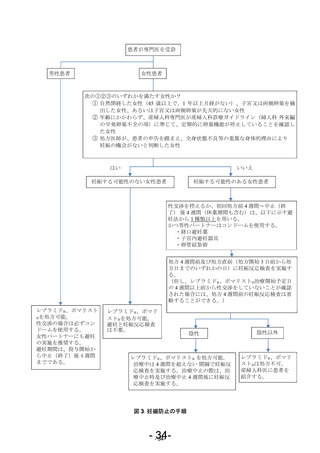
処方開始 3 日前から処方日までのいずれかの日。
※2
尿検査:25mIU/mL の感度以上とし、判定は各医療機関の基準に従う。
血液検査:検査項目は β-HCG 又は HCG とし、判定は各医療機関の基準に従う。
・ また、すべての患者に対し、血液検査等を実施し、血液毒性等の発現に注意する。
11.1.4. 患者へのカウンセリング
・ 処方医師は、患者に対し、RevMate®の遵守事項に関する説明やレブラミド®、ポマリスト®
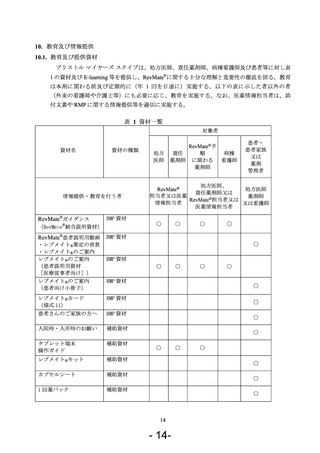
によって発現する可能性のある催奇形性等に関して「10.教育及び情報提供」の表 1 資材一
覧に示す資材を用いて説明し、注意喚起を行う。
・ 処方医師は、「RevMate®遵守状況確認票(様式 20~22)」にて、カウンセリング内容に漏
れがないか確認し、医師確認欄にチェックする。
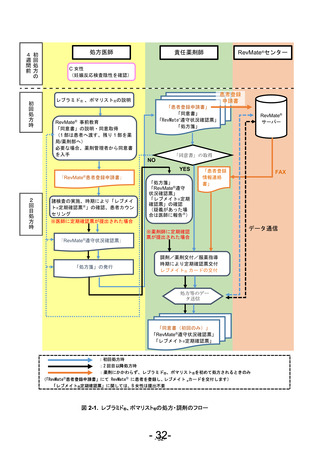
11.1.5. 処方箋の発行
① 処方医師は、レブラミド®、ポマリスト®処方時に「RevMate®遵守状況確認票(様式 20~
22)」を用いた患者カウンセリングや妊娠反応検査等の結果等に全く問題がなく、当該患
者に対しレブラミド®、ポマリスト®の処方が適切と判断した場合のみ、必要な数量の薬剤
を処方する。
② 処方医師は処方箋と共に「RevMate®患者登録申請書(様式 9)」、「レブラミド®・ポマリ
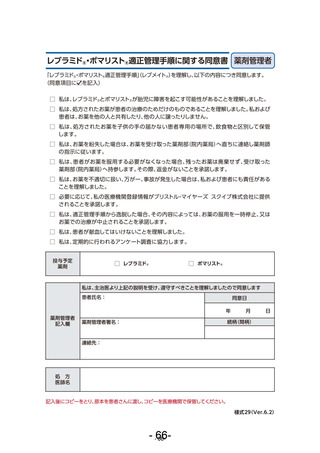
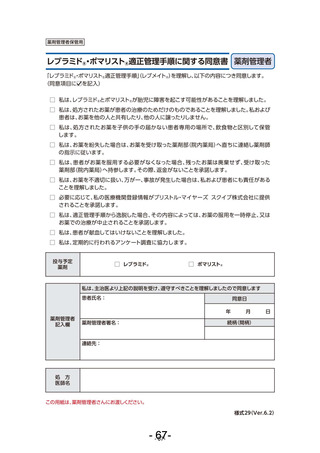
スト®治療に関する同意書(様式 17~19)」及び「レブラミド®・ポマリスト®適正管理手
順に関する同意書(薬剤管理者)(様式 29)」が責任薬剤師に提出されるよう取り計らう。
(タブレット端末を利用しない場合、「RevMate®遵守状況確認票(様式 20~22)」も併せ
て責任薬剤師へ提出されるよう取り計らう。)
11.1.6. 患者の登録(RevMate®センター)
• 責任薬剤師は、初回調剤時までに RevMate®センターに患者登録を実施する。
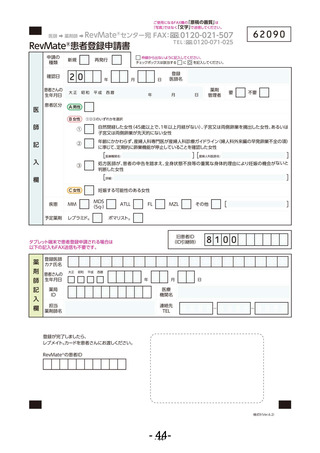
• 責任薬剤師は、「RevMate®患者登録申請書(様式 9)」に不備がないか確認し、医療機関名、
担当薬剤師名、連絡先を記入後、RevMate®センターにタブレット端末で送信する。
• RevMate®センターは、登録を承認後、「RevMate®患者登録情報連絡書(様式 10)」を責任
薬剤師に FAX 等で返信する。
11.1.7. 責任薬剤師による疑義照会
責任薬剤師は「RevMate®患者登録申請書(様式 9)」、「レブラミド®・ポマリスト®治療に
関する同意書(様式 17~19)」、「レブラミド®・ポマリスト®適正管理手順に関する同意書
(薬剤管理者)(様式 29)」及び「RevMate®遵守状況確認票(様式 20~22)」に入力(記入)
された内容に不備等が見つかった場合は、必ず処方医師に疑義照会する。
11.1.8. 調剤時の確認
① 責任薬剤師は、「RevMate®患者登録情報連絡書(様式 10)」を受領後、「レブラミド®・ポ
マリスト®治療に関する同意書(様式 17~19)」、「レブラミド®・ポマリスト®適正管理手
順に関する同意書(薬剤管理者)(様式 29)」及び「RevMate® 遵守状況確認票(様式 20~
22)」の処方医師の入力(記入)内容及び処方箋の内容を確認するとともに、薬剤管理に関
する必要な説明を行う。
② 責任薬剤師は、「RevMate®遵守状況確認票(様式 20~22)」に必要事項を入力(記入)、
16
- 16-
処方開始 3 日前から処方日までのいずれかの日。
※2
尿検査:25mIU/mL の感度以上とし、判定は各医療機関の基準に従う。
血液検査:検査項目は β-HCG 又は HCG とし、判定は各医療機関の基準に従う。
・ また、すべての患者に対し、血液検査等を実施し、血液毒性等の発現に注意する。
11.1.4. 患者へのカウンセリング
・ 処方医師は、患者に対し、RevMate®の遵守事項に関する説明やレブラミド®、ポマリスト®
によって発現する可能性のある催奇形性等に関して「10.教育及び情報提供」の表 1 資材一
覧に示す資材を用いて説明し、注意喚起を行う。
・ 処方医師は、「RevMate®遵守状況確認票(様式 20~22)」にて、カウンセリング内容に漏
れがないか確認し、医師確認欄にチェックする。
11.1.5. 処方箋の発行
① 処方医師は、レブラミド®、ポマリスト®処方時に「RevMate®遵守状況確認票(様式 20~
22)」を用いた患者カウンセリングや妊娠反応検査等の結果等に全く問題がなく、当該患
者に対しレブラミド®、ポマリスト®の処方が適切と判断した場合のみ、必要な数量の薬剤
を処方する。
② 処方医師は処方箋と共に「RevMate®患者登録申請書(様式 9)」、「レブラミド®・ポマリ
スト®治療に関する同意書(様式 17~19)」及び「レブラミド®・ポマリスト®適正管理手
順に関する同意書(薬剤管理者)(様式 29)」が責任薬剤師に提出されるよう取り計らう。
(タブレット端末を利用しない場合、「RevMate®遵守状況確認票(様式 20~22)」も併せ
て責任薬剤師へ提出されるよう取り計らう。)
11.1.6. 患者の登録(RevMate®センター)
• 責任薬剤師は、初回調剤時までに RevMate®センターに患者登録を実施する。
• 責任薬剤師は、「RevMate®患者登録申請書(様式 9)」に不備がないか確認し、医療機関名、
担当薬剤師名、連絡先を記入後、RevMate®センターにタブレット端末で送信する。
• RevMate®センターは、登録を承認後、「RevMate®患者登録情報連絡書(様式 10)」を責任
薬剤師に FAX 等で返信する。
11.1.7. 責任薬剤師による疑義照会
責任薬剤師は「RevMate®患者登録申請書(様式 9)」、「レブラミド®・ポマリスト®治療に
関する同意書(様式 17~19)」、「レブラミド®・ポマリスト®適正管理手順に関する同意書
(薬剤管理者)(様式 29)」及び「RevMate®遵守状況確認票(様式 20~22)」に入力(記入)
された内容に不備等が見つかった場合は、必ず処方医師に疑義照会する。
11.1.8. 調剤時の確認
① 責任薬剤師は、「RevMate®患者登録情報連絡書(様式 10)」を受領後、「レブラミド®・ポ
マリスト®治療に関する同意書(様式 17~19)」、「レブラミド®・ポマリスト®適正管理手
順に関する同意書(薬剤管理者)(様式 29)」及び「RevMate® 遵守状況確認票(様式 20~
22)」の処方医師の入力(記入)内容及び処方箋の内容を確認するとともに、薬剤管理に関
する必要な説明を行う。
② 責任薬剤師は、「RevMate®遵守状況確認票(様式 20~22)」に必要事項を入力(記入)、
16
- 16-