よむ、つかう、まなぶ。
【資料01】薬事審議会規程の改正について[497KB] (22 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71799.html |
| 出典情報 | 薬事審議会(令和7年度第5回 3/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
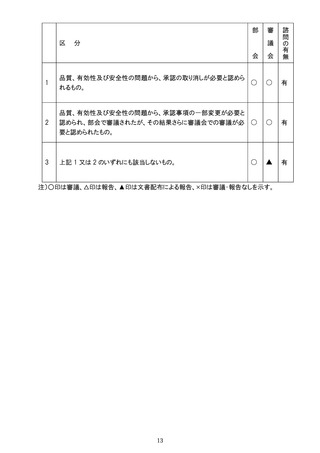
部会報告なし、審議会報告なし、諮問なし。
7の2~17 略
(旧)
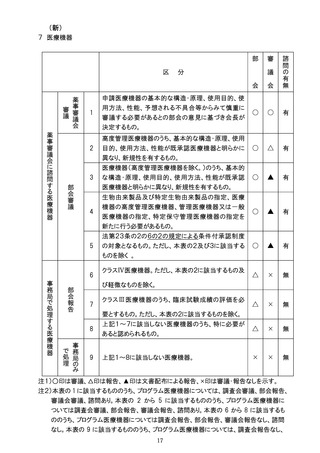
7 医療機器
部
会
会
諮
問
の
有
無
○
○
有
2
高度管理医療機器のうち、基本的な構造・原理、使用
目的、使用方法、性能が既承認医療機器と明らかに
異なり、新規性を有するもの。
○
△
有
3
医療機器(高度管理医療機器を除く。)のうち、基本的
な構造・原理、使用目的、使用方法、性能が既承認
医療機器と明らかに異なり、新規性を有するもの。
○
▲
有
○
▲
有
○
▲
有
△
×
無
△
×
無
区
薬
事
審 審
議 議
会
薬
事
審
議
会
に
諮
問
す
る
医
療
機
器
部
会
審
議
1
事
で 務
処 局
理 の
み
用方法、性能、予想される不具合等からみて慎重に
審議する必要があるとの部会の意見に基づき会長が
決定するもの。
生物由来製品及び特定生物由来製品の指定、医療
4
6
部
会
報
告
議
申請医療機器の基本的な構造・原理、使用目的、使
5
事
務
局
で
処
理
す
る
医
療
機
器
分
審
機器の高度管理医療機器、管理医療機器又は一般
医療機器の指定、特定保守管理医療機器の指定を
新たに行う必要があるもの。
法第23条の2の5第5項に基づき、臨床試験の試験
成績に関する資料の一部の提出を要しないとするもの
(条件付き承認制度の対象となるもの)の承認の際に
付する条件に関する事項。ただし、本表の2及び3に該
当するものを除く 。
クラスⅣ医療機器。ただし、本表の2に該当するもの及
び軽微なものを除く。
7
クラスⅢ医療機器のうち、臨床試験成績の評価を必
要とするもの。ただし、本表の2に該当するものを除く。
8
上記1~7に該当しない医療機器のうち、特に必要が
あると認められるもの。
△
×
無
9
上記1~8に該当しない医療機器。
×
×
無
18
7の2~17 略
(旧)
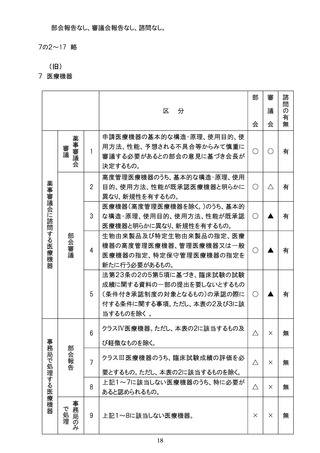
7 医療機器
部
会
会
諮
問
の
有
無
○
○
有
2
高度管理医療機器のうち、基本的な構造・原理、使用
目的、使用方法、性能が既承認医療機器と明らかに
異なり、新規性を有するもの。
○
△
有
3
医療機器(高度管理医療機器を除く。)のうち、基本的
な構造・原理、使用目的、使用方法、性能が既承認
医療機器と明らかに異なり、新規性を有するもの。
○
▲
有
○
▲
有
○
▲
有
△
×
無
△
×
無
区
薬
事
審 審
議 議
会
薬
事
審
議
会
に
諮
問
す
る
医
療
機
器
部
会
審
議
1
事
で 務
処 局
理 の
み
用方法、性能、予想される不具合等からみて慎重に
審議する必要があるとの部会の意見に基づき会長が
決定するもの。
生物由来製品及び特定生物由来製品の指定、医療
4
6
部
会
報
告
議
申請医療機器の基本的な構造・原理、使用目的、使
5
事
務
局
で
処
理
す
る
医
療
機
器
分
審
機器の高度管理医療機器、管理医療機器又は一般
医療機器の指定、特定保守管理医療機器の指定を
新たに行う必要があるもの。
法第23条の2の5第5項に基づき、臨床試験の試験
成績に関する資料の一部の提出を要しないとするもの
(条件付き承認制度の対象となるもの)の承認の際に
付する条件に関する事項。ただし、本表の2及び3に該
当するものを除く 。
クラスⅣ医療機器。ただし、本表の2に該当するもの及
び軽微なものを除く。
7
クラスⅢ医療機器のうち、臨床試験成績の評価を必
要とするもの。ただし、本表の2に該当するものを除く。
8
上記1~7に該当しない医療機器のうち、特に必要が
あると認められるもの。
△
×
無
9
上記1~8に該当しない医療機器。
×
×
無
18