よむ、つかう、まなぶ。
【資料01】薬事審議会規程の改正について[497KB] (14 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71799.html |
| 出典情報 | 薬事審議会(令和7年度第5回 3/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
上記の1~4のいずれにも該当しないもの、又は承認
事項の一部変更が必要と認められるものであって、当
5
該変更について行政上緊急に措置をとる必要がない
もの(例えば、効能・効果の名称を現在の医学・薬学
的常識から判断して適当なものに変更するもの)。
△
×
無
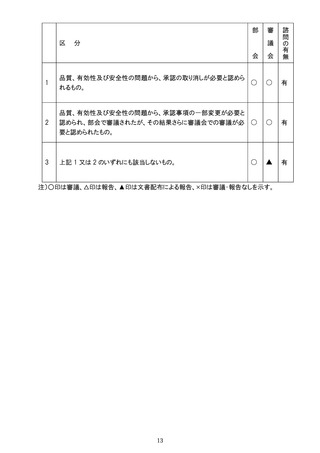
注)○印は審議、△印は報告、▲印は文書配布による報告、×印は審議・報告なしを示す。
1の3 条件付承認した医療用医薬品(体外診断用医薬品を除く)の中間評価
部
会
会
諮
問
の
有
無
1
品質、有効性及び安全性の問題から、承認の取り消しが必要と認めら
○
れるもの。
○
有
2
品質、有効性及び安全性の問題から、承認事項の一部変更が必要と
認められ、部会で審議されたが、その結果さらに審議会での審議が必 ○
要と認められたもの。
○
有
3
上記 1 又は 2 のいずれにも該当しないもの。
○
▲
有
区
分
審
議
注)○印は審議、△印は報告、▲印は文書配布による報告、×印は審議・報告なしを示す。
10
事項の一部変更が必要と認められるものであって、当
5
該変更について行政上緊急に措置をとる必要がない
もの(例えば、効能・効果の名称を現在の医学・薬学
的常識から判断して適当なものに変更するもの)。
△
×
無
注)○印は審議、△印は報告、▲印は文書配布による報告、×印は審議・報告なしを示す。
1の3 条件付承認した医療用医薬品(体外診断用医薬品を除く)の中間評価
部
会
会
諮
問
の
有
無
1
品質、有効性及び安全性の問題から、承認の取り消しが必要と認めら
○
れるもの。
○
有
2
品質、有効性及び安全性の問題から、承認事項の一部変更が必要と
認められ、部会で審議されたが、その結果さらに審議会での審議が必 ○
要と認められたもの。
○
有
3
上記 1 又は 2 のいずれにも該当しないもの。
○
▲
有
区
分
審
議
注)○印は審議、△印は報告、▲印は文書配布による報告、×印は審議・報告なしを示す。
10