よむ、つかう、まなぶ。
核酸等を用いる医療技術を用いて行われる再生医療等に関する再生医療等提供計画に添付する「提供する再生医療等の詳細を記した書類」に記載及び添付が必要な事項について[510KB] (14 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_58780.html |
| 出典情報 | 厚生科学審議会 再生医療等評価部会(第107回 5/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
別紙2
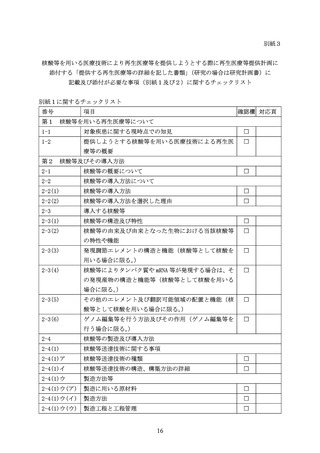
核酸等を用いる医療技術により再生医療等を提供しようとする際に再生医療等提供計画に
添付する「提供する再生医療等の詳細を記した書類」(研究の場合は研究計画書)に
添付が必要な資料及びその内容について
核酸等を用いる医療技術により再生医療等を提供しようとする際には、別紙1の記載事項
の詳細を示した下記の文書を添付すること。
記
第1
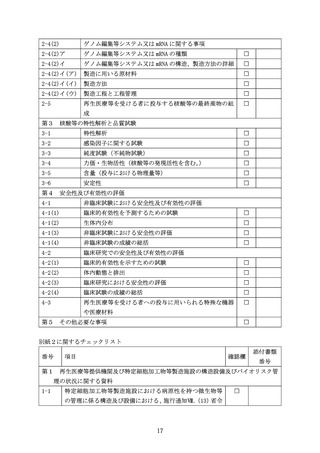
再生医療等提供機関及び特定細胞加工物等製造施設の構造設備及びバイオリスク管
理の状況に関する以下の事項に係る資料
1
特定細胞加工物等製造施設における病原性を持つ微生物等の管理に係る構造及び
設備における、施行通知Ⅶ.(13)省令第 89 条第 13 号関係及び施行通知Ⅶ.(14)
省令 89 条第 15 号関係に関する事項
2
特定細胞加工物等製造施設におけるバイオセーフティ及びバイオセキュリティの
規程に関する事項
第2
再生医療等提供機関における当該再生医療等又はそれに類似する再生医療等に関す
る有効性を示す又は示唆する試験及び安全性に関する以下の研究成果がある場合には、
当該試験及び研究の成果※1※2に係る資料
1
培養細胞や実験動物を用いた研究の成果
2
研究の概要に加え、培養細胞における遺伝子導入又はゲノム編集等の効率、導入遺
伝子の発現又はゲノム編集等により生じた変化とその持続性、導入遺伝子又はゲノ
ム編集等により発現したタンパク質等の機能等についての詳細な研究成果
3
臨床研究における有効性の示唆、又は安全性の担保に関し、研究機関等で得られて
いる詳細なデータ及びその総括
4
第3
関連する研究成果についての投稿論文等の情報
再生医療等提供機関以外において、国内外で実施されている当該核酸等又はそれに類
似したものを用いた医療技術に関する研究又は医療の提供の状況に係る資料
第4
遺伝子組換え生物等の使用等の規制による生物の多様性の確保に関する法律(平成 15
年法律第 97 号)に規定される遺伝子組換え生物等を用いる場合であって、その第一種
使用規程が承認されていない場合には、
「再生医療等の安全性の確保等に関する法律に
基づく再生医療等に関連した「遺伝子組換え生物等の使用等の規制による生物の多様性
の確保に関する法律」に基づく手続等について」
(令和7年5月 30 日付け医政研発 0530
第1号厚生労働省医政局研究開発政策課長通知)に示された提出予定の第一種使用規程
申請書、生物多様性影響評価書及びその他の文書(申請書等)
第5
その他必要な以下の事項に係る資料※2
14
核酸等を用いる医療技術により再生医療等を提供しようとする際に再生医療等提供計画に
添付する「提供する再生医療等の詳細を記した書類」(研究の場合は研究計画書)に
添付が必要な資料及びその内容について
核酸等を用いる医療技術により再生医療等を提供しようとする際には、別紙1の記載事項
の詳細を示した下記の文書を添付すること。
記
第1
再生医療等提供機関及び特定細胞加工物等製造施設の構造設備及びバイオリスク管
理の状況に関する以下の事項に係る資料
1
特定細胞加工物等製造施設における病原性を持つ微生物等の管理に係る構造及び
設備における、施行通知Ⅶ.(13)省令第 89 条第 13 号関係及び施行通知Ⅶ.(14)
省令 89 条第 15 号関係に関する事項
2
特定細胞加工物等製造施設におけるバイオセーフティ及びバイオセキュリティの
規程に関する事項
第2
再生医療等提供機関における当該再生医療等又はそれに類似する再生医療等に関す
る有効性を示す又は示唆する試験及び安全性に関する以下の研究成果がある場合には、
当該試験及び研究の成果※1※2に係る資料
1
培養細胞や実験動物を用いた研究の成果
2
研究の概要に加え、培養細胞における遺伝子導入又はゲノム編集等の効率、導入遺
伝子の発現又はゲノム編集等により生じた変化とその持続性、導入遺伝子又はゲノ
ム編集等により発現したタンパク質等の機能等についての詳細な研究成果
3
臨床研究における有効性の示唆、又は安全性の担保に関し、研究機関等で得られて
いる詳細なデータ及びその総括
4
第3
関連する研究成果についての投稿論文等の情報
再生医療等提供機関以外において、国内外で実施されている当該核酸等又はそれに類
似したものを用いた医療技術に関する研究又は医療の提供の状況に係る資料
第4
遺伝子組換え生物等の使用等の規制による生物の多様性の確保に関する法律(平成 15
年法律第 97 号)に規定される遺伝子組換え生物等を用いる場合であって、その第一種
使用規程が承認されていない場合には、
「再生医療等の安全性の確保等に関する法律に
基づく再生医療等に関連した「遺伝子組換え生物等の使用等の規制による生物の多様性
の確保に関する法律」に基づく手続等について」
(令和7年5月 30 日付け医政研発 0530
第1号厚生労働省医政局研究開発政策課長通知)に示された提出予定の第一種使用規程
申請書、生物多様性影響評価書及びその他の文書(申請書等)
第5
その他必要な以下の事項に係る資料※2
14