よむ、つかう、まなぶ。
1 先進医療Aに係る新規技術の科学的評価等について(別紙1)[3.0MB] (19 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00106.html |
| 出典情報 | 先進医療会議(第144回 6/5)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
【別添3】
「進行または再発した固形がん患者に対して標準治療終了前に実施す
る包括的ゲノムプロファイリング検査」の被験者の適格基準及び選
定方法(申請書類より抜粋)
5.被験者の適格基準及び選定方法
以下の適格規準をすべて満たす患者を登録適格例とする。
適格規準
1)
病理学的診断によって悪性腫瘍と診断されていること。
2)
全身薬物療法の対象となる進行または再発の病期であること。
3)
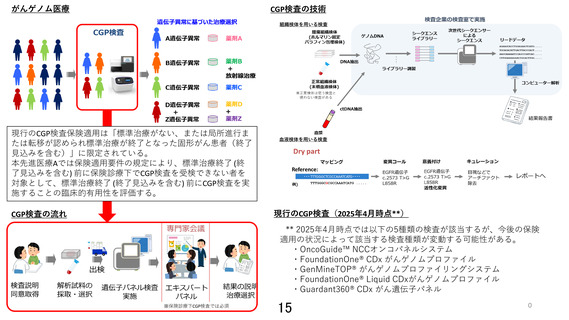
保険適用下の CGP 検査を未施行であること。
4)
研究参加時点において現行の CGP 検査が保険適用外であると担当医が判断していること。
5)
遺伝子解析が可能な検体(①②のいずれか 1 つ以上)が提出できる。
①診療後残余腫瘍組織試料
②本研究のために新たに採取される末梢血液試料
6)
がんゲノム情報管理センター(C-CAT)へ患者情報を登録し、データが利活用されることに同意し
ていること。
7)
本研究の参加について患者本人から文書で同意が得られていること(18 歳未満の患者は、本人か
らの同意に加え、代諾者の同意を必須とする)。ただし、説明の内容を理解し、同意の意志があっても、神
経症状などにより患者本人の署名が困難でありかつ患者本人が希望する場合には、患者本人の同意の確認
の署名を代筆者が行っても良い。
除外規準
1)
既に本研究に参加し、先進医療 A の枠組みの下で CGP 検査を受検したことがある被験者
19
「進行または再発した固形がん患者に対して標準治療終了前に実施す
る包括的ゲノムプロファイリング検査」の被験者の適格基準及び選
定方法(申請書類より抜粋)
5.被験者の適格基準及び選定方法
以下の適格規準をすべて満たす患者を登録適格例とする。
適格規準
1)
病理学的診断によって悪性腫瘍と診断されていること。
2)
全身薬物療法の対象となる進行または再発の病期であること。
3)
保険適用下の CGP 検査を未施行であること。
4)
研究参加時点において現行の CGP 検査が保険適用外であると担当医が判断していること。
5)
遺伝子解析が可能な検体(①②のいずれか 1 つ以上)が提出できる。
①診療後残余腫瘍組織試料
②本研究のために新たに採取される末梢血液試料
6)
がんゲノム情報管理センター(C-CAT)へ患者情報を登録し、データが利活用されることに同意し
ていること。
7)
本研究の参加について患者本人から文書で同意が得られていること(18 歳未満の患者は、本人か
らの同意に加え、代諾者の同意を必須とする)。ただし、説明の内容を理解し、同意の意志があっても、神
経症状などにより患者本人の署名が困難でありかつ患者本人が希望する場合には、患者本人の同意の確認
の署名を代筆者が行っても良い。
除外規準
1)
既に本研究に参加し、先進医療 A の枠組みの下で CGP 検査を受検したことがある被験者
19