よむ、つかう、まなぶ。
1 先進医療Aに係る新規技術の科学的評価等について(別紙1)[3.0MB] (16 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00106.html |
| 出典情報 | 先進医療会議(第144回 6/5)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
保険収載までのロードマップ
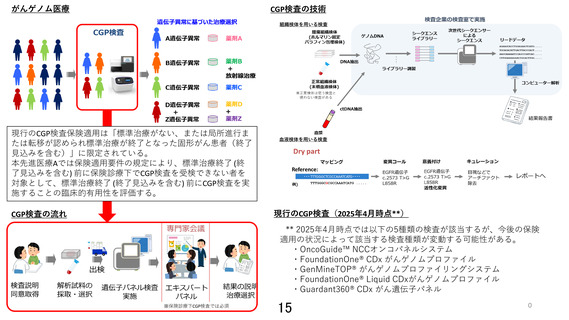
先進医療技術名:標準治療終了 (終了見込みを含む) 前の包括的ゲノムプロファイリング(CGP)検査
先進医療での適応症:保険適用要件の規定により、標準治療終了 (終了見込みを含む) 前に保険診療下
でCGP検査を受検できない固形腫瘍
臨床研究
・ 試験名:NCCH1908(UPFRONT試験)
・ 試験デザイン:単群前向き研究
・ 期間:令和2年6月~令和6年9月
・ 被験者数:201例
・ 結果の概要:
-192 例でCGP 検査を実施し、観察期間中央値は19.4 ヶ月。
-Actionable 遺伝子異常は全体の57.6% で認めた。
-actionableな遺伝子異常に対応する分子標的治療を受けた
患者の割合は7.3%(コンパニオン診断を除く)だった。
-全体の生存期間中央値は24.3 ヶ月(95% CI: 20.2-30.9)だった。
-重篤な有害事象の報告はない。
当該先進医療における
選択基準
1)全身薬物療法の対象となる進行再発の固形腫瘍
2)研究参加時点において現行のCGP検査が保険適用外で
あると担当医が判断している
3)C-CATへ患者情報を登録し、学術利用目的にデータが
利活用されることに同意している
除外基準
先進医療Aの枠組みの下でCGP検査を受検したことがあ
る被験者
予想される有害事象:重篤な有害事象の想定はない
関連する技術等の本邦での保険適用の状況
2025年4月時点、「標準治療がない、または局所進行または
転移が認められ標準治療が終了となった固形がん患者(終了
見込みを含む)」に対して保険適用となっている。
先進医療
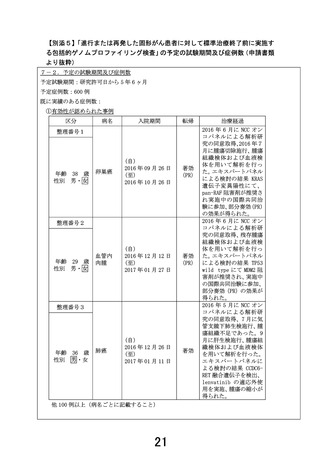
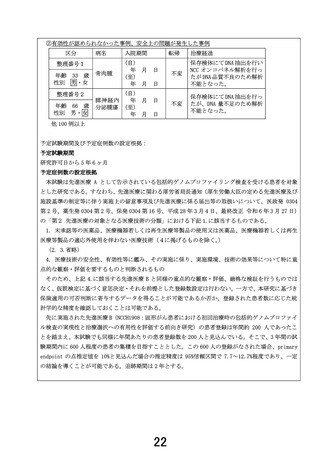
・ 試験名:進行または再発した固形がん患者に対して標準治療終了前に
実施するCGP検査の臨床的有用性を評価する前向き研究
・ 試験デザイン:単群前向き研究
・ 期間:令和7年7月~令和13年1月
・ 主要評価項目:本試験で実施したCGP検査結果で検出された治療標的と
なる遺伝子異常(=actionableな遺伝子異常)に対応する分子標的治療を
受ける患者の割合(コンパニオン診断を含む)
・ 副次評価項目:
(1) 本試験で実施したCGP検査結果で検出された
-actionableな遺伝子異常に対応する分子標的治療が推奨された患者の
割合(コンパニオン診断を含む)
-actionableな遺伝子異常に対応する分子標的治療を行う治験への登録
割合
-診断に有用な遺伝子異常が検出された患者の割合
(2) 全生存期間
海外での現状
保険適用:米国(有)、英国(有)、ドイツ(有)、カナダ(有)
ガイドライン記載:(有)
海外ではCGP検査の実施時期に関する制限はなく、NCCN(米)をはじめとし
たガイドラインでも、治療開始前(=診断直後)に NGSベースのCGP検査を
実施することが推奨されている。
進行中の臨床試験(無)
本邦での現状
ガイドライン記載:(無)
進行中の臨床試験: (無)
16
保
険
収
載
先進医療技術名:標準治療終了 (終了見込みを含む) 前の包括的ゲノムプロファイリング(CGP)検査
先進医療での適応症:保険適用要件の規定により、標準治療終了 (終了見込みを含む) 前に保険診療下
でCGP検査を受検できない固形腫瘍
臨床研究
・ 試験名:NCCH1908(UPFRONT試験)
・ 試験デザイン:単群前向き研究
・ 期間:令和2年6月~令和6年9月
・ 被験者数:201例
・ 結果の概要:
-192 例でCGP 検査を実施し、観察期間中央値は19.4 ヶ月。
-Actionable 遺伝子異常は全体の57.6% で認めた。
-actionableな遺伝子異常に対応する分子標的治療を受けた
患者の割合は7.3%(コンパニオン診断を除く)だった。
-全体の生存期間中央値は24.3 ヶ月(95% CI: 20.2-30.9)だった。
-重篤な有害事象の報告はない。
当該先進医療における
選択基準
1)全身薬物療法の対象となる進行再発の固形腫瘍
2)研究参加時点において現行のCGP検査が保険適用外で
あると担当医が判断している
3)C-CATへ患者情報を登録し、学術利用目的にデータが
利活用されることに同意している
除外基準
先進医療Aの枠組みの下でCGP検査を受検したことがあ
る被験者
予想される有害事象:重篤な有害事象の想定はない
関連する技術等の本邦での保険適用の状況
2025年4月時点、「標準治療がない、または局所進行または
転移が認められ標準治療が終了となった固形がん患者(終了
見込みを含む)」に対して保険適用となっている。
先進医療
・ 試験名:進行または再発した固形がん患者に対して標準治療終了前に
実施するCGP検査の臨床的有用性を評価する前向き研究
・ 試験デザイン:単群前向き研究
・ 期間:令和7年7月~令和13年1月
・ 主要評価項目:本試験で実施したCGP検査結果で検出された治療標的と
なる遺伝子異常(=actionableな遺伝子異常)に対応する分子標的治療を
受ける患者の割合(コンパニオン診断を含む)
・ 副次評価項目:
(1) 本試験で実施したCGP検査結果で検出された
-actionableな遺伝子異常に対応する分子標的治療が推奨された患者の
割合(コンパニオン診断を含む)
-actionableな遺伝子異常に対応する分子標的治療を行う治験への登録
割合
-診断に有用な遺伝子異常が検出された患者の割合
(2) 全生存期間
海外での現状
保険適用:米国(有)、英国(有)、ドイツ(有)、カナダ(有)
ガイドライン記載:(有)
海外ではCGP検査の実施時期に関する制限はなく、NCCN(米)をはじめとし
たガイドラインでも、治療開始前(=診断直後)に NGSベースのCGP検査を
実施することが推奨されている。
進行中の臨床試験(無)
本邦での現状
ガイドライン記載:(無)
進行中の臨床試験: (無)
16
保
険
収
載