よむ、つかう、まなぶ。
「再生医療等の安全性の確保等に関する法律及び臨床研究法の一部を改正する法律」の施行について (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_57618.html |
| 出典情報 | 厚生科学審議会 再生医療等評価部会(第106回 5/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
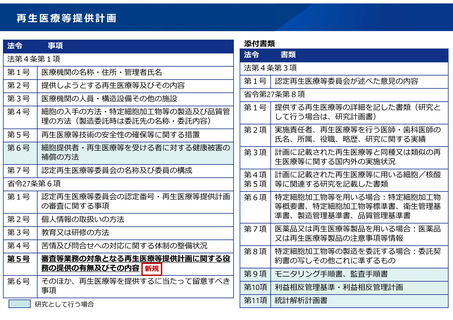
再生医療等提供計画
法令
事項
法第4条第1項
第1号
医療機関の名称・住所・管理者氏名
第2号
提供しようとする再生医療等及びその内容
第3号
医療機関の人員・構造設備その他の施設
第4号
細胞の入手の方法・特定細胞加工物等の製造及び品質管
理の方法(製造委託時は委託先の名称・委託内容)
第5号
再生医療等技術の安全性の確保等に関する措置
第6号
細胞提供者・再生医療等を受ける者に対する健康被害の
補償の方法
第7号
認定再生医療等委員会の名称及び委員の構成
省令27条第6項
第1号
認定再生医療等委員会の認定番号・再生医療等提供計画
の審査に関する事項
第2号
個人情報の取扱いの方法
第3号
教育又は研修の方法
第4号
苦情及び問合せへの対応に関する体制の整備状況
第5号
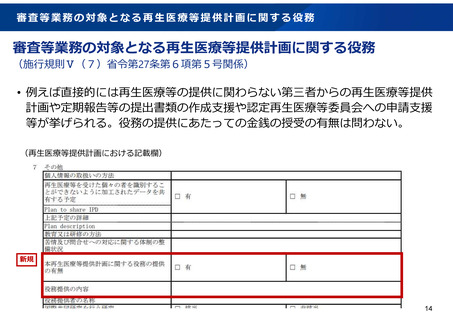
審査等業務の対象となる再生医療等提供計画に関する役
務の提供の有無及びその内容 新規
第6号
そのほか、再生医療等を提供するに当たって留意すべき
事項
研究として行う場合
添付書類
法令
書類
法第4条第3項
第1号
認定再生医療等委員会が述べた意見の内容
省令第27条第8項
第1号
提供する再生医療等の詳細を記した書類(研究と
して行う場合は、研究計画書)
第2項
実施責任者、再生医療等を行う医師・歯科医師の
氏名、所属、役職、略歴、研究に関する実績
第3項
計画に記載された再生医療等と同種又は類似の再
生医療等に関する国内外の実施状況
第4項
第5項
計画に記載された再生医療等に用いる細胞/核酸
等に関連する研究を記載した書類
第6項
特定細胞加工物等を用いる場合:特定細胞加工物
等概要書、特定細胞加工物等標準書、衛生管理基
準書、製造管理基準書、品質管理基準書
第7項
医薬品又は再生医療等製品を用いる場合:医薬品
又は再生医療等製品の注意事項等情報
第8項
特定細胞加工物等の製造を委託する場合:委託契
約書の写しその他これに準ずるもの
第9項
モニタリング手順書、監査手順書
第10項 利益相反管理基準・利益相反管理計画
第11項 統計解析計画書
13
法令
事項
法第4条第1項
第1号
医療機関の名称・住所・管理者氏名
第2号
提供しようとする再生医療等及びその内容
第3号
医療機関の人員・構造設備その他の施設
第4号
細胞の入手の方法・特定細胞加工物等の製造及び品質管
理の方法(製造委託時は委託先の名称・委託内容)
第5号
再生医療等技術の安全性の確保等に関する措置
第6号
細胞提供者・再生医療等を受ける者に対する健康被害の
補償の方法
第7号
認定再生医療等委員会の名称及び委員の構成
省令27条第6項
第1号
認定再生医療等委員会の認定番号・再生医療等提供計画
の審査に関する事項
第2号
個人情報の取扱いの方法
第3号
教育又は研修の方法
第4号
苦情及び問合せへの対応に関する体制の整備状況
第5号
審査等業務の対象となる再生医療等提供計画に関する役
務の提供の有無及びその内容 新規
第6号
そのほか、再生医療等を提供するに当たって留意すべき
事項
研究として行う場合
添付書類
法令
書類
法第4条第3項
第1号
認定再生医療等委員会が述べた意見の内容
省令第27条第8項
第1号
提供する再生医療等の詳細を記した書類(研究と
して行う場合は、研究計画書)
第2項
実施責任者、再生医療等を行う医師・歯科医師の
氏名、所属、役職、略歴、研究に関する実績
第3項
計画に記載された再生医療等と同種又は類似の再
生医療等に関する国内外の実施状況
第4項
第5項
計画に記載された再生医療等に用いる細胞/核酸
等に関連する研究を記載した書類
第6項
特定細胞加工物等を用いる場合:特定細胞加工物
等概要書、特定細胞加工物等標準書、衛生管理基
準書、製造管理基準書、品質管理基準書
第7項
医薬品又は再生医療等製品を用いる場合:医薬品
又は再生医療等製品の注意事項等情報
第8項
特定細胞加工物等の製造を委託する場合:委託契
約書の写しその他これに準ずるもの
第9項
モニタリング手順書、監査手順書
第10項 利益相反管理基準・利益相反管理計画
第11項 統計解析計画書
13