よむ、つかう、まなぶ。
資料5-2 令和3年度医薬品等自主回収一覧 (31 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26332.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第1回 6/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
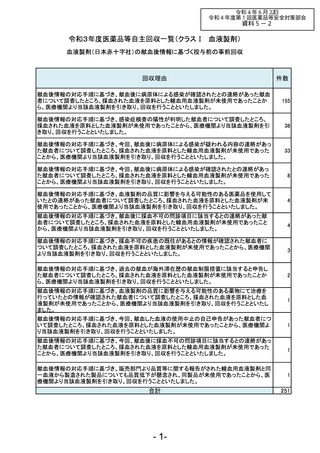
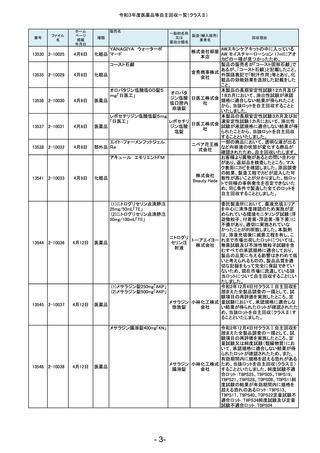
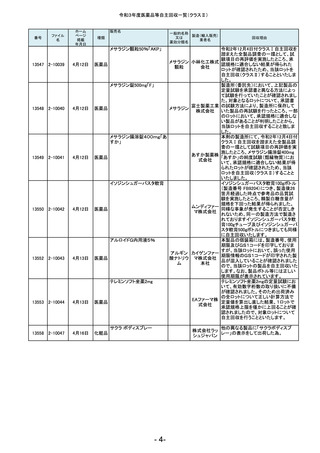
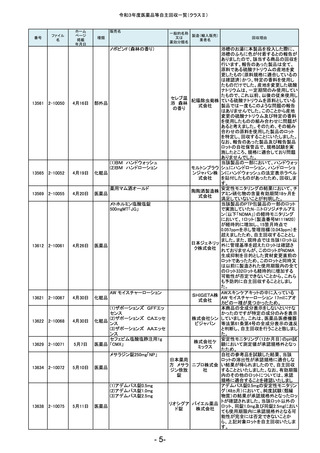
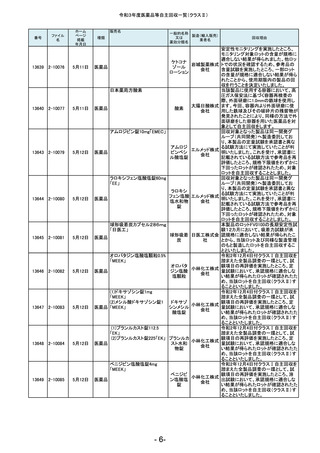
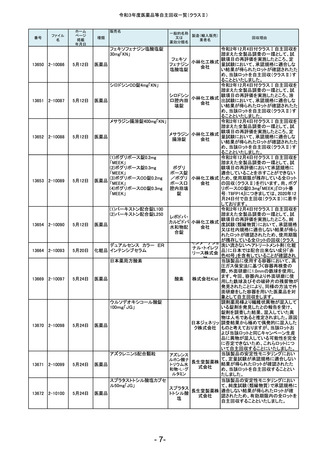
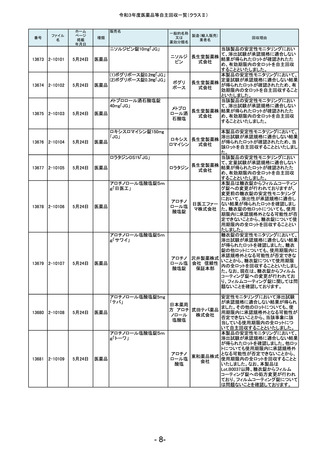
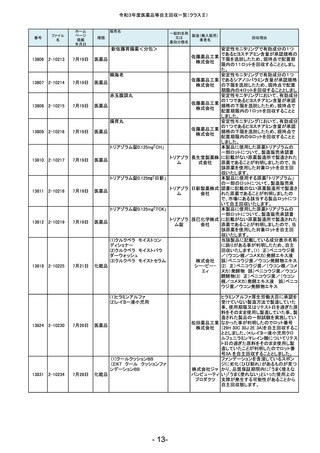
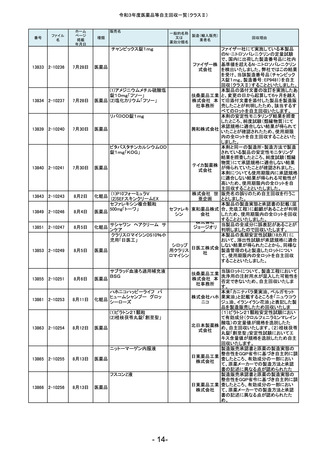
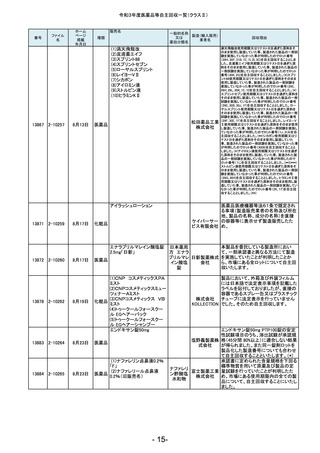
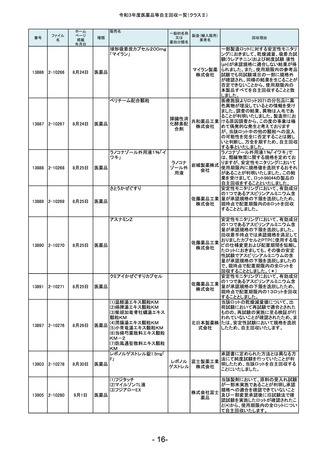
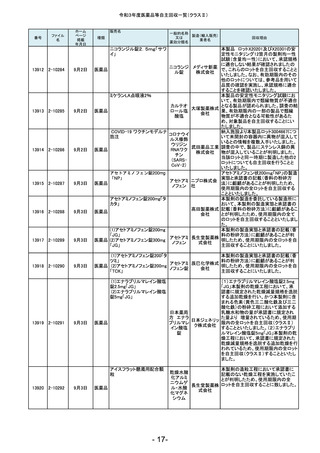
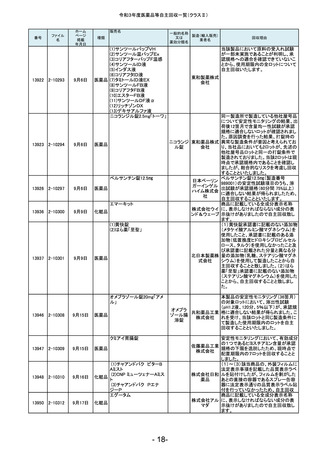
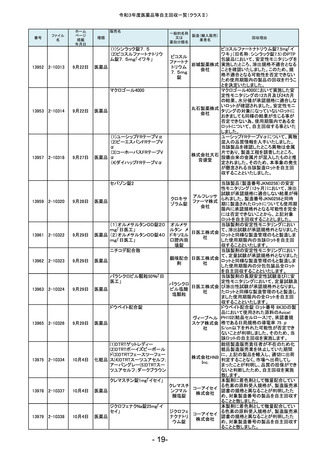
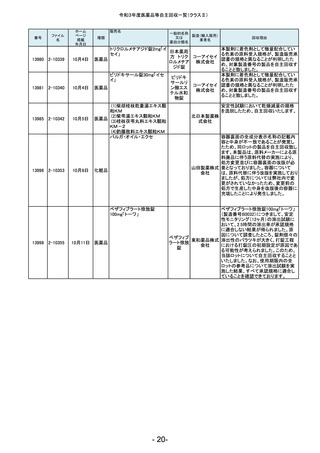
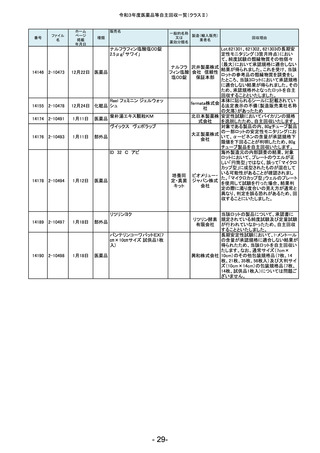
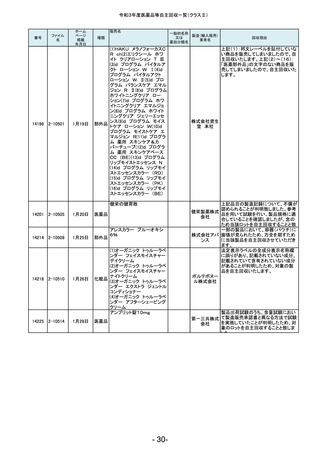
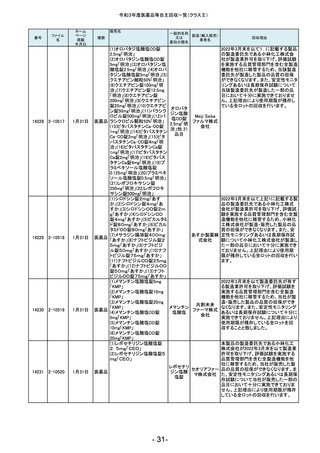
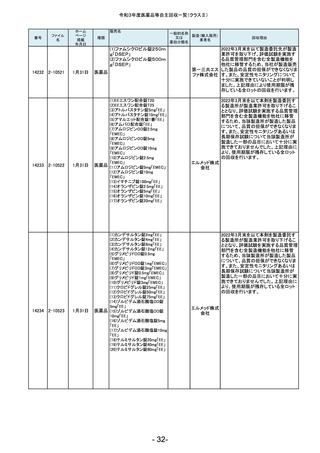
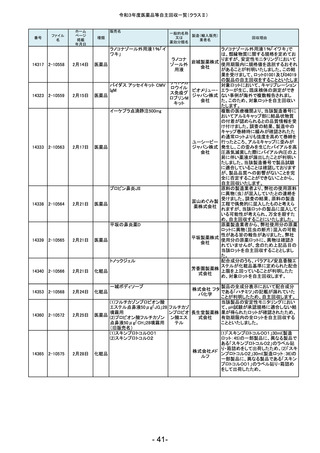
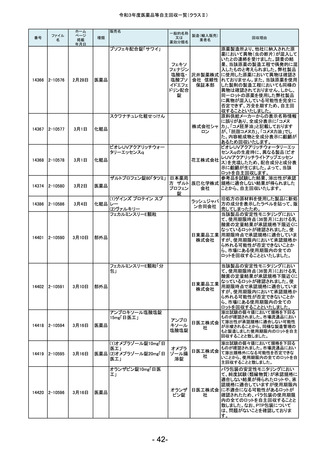
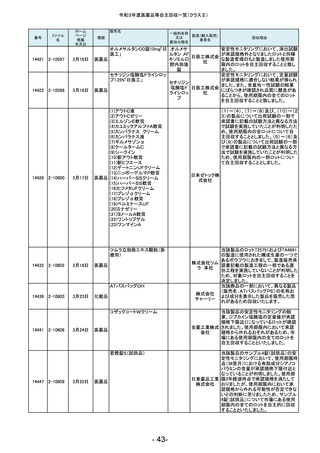
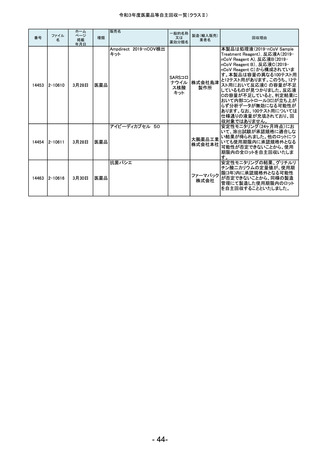
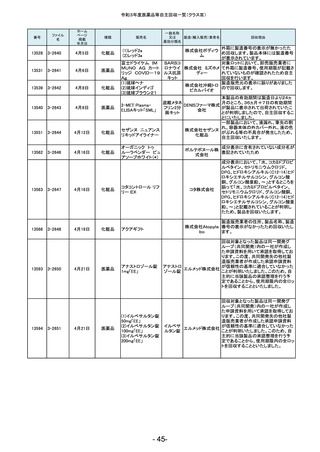
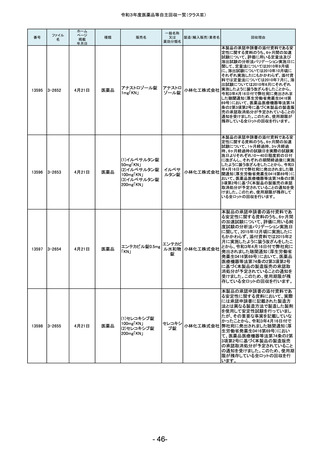
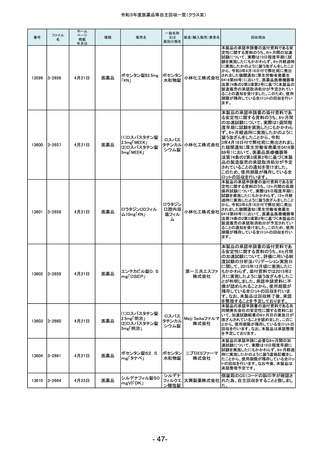
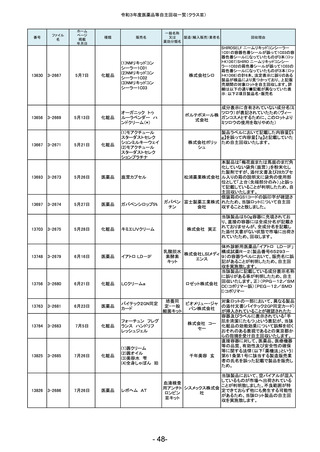
令和3年度医薬品等自主回収一覧(クラスⅡ)
番号
ファイル
名
14228 2-10517
14229 2-10518
14230 2-10519
14231 2-10520
ホーム
ページ
掲載
年月日
1月31日
1月31日
1月31日
1月31日
販売名
一般的名称
製造(輸入販売)
又は
業者名
薬効分類名
種類
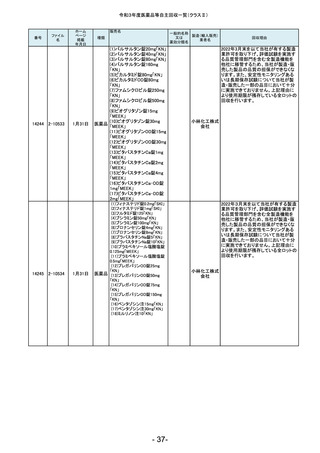
(1)オロパタジ塩酸塩OD錠
2.5mg「明治」
(2)オロパタジン塩酸塩OD錠
5mg「明治」(3)オロパタジン塩
酸塩錠2.5mg「明治」(4)オロパ
タジン塩酸塩錠5mg「明治」(5)
クエチアピン細粒50%「明治」
(6)クエチアピン錠100mg「明
治」(7)クエチアピン錠12.5mg
「明治」(8)クエチアピン錠
200mg「明治」(9)クエチアピン
錠25mg「明治」(10)クエチアピ
ン錠50mg「明治」(11)バラシク
ロビル錠500mg「明治」(12)バ
医薬品 ラシクロビル顆粒50%「明治」
(13)ピタバスタチンCa・OD錠
1mg「明治」(14)ピタバスタチン
Ca・OD錠2mg「明治」(15)ピタ
バスタチンCa・OD錠4mg「明
治」(16)ピタバスタチンCa錠
1mg「明治」(17)ピタバスタチン
Ca錠2mg「明治」(18)ピタバス
タチンCa錠4mg「明治」(19)プ
ラミペキソール塩酸塩錠
0.125mg「明治」(20)プラミペキ
ソール塩酸塩錠0.5mg「明治」
(21)レボフロキサシン錠
250mg「明治」(22)レボフロキ
サシン錠500mg「明治」
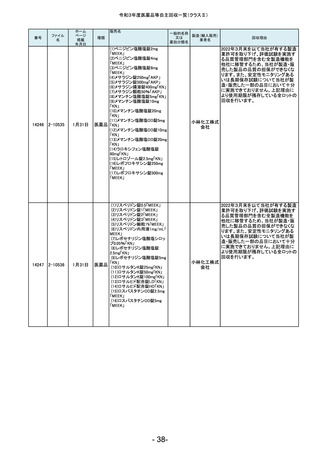
(1)シロドシン錠2mg「あす
か」(2)シロドシン錠4mg「あ
すか」(3)シロドシンOD錠2m
g「あすか」(4)シロドシンOD
錠4mg「あすか」(5)ビカルタミ
ド錠80mg「あすか」(6)ビカル
タミドOD錠80mg「あすか」
(7)メサラジン腸溶錠400mg
医薬品
「あすか」(8)ナフトピジル錠2
5mg「あすか」(9)ナフトピジ
ル錠50mg「あすか」(10)ナフ
トピジル錠75mg「あすか」
(11)ナフトピジルOD錠25mg
「あすか」(12)ナフトピジルOD
錠50mg「あすか」(13)ナフト
ピジルOD錠75mg「あすか」
(1)メマンチン塩酸塩錠5mg
「KMP」
(2)メマンチン塩酸塩錠10mg
「KMP」
(3)メマンチン塩酸塩錠20mg
「KMP」
医薬品
(4)メマンチン塩酸塩OD錠
5mg「KMP」
(5)メマンチン塩酸塩OD錠
10mg「KMP」
(6)メマンチン塩酸塩OD錠
20mg「KMP」
(1)レボセチリジン塩酸塩錠
2.5mg「CEO」
(2)レボセチリジン塩酸塩錠5
mg「CEO」
医薬品
- 31-
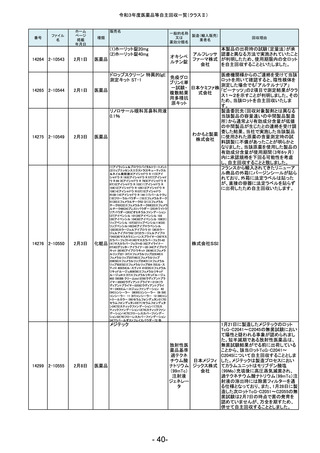
オロパタ
ジン塩酸
Meiji Seika
塩OD錠
ファルマ株式
2.5mg「明
会社
治」他 21
品目
回収理由
2022年3月末を以て1.に記載する製品
の製造委託先である小林化工株式会
社が製造業許可を取り下げ、評価試験
を実施する品質管理部門を含む全製造
機能を他社に移管するため、当該製造
委託先が製造した製品の品質の担保
ができなくなります。また、安定性モニタ
リングあるいは長期保存試験について
当該製造委託先が製造した一部の品
目において十分に実施できておりませ
ん。上記理由により使用期限が残存し
ている全ロットの回収を行います。
2022年3月末を以て上記1に記載する製
品の製造委託先である小林化工株式
会社が製造業許可を取り下げ、評価試
験を実施する品質管理部門を含む全製
造機能を他社に移管するため、小林化
工株式会社が製造・販売した製品の品
質の担保ができなくなります。また、安
あすか製薬株 定性モニタリングあるいは長期保存試
式会社
験について小林化工株式会社が製造し
た一部の品目において十分に実施でき
ておりません。上記理由により使用期
限が残存している全ロットの回収を行い
ます。
2022年3月末を以て製造委託先が有す
る製造業許可を取り下げ、評価試験を
実施する品質管理部門を含む全製造
機能を他社に移管するため、当社が製
造・販売した製品の品質の担保ができ
共創未来
なくなります。また、安定性モニタリング
メマンチン
ファーマ株式
塩酸塩
あるいは長期保存試験について十分に
会社
実施できておりません。上記理由により
使用期限が残存している全ロットを回
収することと致しました。
本製品の製造委託先である小林化工
株式会社が2022年3月末を以て製造業
許可を取り下げ、評価試験を実施する
品質管理部門を含む全製造機能を他
社に移管するため、当社が販売した製
レボセチリ
セオリアファー 品の品質の担保ができなくなります。ま
ジン塩酸
マ株式会社 た、安定性モニタリングあるいは長期保
塩錠
存試験について当社が販売した一部の
品目において十分に実施できておりま
せん。上記理由により使用期限が残存
している全ロットの回収を行います。
番号
ファイル
名
14228 2-10517
14229 2-10518
14230 2-10519
14231 2-10520
ホーム
ページ
掲載
年月日
1月31日
1月31日
1月31日
1月31日
販売名
一般的名称
製造(輸入販売)
又は
業者名
薬効分類名
種類
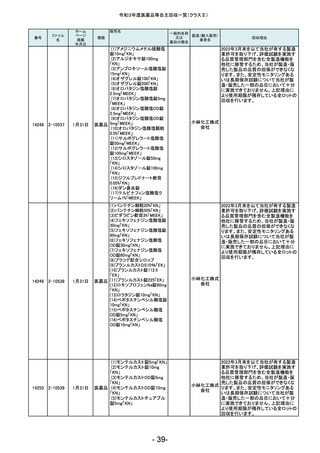
(1)オロパタジ塩酸塩OD錠
2.5mg「明治」
(2)オロパタジン塩酸塩OD錠
5mg「明治」(3)オロパタジン塩
酸塩錠2.5mg「明治」(4)オロパ
タジン塩酸塩錠5mg「明治」(5)
クエチアピン細粒50%「明治」
(6)クエチアピン錠100mg「明
治」(7)クエチアピン錠12.5mg
「明治」(8)クエチアピン錠
200mg「明治」(9)クエチアピン
錠25mg「明治」(10)クエチアピ
ン錠50mg「明治」(11)バラシク
ロビル錠500mg「明治」(12)バ
医薬品 ラシクロビル顆粒50%「明治」
(13)ピタバスタチンCa・OD錠
1mg「明治」(14)ピタバスタチン
Ca・OD錠2mg「明治」(15)ピタ
バスタチンCa・OD錠4mg「明
治」(16)ピタバスタチンCa錠
1mg「明治」(17)ピタバスタチン
Ca錠2mg「明治」(18)ピタバス
タチンCa錠4mg「明治」(19)プ
ラミペキソール塩酸塩錠
0.125mg「明治」(20)プラミペキ
ソール塩酸塩錠0.5mg「明治」
(21)レボフロキサシン錠
250mg「明治」(22)レボフロキ
サシン錠500mg「明治」
(1)シロドシン錠2mg「あす
か」(2)シロドシン錠4mg「あ
すか」(3)シロドシンOD錠2m
g「あすか」(4)シロドシンOD
錠4mg「あすか」(5)ビカルタミ
ド錠80mg「あすか」(6)ビカル
タミドOD錠80mg「あすか」
(7)メサラジン腸溶錠400mg
医薬品
「あすか」(8)ナフトピジル錠2
5mg「あすか」(9)ナフトピジ
ル錠50mg「あすか」(10)ナフ
トピジル錠75mg「あすか」
(11)ナフトピジルOD錠25mg
「あすか」(12)ナフトピジルOD
錠50mg「あすか」(13)ナフト
ピジルOD錠75mg「あすか」
(1)メマンチン塩酸塩錠5mg
「KMP」
(2)メマンチン塩酸塩錠10mg
「KMP」
(3)メマンチン塩酸塩錠20mg
「KMP」
医薬品
(4)メマンチン塩酸塩OD錠
5mg「KMP」
(5)メマンチン塩酸塩OD錠
10mg「KMP」
(6)メマンチン塩酸塩OD錠
20mg「KMP」
(1)レボセチリジン塩酸塩錠
2.5mg「CEO」
(2)レボセチリジン塩酸塩錠5
mg「CEO」
医薬品
- 31-
オロパタ
ジン塩酸
Meiji Seika
塩OD錠
ファルマ株式
2.5mg「明
会社
治」他 21
品目
回収理由
2022年3月末を以て1.に記載する製品
の製造委託先である小林化工株式会
社が製造業許可を取り下げ、評価試験
を実施する品質管理部門を含む全製造
機能を他社に移管するため、当該製造
委託先が製造した製品の品質の担保
ができなくなります。また、安定性モニタ
リングあるいは長期保存試験について
当該製造委託先が製造した一部の品
目において十分に実施できておりませ
ん。上記理由により使用期限が残存し
ている全ロットの回収を行います。
2022年3月末を以て上記1に記載する製
品の製造委託先である小林化工株式
会社が製造業許可を取り下げ、評価試
験を実施する品質管理部門を含む全製
造機能を他社に移管するため、小林化
工株式会社が製造・販売した製品の品
質の担保ができなくなります。また、安
あすか製薬株 定性モニタリングあるいは長期保存試
式会社
験について小林化工株式会社が製造し
た一部の品目において十分に実施でき
ておりません。上記理由により使用期
限が残存している全ロットの回収を行い
ます。
2022年3月末を以て製造委託先が有す
る製造業許可を取り下げ、評価試験を
実施する品質管理部門を含む全製造
機能を他社に移管するため、当社が製
造・販売した製品の品質の担保ができ
共創未来
なくなります。また、安定性モニタリング
メマンチン
ファーマ株式
塩酸塩
あるいは長期保存試験について十分に
会社
実施できておりません。上記理由により
使用期限が残存している全ロットを回
収することと致しました。
本製品の製造委託先である小林化工
株式会社が2022年3月末を以て製造業
許可を取り下げ、評価試験を実施する
品質管理部門を含む全製造機能を他
社に移管するため、当社が販売した製
レボセチリ
セオリアファー 品の品質の担保ができなくなります。ま
ジン塩酸
マ株式会社 た、安定性モニタリングあるいは長期保
塩錠
存試験について当社が販売した一部の
品目において十分に実施できておりま
せん。上記理由により使用期限が残存
している全ロットの回収を行います。