よむ、つかう、まなぶ。
資料3-1 アレムツズマブ(遺伝子組換え)[814KB] (23 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00043.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第65回 9/29)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
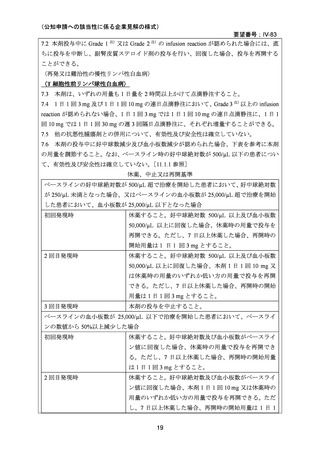
(公知申請への該当性に係る企業見解の様式)
要望番号;IV-83
7.2 本剤投与中に Grade 1 注)又は Grade 2 注)の infusion reaction が認められた場合には、直
ちに投与を中断し、副腎皮質ステロイド剤の投与を行い、回復した場合、投与を再開する
ことができる。
〈再発又は難治性の慢性リンパ性白血病〉
〈T 細胞性前リンパ球性白血病〉
7.3
本剤は、いずれの用量も 1 日量を 2 時間以上かけて点滴静注すること。
7.4
1 日 1 回 3 mg 及び 1 日 1 回 10 mg の連日点滴静注において、Grade 3 注)以上の infusion
reaction が認められない場合、1 日 1 回 3 mg では 1 日 1 回 10 mg の連日点滴静注に、1 日 1
回 10 mg では 1 日 1 回 30 mg の週 3 回隔日点滴静注に、それぞれ増量することができる。
7.5
他の抗悪性腫瘍剤との併用について、有効性及び安全性は確立していない。
7.6
本剤の投与中に好中球数減少及び血小板数減少が認められた場合、下表を参考に本剤
の用量を調節すること。なお、ベースライン時の好中球絶対数が 500/µL 以下の患者につい
て、有効性及び安全性は確立していない。
[11.1.1 参照]
休薬、中止又は再開基準
ベースラインの好中球絶対数が 500/µL 超で治療を開始した患者において、好中球絶対数
が 250/µL 未満となった場合、又はベースラインの血小板数が 25,000/µL 超で治療を開始
した患者において、血小板数が 25,000/µL 以下となった場合
初回発現時
休薬すること。好中球絶対数 500/µL 以上及び血小板数
50,000/µL 以上に回復した場合、休薬時の用量で投与を
再開できる。ただし、7 日以上休薬した場合、再開時の
開始用量は 1 日 1 回 3 mg とすること。
2 回目発現時
休薬すること。好中球絶対数 500/µL 以上及び血小板数
50,000/µL 以上に回復した場合、本剤 1 日 1 回 10 mg 又
は休薬時の用量のいずれか低い方の用量で投与を再開
できる。ただし、7 日以上休薬した場合、再開時の開始
用量は 1 日 1 回 3 mg とすること。
3 回目発現時
本剤の投与を中止すること。
ベースラインの血小板数が 25,000/µL 以下で治療を開始した患者において、ベースライ
ンの数値から 50%以上減少した場合
初回発現時
休薬すること。好中球絶対数及び血小板数がベースライ
ン値に回復した場合、休薬時の用量で投与を再開でき
る。ただし、7 日以上休薬した場合、再開時の開始用量
は 1 日 1 回 3 mg とすること。
2 回目発現時
休薬すること。好中球絶対数及び血小板数がベースライ
ン値に回復した場合、本剤 1 日 1 回 10 mg 又は休薬時の
用量のいずれか低い方の用量で投与を再開できる。ただ
し、7 日以上休薬した場合、再開時の開始用量は 1 日 1
19
要望番号;IV-83
7.2 本剤投与中に Grade 1 注)又は Grade 2 注)の infusion reaction が認められた場合には、直
ちに投与を中断し、副腎皮質ステロイド剤の投与を行い、回復した場合、投与を再開する
ことができる。
〈再発又は難治性の慢性リンパ性白血病〉
〈T 細胞性前リンパ球性白血病〉
7.3
本剤は、いずれの用量も 1 日量を 2 時間以上かけて点滴静注すること。
7.4
1 日 1 回 3 mg 及び 1 日 1 回 10 mg の連日点滴静注において、Grade 3 注)以上の infusion
reaction が認められない場合、1 日 1 回 3 mg では 1 日 1 回 10 mg の連日点滴静注に、1 日 1
回 10 mg では 1 日 1 回 30 mg の週 3 回隔日点滴静注に、それぞれ増量することができる。
7.5
他の抗悪性腫瘍剤との併用について、有効性及び安全性は確立していない。
7.6
本剤の投与中に好中球数減少及び血小板数減少が認められた場合、下表を参考に本剤
の用量を調節すること。なお、ベースライン時の好中球絶対数が 500/µL 以下の患者につい
て、有効性及び安全性は確立していない。
[11.1.1 参照]
休薬、中止又は再開基準
ベースラインの好中球絶対数が 500/µL 超で治療を開始した患者において、好中球絶対数
が 250/µL 未満となった場合、又はベースラインの血小板数が 25,000/µL 超で治療を開始
した患者において、血小板数が 25,000/µL 以下となった場合
初回発現時
休薬すること。好中球絶対数 500/µL 以上及び血小板数
50,000/µL 以上に回復した場合、休薬時の用量で投与を
再開できる。ただし、7 日以上休薬した場合、再開時の
開始用量は 1 日 1 回 3 mg とすること。
2 回目発現時
休薬すること。好中球絶対数 500/µL 以上及び血小板数
50,000/µL 以上に回復した場合、本剤 1 日 1 回 10 mg 又
は休薬時の用量のいずれか低い方の用量で投与を再開
できる。ただし、7 日以上休薬した場合、再開時の開始
用量は 1 日 1 回 3 mg とすること。
3 回目発現時
本剤の投与を中止すること。
ベースラインの血小板数が 25,000/µL 以下で治療を開始した患者において、ベースライ
ンの数値から 50%以上減少した場合
初回発現時
休薬すること。好中球絶対数及び血小板数がベースライ
ン値に回復した場合、休薬時の用量で投与を再開でき
る。ただし、7 日以上休薬した場合、再開時の開始用量
は 1 日 1 回 3 mg とすること。
2 回目発現時
休薬すること。好中球絶対数及び血小板数がベースライ
ン値に回復した場合、本剤 1 日 1 回 10 mg 又は休薬時の
用量のいずれか低い方の用量で投与を再開できる。ただ
し、7 日以上休薬した場合、再開時の開始用量は 1 日 1
19