よむ、つかう、まなぶ。
資料3-1 アレムツズマブ(遺伝子組換え)[814KB] (22 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00043.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第65回 9/29)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(公知申請への該当性に係る企業見解の様式)
要望番号;IV-83
【効能・効果】
(下線部追記)
○再発又は難治性の慢性リンパ性白血病
○同種造血幹細胞移植の前治療
○T 細胞性前リンパ球性白血病
(2)用法・用量について
T-PLL に対する用法及び用量は、本邦において「再発又は難治性の慢性リンパ性白血病」
に対して承認されている用法及び用量と同一とすることが適切と考える。T-PLL に対する
本剤の臨床試験の多くは国内で再発・難治性の慢性リンパ性白血病に対して承認されてい
る用法・用量で行われたものであり、先行して承認されている疾患に対する用法・用量と
同一であることは日本人での安全性が実臨床でも確かめられているため、妥当と考えられ
る。投与期間については、海外後方視研究 3)で 12 週までの投与が行われており、同様の投
与期間が T-PLL 国際研究グループ(TPLL-ISG)コンセンサスガイドライン 16)で推奨されて
いる。一方、12 週を超えての維持療法の有用性を示す知見はない。このため、国内で再発・
難治性の慢性リンパ性白血病に対して承認されている用法・用量と同様、投与開始から 12
週間までの投与とする投与期間は妥当と考える。
また、
「7.公知申請の妥当性について(2)要望内容に係る外国人におけるエビデンス及
び日本人における安全性の総合評価について」での安全性の総合評価及び T-PLL に対する
用法及び用量が、国内で再発又は難治性の慢性リンパ性白血病に対して承認されている用
法及び用量と同一とすることを踏まえると、T-PLL に対する用法及び用量に関連する注意
についても、本邦において「再発又は難治性の慢性リンパ性白血病」に対して承認されて
いる用法及び用量に関連する注意と同様の注意喚起が適切と考える。
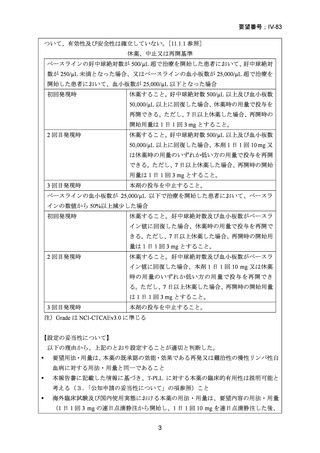
【用法及び用量】(下線部追記)(今回の要望に関連する部分のみ抜粋)
〈再発又は難治性の慢性リンパ性白血病〉
〈T 細胞性前リンパ球性白血病〉
通常、成人にはアレムツズマブ(遺伝子組換え)として 1 日 1 回 3 mg の連日点滴静注から
開始し、1 日 1 回 10 mg を連日点滴静注した後、1 日 1 回 30 mg を週 3 回隔日に点滴静注
する。ただし、投与開始から 12 週間までの投与とする。なお、患者の状態により適宜減量
する。
【用法及び用量に関連する注意】
(下線部追記)(今回の要望に関連する部分のみ抜粋)
〈効能共通〉
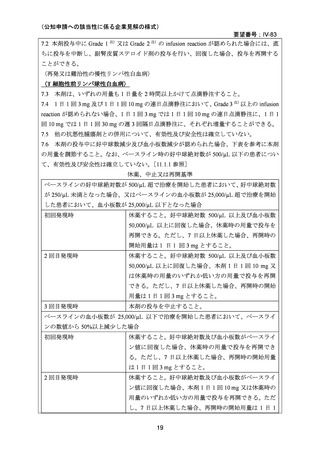
7.1 infusion reaction を軽減するため、本剤の投与前に抗ヒスタミン剤及び解熱鎮痛剤を投与
すること。さらに、本剤投与前に副腎皮質ステロイド剤を投与すると infusion reaction が軽
減されることがある。
[1.2、11.1.2 参照]
18
要望番号;IV-83
【効能・効果】
(下線部追記)
○再発又は難治性の慢性リンパ性白血病
○同種造血幹細胞移植の前治療
○T 細胞性前リンパ球性白血病
(2)用法・用量について
T-PLL に対する用法及び用量は、本邦において「再発又は難治性の慢性リンパ性白血病」
に対して承認されている用法及び用量と同一とすることが適切と考える。T-PLL に対する
本剤の臨床試験の多くは国内で再発・難治性の慢性リンパ性白血病に対して承認されてい
る用法・用量で行われたものであり、先行して承認されている疾患に対する用法・用量と
同一であることは日本人での安全性が実臨床でも確かめられているため、妥当と考えられ
る。投与期間については、海外後方視研究 3)で 12 週までの投与が行われており、同様の投
与期間が T-PLL 国際研究グループ(TPLL-ISG)コンセンサスガイドライン 16)で推奨されて
いる。一方、12 週を超えての維持療法の有用性を示す知見はない。このため、国内で再発・
難治性の慢性リンパ性白血病に対して承認されている用法・用量と同様、投与開始から 12
週間までの投与とする投与期間は妥当と考える。
また、
「7.公知申請の妥当性について(2)要望内容に係る外国人におけるエビデンス及
び日本人における安全性の総合評価について」での安全性の総合評価及び T-PLL に対する
用法及び用量が、国内で再発又は難治性の慢性リンパ性白血病に対して承認されている用
法及び用量と同一とすることを踏まえると、T-PLL に対する用法及び用量に関連する注意
についても、本邦において「再発又は難治性の慢性リンパ性白血病」に対して承認されて
いる用法及び用量に関連する注意と同様の注意喚起が適切と考える。
【用法及び用量】(下線部追記)(今回の要望に関連する部分のみ抜粋)
〈再発又は難治性の慢性リンパ性白血病〉
〈T 細胞性前リンパ球性白血病〉
通常、成人にはアレムツズマブ(遺伝子組換え)として 1 日 1 回 3 mg の連日点滴静注から
開始し、1 日 1 回 10 mg を連日点滴静注した後、1 日 1 回 30 mg を週 3 回隔日に点滴静注
する。ただし、投与開始から 12 週間までの投与とする。なお、患者の状態により適宜減量
する。
【用法及び用量に関連する注意】
(下線部追記)(今回の要望に関連する部分のみ抜粋)
〈効能共通〉
7.1 infusion reaction を軽減するため、本剤の投与前に抗ヒスタミン剤及び解熱鎮痛剤を投与
すること。さらに、本剤投与前に副腎皮質ステロイド剤を投与すると infusion reaction が軽
減されることがある。
[1.2、11.1.2 参照]
18