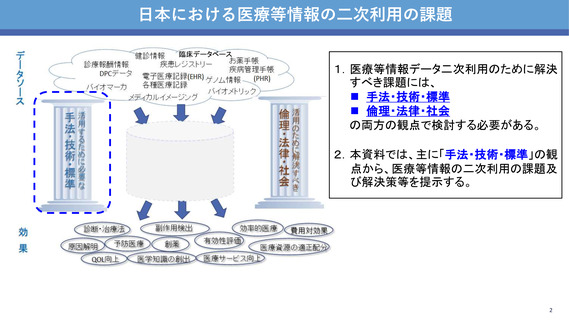
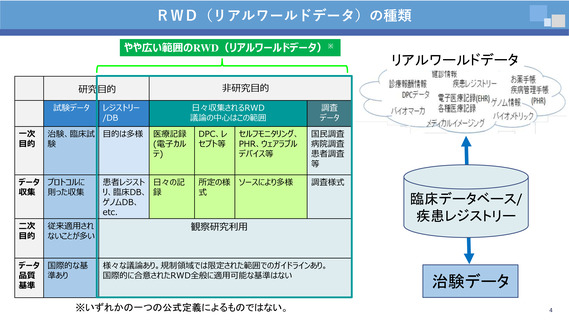
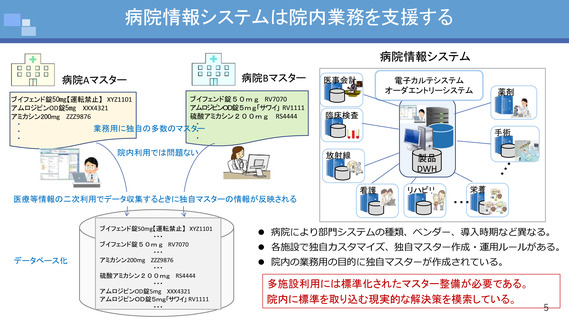
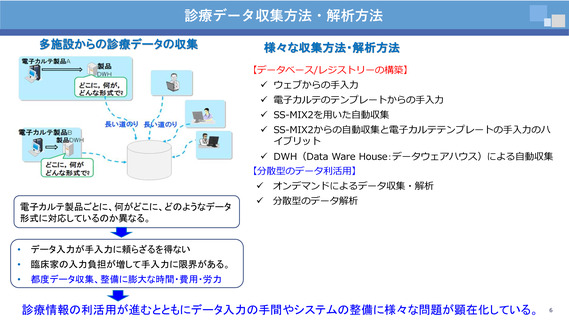
【参考資料6】技術作業班における構成員提出資料 (52 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_38564.html |
| 出典情報 | 健康・医療・介護情報利活用検討会 医療等情報の二次利用に関するワーキンググループ(第4回 3/18)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
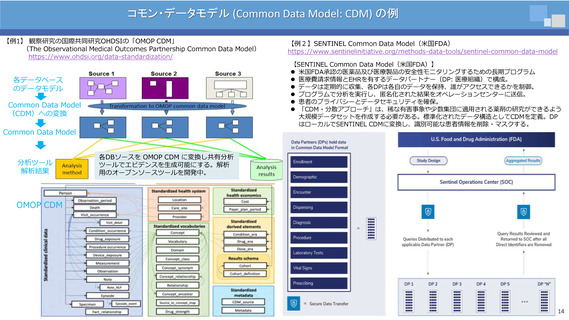
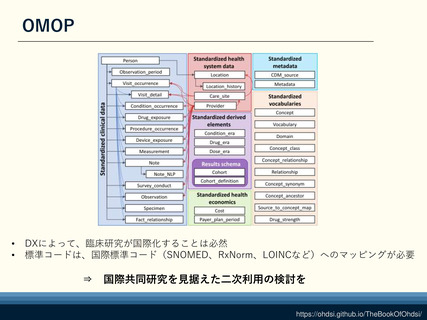
【例1】 観察研究の国際共同研究OHDSIの「OMOP CDM」
(The Observational Medical Outcomes Partnership Common Data Model)
https://www.ohdsi.org/data-standardization/
【SENTINEL Common Data Model(米国FDA)】
⚫ 米国FDA承認の医薬品及び医療製品の安全性モニタリングするための長期プログラム
⚫ 医療費請求情報とEHRを有するデータパートナー(DP: 医療組織)で構成。
⚫ データは定期的に収集、各DPは各自のデータを保持、誰がアクセスできるかを制御。
⚫ プログラムで分析を実行し、匿名化された結果をオペレーションセンターに送信。
⚫ 患者のプライバシーとデータセキュリティを確保。
⚫ 「CDM・分散アプローチ」は、稀な有害事象や少数集団に適用される薬剤の研究ができるよう
大規模データセットを作成する必要がある。標準化されたデータ構造としてCDMを定義。DP
はローカルでSENTINEL CDMに変換し、識別可能な患者情報を削除・マスクする。
各データベース
のデータモデル
Common Data Model
(CDM)への変換
Common Data Model
分析ツール
解析結果
【例2】SENTINEL Common Data Model(米国FDA)
https://www.sentinelinitiative.org/methods-data-tools/sentinel-common-data-model
各DBソースを OMOP CDM に変換し共有分析
ツールでエビデンスを生成可能にする。解析
用のオープンソースツールを開発中。
OMOP CDM
14 14