よむ、つかう、まなぶ。
03【資料1】新型コロナワクチンの接種について (41 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26922.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会(第33回 7/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
2.本日の論点:【2】新型コロナワクチンと他のワクチンとの同時接種について
ファイザー社又はアストラゼネカ社ワクチンとインフルエンザワクチン
同時接種の安全性
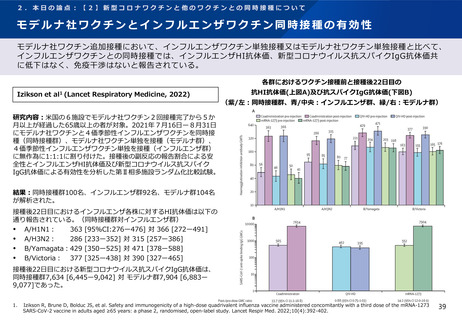
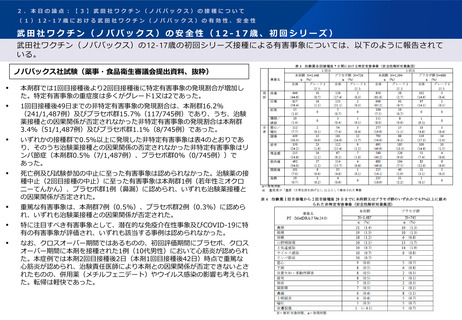
新型コロナワクチン2回目接種において、ファイザー社又はアストラゼネカ社ワクチン単独接種と比べ、インフルエ
ンザワクチンとの同時接種では安全性の懸念を認めなかったと報告されている。
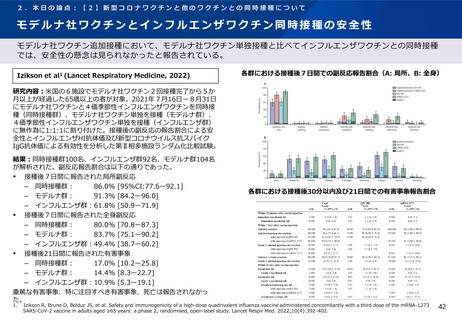
Lazarus et al1 (Lancet, 2021)
新型コロナワクチン2回目接種後7日間での非同時接種群と
研究内容:2021年4月1日ー6月26日に英国における12のNHS施設でファ
比較した同時接種群における1つ以上の全身副反応報告割合の差
イザー社又はアストラゼネカ社ワクチンを1回接種した成人が対象。2回目接
種を①新型コロナワクチンと季節性インフルエンザワクチンを同時接種し3週
間後にプラセボを接種(同時接種群)、②新型コロナワクチンとプラセボを接
種し3週間後に季節性インフルエンザワクチンを接種(非同時接種群)に無作
為に1:1に割り付け。新型コロナワクチンの2回目接種後の副反応の報告割合
による安全性と新型コロナウイルス抗スパイク(抗s)IgG抗体価とインフル
エンザウイルスHI抗体価による有効性を分析した第Ⅳ相多施設盲検ランダム
化比較試験。
結果:679名(同時接種群340名、非同時接種群339名)が新型コロナワクチ
ン2種類と季節性インフルエンザワクチン3種類※1の組合せにより6つのグ
ループに分類された。非同時接種群と比較して、同時接種群の新型コロナワク
全観察期間での非同時接種群と比較した
チン2回目接種後7日間での全身副反応報告割合の差は以下の通りであった。
同時接種群における1つ以上の全身副反応報告割合の差
4グループで非劣性(非劣性マージン25%)が示された。
‒ アストラゼネカ社/QIVc※1:-1.29% [95%CI: -14.69ー12.11]
‒ ファイザー社/QIVc:
6.17% [-6.27ー18.61]
※1
‒ ファイザー社/aTIV :
-12.9% [-34.15ー8.37]
※1
‒ アストラゼネカ社/QIVr : 2.53% [-13.25ー18.31]
2グループで95%CIの上限値が非劣性マージンを超えた。
‒ アストラゼネカ社/aTIV: 10.3% [-5.44ー26.03]
‒ ファイザー社/QIVr:
6.75% [-11.75ー25.25]
観察期間を通じた全身副反応報告割合は非同時接種群と比較して、同時接種群
でも同程度であった。全体で7例の重篤な有害事象が報告され、うち1例(ア
ストラゼネカ社ワクチンとインフルエンザワクチンを同時接種し、片頭痛を発
症)がワクチンと関連があると考えられた。
※1 aTIV、QIVc、QIVrはいずれもインフルエンザ不活化ワクチンで、aTIVは3価のMF59Cアジュバントワクチン、QIVc・QIVrは細胞性またはリコンビナント4価ワクチンを指す。
1.Lazarus R, Baos S, Cappel-Porter H, et al. Safety and immunogenicity of concomitant administration of COVID-19 vaccines (ChAdOx1 or BNT162b2) with seasonal influenza vaccines in adults in the
UK (ComFluCOV): a multicentre, randomised, controlled, phase 4 trial. Lancet. 2021;398(10318):2277-2287.
41
ファイザー社又はアストラゼネカ社ワクチンとインフルエンザワクチン
同時接種の安全性
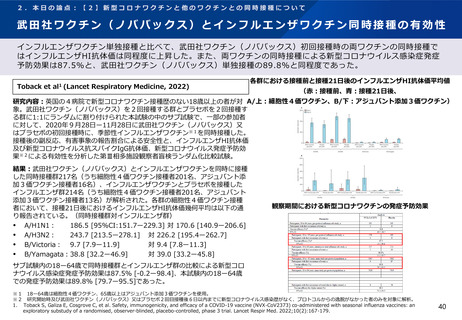
新型コロナワクチン2回目接種において、ファイザー社又はアストラゼネカ社ワクチン単独接種と比べ、インフルエ
ンザワクチンとの同時接種では安全性の懸念を認めなかったと報告されている。
Lazarus et al1 (Lancet, 2021)
新型コロナワクチン2回目接種後7日間での非同時接種群と
研究内容:2021年4月1日ー6月26日に英国における12のNHS施設でファ
比較した同時接種群における1つ以上の全身副反応報告割合の差
イザー社又はアストラゼネカ社ワクチンを1回接種した成人が対象。2回目接
種を①新型コロナワクチンと季節性インフルエンザワクチンを同時接種し3週
間後にプラセボを接種(同時接種群)、②新型コロナワクチンとプラセボを接
種し3週間後に季節性インフルエンザワクチンを接種(非同時接種群)に無作
為に1:1に割り付け。新型コロナワクチンの2回目接種後の副反応の報告割合
による安全性と新型コロナウイルス抗スパイク(抗s)IgG抗体価とインフル
エンザウイルスHI抗体価による有効性を分析した第Ⅳ相多施設盲検ランダム
化比較試験。
結果:679名(同時接種群340名、非同時接種群339名)が新型コロナワクチ
ン2種類と季節性インフルエンザワクチン3種類※1の組合せにより6つのグ
ループに分類された。非同時接種群と比較して、同時接種群の新型コロナワク
全観察期間での非同時接種群と比較した
チン2回目接種後7日間での全身副反応報告割合の差は以下の通りであった。
同時接種群における1つ以上の全身副反応報告割合の差
4グループで非劣性(非劣性マージン25%)が示された。
‒ アストラゼネカ社/QIVc※1:-1.29% [95%CI: -14.69ー12.11]
‒ ファイザー社/QIVc:
6.17% [-6.27ー18.61]
※1
‒ ファイザー社/aTIV :
-12.9% [-34.15ー8.37]
※1
‒ アストラゼネカ社/QIVr : 2.53% [-13.25ー18.31]
2グループで95%CIの上限値が非劣性マージンを超えた。
‒ アストラゼネカ社/aTIV: 10.3% [-5.44ー26.03]
‒ ファイザー社/QIVr:
6.75% [-11.75ー25.25]
観察期間を通じた全身副反応報告割合は非同時接種群と比較して、同時接種群
でも同程度であった。全体で7例の重篤な有害事象が報告され、うち1例(ア
ストラゼネカ社ワクチンとインフルエンザワクチンを同時接種し、片頭痛を発
症)がワクチンと関連があると考えられた。
※1 aTIV、QIVc、QIVrはいずれもインフルエンザ不活化ワクチンで、aTIVは3価のMF59Cアジュバントワクチン、QIVc・QIVrは細胞性またはリコンビナント4価ワクチンを指す。
1.Lazarus R, Baos S, Cappel-Porter H, et al. Safety and immunogenicity of concomitant administration of COVID-19 vaccines (ChAdOx1 or BNT162b2) with seasonal influenza vaccines in adults in the
UK (ComFluCOV): a multicentre, randomised, controlled, phase 4 trial. Lancet. 2021;398(10318):2277-2287.
41