よむ、つかう、まなぶ。
【資料1】生物学的製剤基準の一部改正について (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_24649.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会(令和3年度第4回 3/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
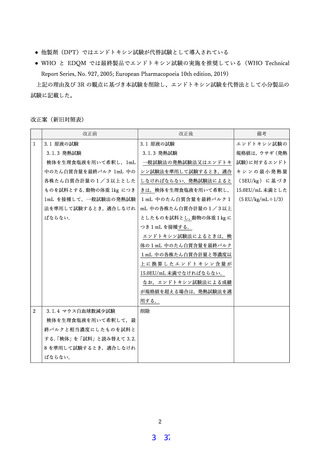
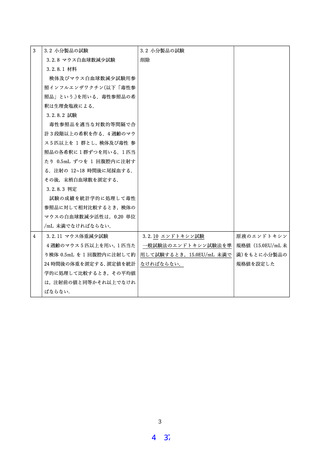
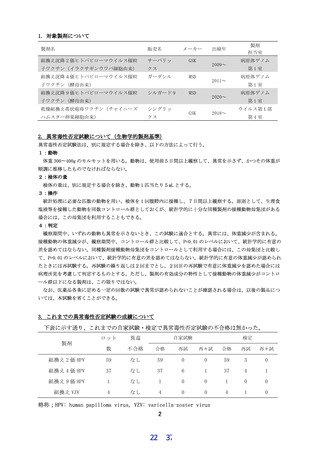
は2回までとし、2回目の再試験で有意に体重減少を認めた場合には病理所見を考慮して判定する
ものとする。ただし、製剤の有効成分の特性として接種動物の体重減少がコントロール群以下にな
る製剤は、この限りではない。
なお、医薬品各条に定める一定の回数の試験で異常が認められないことが確認される場合は、以
後の製品については、本試験を省くことができる。
2.
自家試験成績の検証
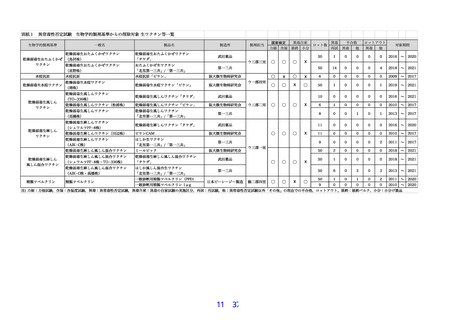
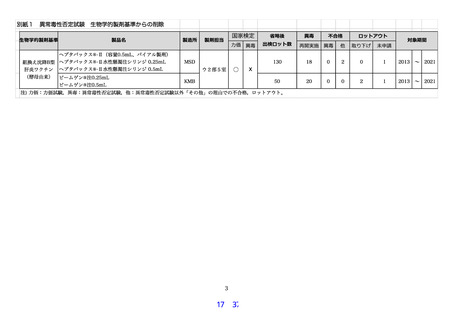
各製剤 6〜50 ロットの異常毒性否定試験の自家試験結果について検証した。承認時期、製造数に
より製剤ごとに検証ロット数は異なるが、以下の点について確認された。
①検証した全ての製剤において異常毒性否定試験の結果により「不合格」となり,出検されなかっ
たロットおよびロットアウトした製剤はなかった。
②8 品目については再試が行われていたが、再試の結果は全て「適合」であった。
③病理学的解析の結果,異常所見の検出例は報告なかった。
13 / 37
ものとする。ただし、製剤の有効成分の特性として接種動物の体重減少がコントロール群以下にな
る製剤は、この限りではない。
なお、医薬品各条に定める一定の回数の試験で異常が認められないことが確認される場合は、以
後の製品については、本試験を省くことができる。
2.
自家試験成績の検証
各製剤 6〜50 ロットの異常毒性否定試験の自家試験結果について検証した。承認時期、製造数に
より製剤ごとに検証ロット数は異なるが、以下の点について確認された。
①検証した全ての製剤において異常毒性否定試験の結果により「不合格」となり,出検されなかっ
たロットおよびロットアウトした製剤はなかった。
②8 品目については再試が行われていたが、再試の結果は全て「適合」であった。
③病理学的解析の結果,異常所見の検出例は報告なかった。
13 / 37