よむ、つかう、まなぶ。
資料3-2 医薬品添付文書改訂相談資料 (25 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_28092.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和4年度第13回 9/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(3)、(4)(略)
2.重要な基本的注意
(1)~(4)(略)
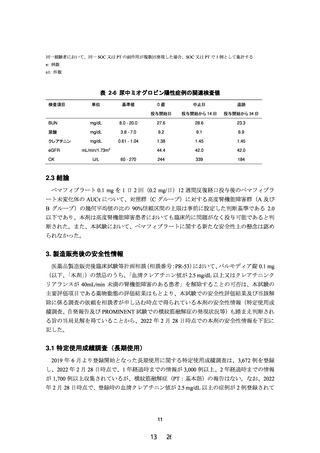
(5)腎機能障害を有する患者において急激な腎機能の悪化を伴
う横紋筋融解症(「副作用(1)重大な副作用」の項参照)
があらわれることがあるので、投与にあたっては患者の腎
機能を検査し、 血清クレアチニン値が 2.5 mg/dL 以上の場
合には投与を中止し、1.5 mg/dL 以上 2.5 mg/dL 未満 の場合
は減量又は投与間隔の延長等を行うこと。
(6)、(7)(略)
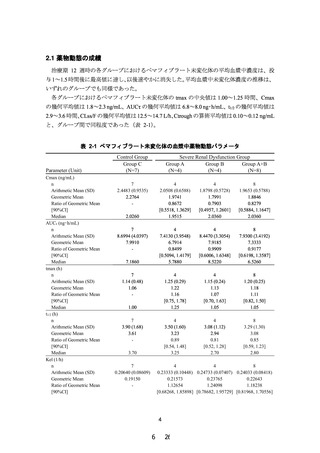
薬物動態
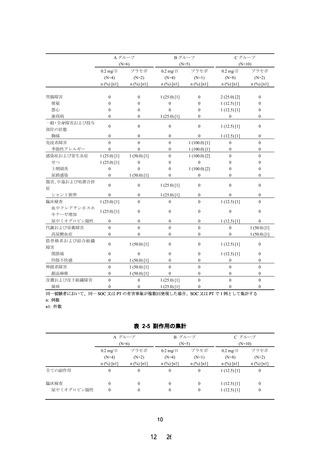
8.腎機能障害者での薬物動態
腎機能障害者(軽度、中等度、高度又は末期腎不全)に、本剤
0.2 mgを 単 回 経 口 投 与 し た と き の 腎 機 能 正 常 者 に 対 す る 薬 物
動態パラメータの比は次表のとおりであり、腎機能正常者群と
比較して、腎機能障害者群では曝露の増加が認められたが、腎
機能障害の程度に依存した曝露の増加は認められなかった。
(略)
(3)、(4)(略)
2.重要な基本的注意
(1)~(4)(略)
(5)腎機能障害を有する患者において急激な腎機能の悪化を伴
う横紋筋融解症(「副作用(1)重大な副作用」の項参照)
があらわれることがあるので、投与にあたっては患者の腎
機能を検査し、eGFR が 30 mL/min/1.73 m 2 未満 の場合は減
量又は投与間隔の延長等を行うこと。
(新設)
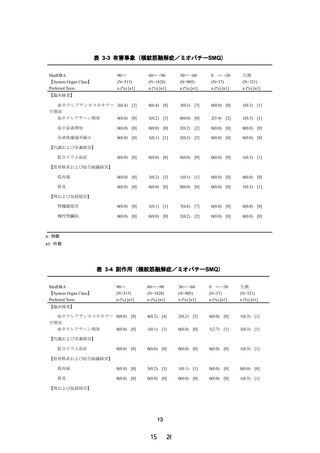
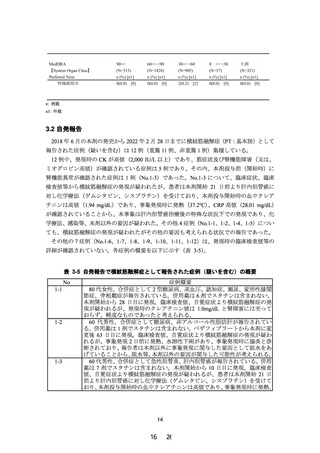
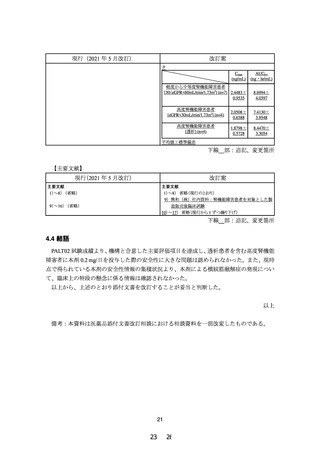
(2)腎機能障害(高度腎機能障害(eGFR<30 mL/min/1.73m 2 又
は 透 析 ) 及 び 軽 度 ~ 中 等 度 腎 機 能 障 害
(30≤eGFR<60 mL/min/1.73 m 2 ))を有するトリグリ
セライド(TG)高値の脂質異常症患者に、本剤 0.2 mg/
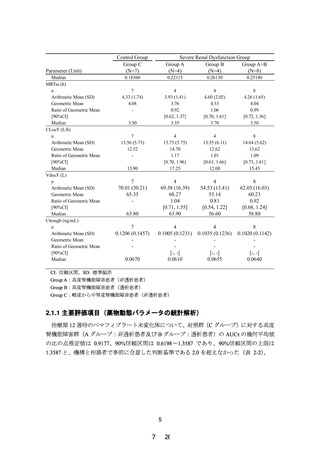
日を 1 日 2 回に分けて朝夕 12 週間投与した。12 週
時における AUC 0-τ について、軽度~中等度腎機能
障害群(対照群)に対する高度腎機能障害群の幾何平
均値の比及びその 90%信頼区間は次表のとおりであ
り、高度腎機能障害者 においても曝露の増加 は認め
られなかった。
(6)、(7)(略)
薬物動態
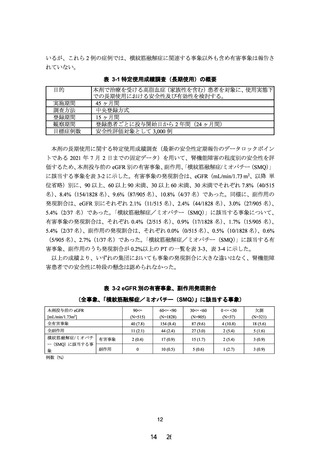
8.腎機能障害者での薬物動態
(1) 腎機能障害者(軽度、中等度、高度又は末期腎不全)に、
本 剤0.2 mgを 単 回 経 口 投 与 し た と き の 腎 機 能 正 常 者
に対する薬物動態パラメータの比は次表のとおりで
あり、腎機能正常者群と比較して、腎機能障害者群で
は曝露の増加が認められたが、腎機能障害の程度に
依存した曝露の増加は認められなかった。
(略)
2
RPI117_興和株式会社_添付文書改訂相談記録
25 / 26
2.重要な基本的注意
(1)~(4)(略)
(5)腎機能障害を有する患者において急激な腎機能の悪化を伴
う横紋筋融解症(「副作用(1)重大な副作用」の項参照)
があらわれることがあるので、投与にあたっては患者の腎
機能を検査し、 血清クレアチニン値が 2.5 mg/dL 以上の場
合には投与を中止し、1.5 mg/dL 以上 2.5 mg/dL 未満 の場合
は減量又は投与間隔の延長等を行うこと。
(6)、(7)(略)
薬物動態
8.腎機能障害者での薬物動態
腎機能障害者(軽度、中等度、高度又は末期腎不全)に、本剤
0.2 mgを 単 回 経 口 投 与 し た と き の 腎 機 能 正 常 者 に 対 す る 薬 物
動態パラメータの比は次表のとおりであり、腎機能正常者群と
比較して、腎機能障害者群では曝露の増加が認められたが、腎
機能障害の程度に依存した曝露の増加は認められなかった。
(略)
(3)、(4)(略)
2.重要な基本的注意
(1)~(4)(略)
(5)腎機能障害を有する患者において急激な腎機能の悪化を伴
う横紋筋融解症(「副作用(1)重大な副作用」の項参照)
があらわれることがあるので、投与にあたっては患者の腎
機能を検査し、eGFR が 30 mL/min/1.73 m 2 未満 の場合は減
量又は投与間隔の延長等を行うこと。
(新設)
(2)腎機能障害(高度腎機能障害(eGFR<30 mL/min/1.73m 2 又
は 透 析 ) 及 び 軽 度 ~ 中 等 度 腎 機 能 障 害
(30≤eGFR<60 mL/min/1.73 m 2 ))を有するトリグリ
セライド(TG)高値の脂質異常症患者に、本剤 0.2 mg/
日を 1 日 2 回に分けて朝夕 12 週間投与した。12 週
時における AUC 0-τ について、軽度~中等度腎機能
障害群(対照群)に対する高度腎機能障害群の幾何平
均値の比及びその 90%信頼区間は次表のとおりであ
り、高度腎機能障害者 においても曝露の増加 は認め
られなかった。
(6)、(7)(略)
薬物動態
8.腎機能障害者での薬物動態
(1) 腎機能障害者(軽度、中等度、高度又は末期腎不全)に、
本 剤0.2 mgを 単 回 経 口 投 与 し た と き の 腎 機 能 正 常 者
に対する薬物動態パラメータの比は次表のとおりで
あり、腎機能正常者群と比較して、腎機能障害者群で
は曝露の増加が認められたが、腎機能障害の程度に
依存した曝露の増加は認められなかった。
(略)
2
RPI117_興和株式会社_添付文書改訂相談記録
25 / 26