よむ、つかう、まなぶ。
資料3-2 医薬品添付文書改訂相談資料 (21 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_28092.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和4年度第13回 9/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
能を検査し、血清クレアチニン値が 2.5mg/dL 以上の場合には投与を中止し、1.5mg/dL 以
上 2.5mg/dL 未満の場合は減量又は投与間隔の延長等を行うこと。
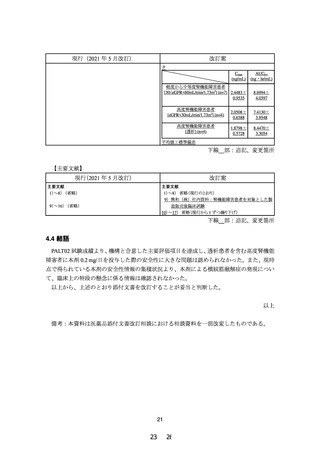
PALT02 試験の成績より、透析患者を含む高度腎機能障害患者での本剤投与時の安全性へ
の懸念は認められなかったが、現時点では使用経験が限られていることから、高度腎機能障
害者に対しては慎重投与の規定を設定し、最大用量を 1 日 0.2 mg とすることが適切と判断し
た。
なお、腎機能低下の目安の指標については、2019 年 9 月日本動脈硬化学会からの要望にお
いても「eGFR に変更すること」が要望されているが、日本腎臓学会が発行している「エビデ
ンスに基づく CKD 診療ガイドライン 2018」では eGFR が採用されている。PALT02 試験では
腎機能低下の指標として eGFR を用いて試験を実施したこと、クレアチニンクリアランスの
測定には蓄尿が必要であり、外来診療の中では現実的ではなく医療現場の実態としても
eGFR を用いることが適切と判断した。
4.3 添付文書改訂案について
PALT02 試験成績より得られた知見に基づき、以下に添付文書改訂案を提示する。
【使用上の注意】
現行(2021 年 5 月改訂)
改訂案
禁忌(次の患者には投与しないこと)
(1)~(2) 省略
(3)血清クレアチニン値が2.5mg/dL以上又はクレアチニン
クリアランスが40mL/min未満の腎機能障害のある患者
〔横紋筋融解症があらわれることがある。〕
(4)~(6) 省略
禁忌(次の患者には投与しないこと)
(1)~(2) 省略(現行のとおり)
(3)~(5) 省略(現行から1ずつ繰り上げ)
用法・用量
通常、成人にはペマフィブラートとして1回0.1mgを1日2回
朝夕に経口投与する。なお、年齢、症状に応じて適宜増減
するが、最大用量は1回0.2mgを1日2回までとする。
用法・用量
通常、成人にはペマフィブラートとして1回0.1mgを1日2回
朝夕に経口投与する。なお、年齢、症状に応じて適宜増減
するが、最大用量は1回0.2mgを1日2回までとする。
〔用法・用量に関連する使用上の注意〕
(1) 省略
(2)急激な腎機能の悪化を伴う横紋筋融解症
(「副作用(1)重大な副作用」の項参照)があらわれる
ことがあるので、投与にあたっては患者の腎機能を
検査し、血清クレアチニン値が2.5mg/dL以上の場合には
投与を中止し、1.5mg/dL以上2.5mg/dL未満の場合は
低用量から投与を開始するか、投与間隔を延長して
使用すること。
〔用法・用量に関連する使用上の注意〕
(1) 省略(現行のとおり)
(2)急激な腎機能の悪化を伴う横紋筋融解症
(「副作用(1)重大な副作用」の項参照)があらわれる
ことがあるので、投与にあたっては患者の腎機能を
検査し、eGFRが30mL/min/1.73m2未満の場合は
低用量から投与を開始するか、投与間隔を延長して
使用すること。ただし、最大用量は1日0.2mgまでとする。
19
21 / 26
上 2.5mg/dL 未満の場合は減量又は投与間隔の延長等を行うこと。
PALT02 試験の成績より、透析患者を含む高度腎機能障害患者での本剤投与時の安全性へ
の懸念は認められなかったが、現時点では使用経験が限られていることから、高度腎機能障
害者に対しては慎重投与の規定を設定し、最大用量を 1 日 0.2 mg とすることが適切と判断し
た。
なお、腎機能低下の目安の指標については、2019 年 9 月日本動脈硬化学会からの要望にお
いても「eGFR に変更すること」が要望されているが、日本腎臓学会が発行している「エビデ
ンスに基づく CKD 診療ガイドライン 2018」では eGFR が採用されている。PALT02 試験では
腎機能低下の指標として eGFR を用いて試験を実施したこと、クレアチニンクリアランスの
測定には蓄尿が必要であり、外来診療の中では現実的ではなく医療現場の実態としても
eGFR を用いることが適切と判断した。
4.3 添付文書改訂案について
PALT02 試験成績より得られた知見に基づき、以下に添付文書改訂案を提示する。
【使用上の注意】
現行(2021 年 5 月改訂)
改訂案
禁忌(次の患者には投与しないこと)
(1)~(2) 省略
(3)血清クレアチニン値が2.5mg/dL以上又はクレアチニン
クリアランスが40mL/min未満の腎機能障害のある患者
〔横紋筋融解症があらわれることがある。〕
(4)~(6) 省略
禁忌(次の患者には投与しないこと)
(1)~(2) 省略(現行のとおり)
(3)~(5) 省略(現行から1ずつ繰り上げ)
用法・用量
通常、成人にはペマフィブラートとして1回0.1mgを1日2回
朝夕に経口投与する。なお、年齢、症状に応じて適宜増減
するが、最大用量は1回0.2mgを1日2回までとする。
用法・用量
通常、成人にはペマフィブラートとして1回0.1mgを1日2回
朝夕に経口投与する。なお、年齢、症状に応じて適宜増減
するが、最大用量は1回0.2mgを1日2回までとする。
〔用法・用量に関連する使用上の注意〕
(1) 省略
(2)急激な腎機能の悪化を伴う横紋筋融解症
(「副作用(1)重大な副作用」の項参照)があらわれる
ことがあるので、投与にあたっては患者の腎機能を
検査し、血清クレアチニン値が2.5mg/dL以上の場合には
投与を中止し、1.5mg/dL以上2.5mg/dL未満の場合は
低用量から投与を開始するか、投与間隔を延長して
使用すること。
〔用法・用量に関連する使用上の注意〕
(1) 省略(現行のとおり)
(2)急激な腎機能の悪化を伴う横紋筋融解症
(「副作用(1)重大な副作用」の項参照)があらわれる
ことがあるので、投与にあたっては患者の腎機能を
検査し、eGFRが30mL/min/1.73m2未満の場合は
低用量から投与を開始するか、投与間隔を延長して
使用すること。ただし、最大用量は1日0.2mgまでとする。
19
21 / 26