よむ、つかう、まなぶ。
資料1-3 ビソプロロール 調査結果報告書及び添付文書[2.5MB] (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_38855.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和5年度第15回 3/26)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
なお、機構は、本調査において専門協議を実施しており、本専門協議の専門委員は、調査
対象品目についての専門委員からの申し出等に基づき、
「医薬品医療機器総合機構における
専門協議等の実施に関する達」
(平成 20 年 12 月 25 日付 20 達第 8 号)の規程により、指名
した。
III. WG における検討
本薬の添付文書における「妊婦又は妊娠している可能性のある女性」への注意事項の適切
性について、表 1 に示す項目を含む WG 報告書(別添 2)が取りまとめられた。
表 1.
WG 報告書の項目
1.品目の概要
5.臨床使用に関する報告
2.背景
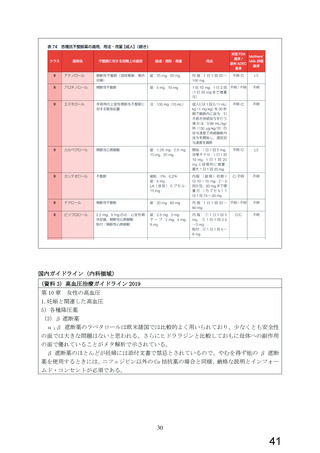
6.国内外のガイドライン
3.海外添付文書における記載状況
7.禁忌解除の妥当性
4.動物試験
8.添付文書の改訂案
IV. 機構における調査
機構は、WG 報告書を踏まえ、以下の点について検討を行った。
1. 非臨床試験に基づく情報(WG 報告書「4. 動物試験」参照)
1-1.公表文献
WG により、本薬の先発医薬品の承認時の生殖発生毒性試験が評価されている(WG 報告
書「4. 動物試験」参照)
。
WG での評価に追加して、本薬の製造販売承認後における本薬の生殖発生毒性に関する公
表文献について、本薬の先発医薬品の製造販売承認取得者(田辺三菱製薬株式会社 2、トー
アエイヨー株式会社 3)により検索が行われた。非臨床試験において生殖発生毒性のリスク
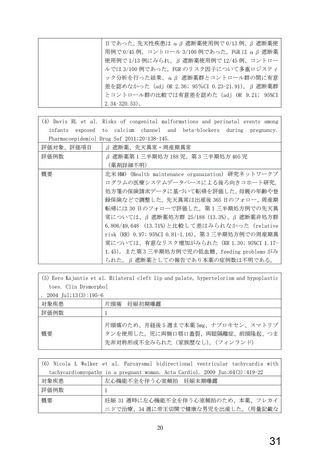
を示す報告が 1 報抽出され、その概要は以下のとおりであった。高血圧ラットにおける胎児
の死亡・発育抑制、出生児の発育毒性に関する報告であり、製造販売承認時に評価された生
殖発生毒性に関しての知見に加え、新たな毒性所見は認められなかった。
① Effect of nebivolol treatment during pregnancy on the intrauterine fetal growth, mortality
and pup postnatal development in the l-NAME-induced hypertensive rats ( Eur J
2 検索データベース(JMEDPlus, MEDLINE)
、検索条件(動物 or 人×ビソプロロール×妊娠・妊婦、胎児、子宮内、催奇形
性、生殖発生毒)、対象期間(JMEDPlus :1981 年 4 月~2023 年 8 月 15 日, MEDLINE: 1964 年~2023 年 8 月 21 日)。な
お、抽出結果にはヒトで先天異常を認めたとする報告 2 報が含まれるが、いずれも WG 報告に記載の報告であった。
3 検索データベース(MEDLINE, PhaDOMs)
、検索条件(MEDLINE:mesh.#(Bisoprolol)ORti,ab,subst(bisoprolol), PhaDOMs
(2013 年 6 月 28 日~2014 年 3 月 31 日)
:「bisoprolol およびその塩」を有効成分とする医薬品(単剤)の安全性情報(副
作用・感染症・安全性・相互作用・品質)および有効性欠如・無効の情報、PhaDOMs(2014 年 4 月 1 日~2023 年 9 月 4 日)
:
「bisoprolol およびその塩」を有効成分とする医薬品(単剤)の安全性情報(副作用・感染症・有害事象・自殺企図・毒性等・
相互作用・職業上の曝露・品質・その他)および有効性欠如・無効の情報)、対象期間(2013 年 6 月 28 日~2023 年 9 月
4 日)。
2
対象品目についての専門委員からの申し出等に基づき、
「医薬品医療機器総合機構における
専門協議等の実施に関する達」
(平成 20 年 12 月 25 日付 20 達第 8 号)の規程により、指名
した。
III. WG における検討
本薬の添付文書における「妊婦又は妊娠している可能性のある女性」への注意事項の適切
性について、表 1 に示す項目を含む WG 報告書(別添 2)が取りまとめられた。
表 1.
WG 報告書の項目
1.品目の概要
5.臨床使用に関する報告
2.背景
6.国内外のガイドライン
3.海外添付文書における記載状況
7.禁忌解除の妥当性
4.動物試験
8.添付文書の改訂案
IV. 機構における調査
機構は、WG 報告書を踏まえ、以下の点について検討を行った。
1. 非臨床試験に基づく情報(WG 報告書「4. 動物試験」参照)
1-1.公表文献
WG により、本薬の先発医薬品の承認時の生殖発生毒性試験が評価されている(WG 報告
書「4. 動物試験」参照)
。
WG での評価に追加して、本薬の製造販売承認後における本薬の生殖発生毒性に関する公
表文献について、本薬の先発医薬品の製造販売承認取得者(田辺三菱製薬株式会社 2、トー
アエイヨー株式会社 3)により検索が行われた。非臨床試験において生殖発生毒性のリスク
を示す報告が 1 報抽出され、その概要は以下のとおりであった。高血圧ラットにおける胎児
の死亡・発育抑制、出生児の発育毒性に関する報告であり、製造販売承認時に評価された生
殖発生毒性に関しての知見に加え、新たな毒性所見は認められなかった。
① Effect of nebivolol treatment during pregnancy on the intrauterine fetal growth, mortality
and pup postnatal development in the l-NAME-induced hypertensive rats ( Eur J
2 検索データベース(JMEDPlus, MEDLINE)
、検索条件(動物 or 人×ビソプロロール×妊娠・妊婦、胎児、子宮内、催奇形
性、生殖発生毒)、対象期間(JMEDPlus :1981 年 4 月~2023 年 8 月 15 日, MEDLINE: 1964 年~2023 年 8 月 21 日)。な
お、抽出結果にはヒトで先天異常を認めたとする報告 2 報が含まれるが、いずれも WG 報告に記載の報告であった。
3 検索データベース(MEDLINE, PhaDOMs)
、検索条件(MEDLINE:mesh.#(Bisoprolol)ORti,ab,subst(bisoprolol), PhaDOMs
(2013 年 6 月 28 日~2014 年 3 月 31 日)
:「bisoprolol およびその塩」を有効成分とする医薬品(単剤)の安全性情報(副
作用・感染症・安全性・相互作用・品質)および有効性欠如・無効の情報、PhaDOMs(2014 年 4 月 1 日~2023 年 9 月 4 日)
:
「bisoprolol およびその塩」を有効成分とする医薬品(単剤)の安全性情報(副作用・感染症・有害事象・自殺企図・毒性等・
相互作用・職業上の曝露・品質・その他)および有効性欠如・無効の情報)、対象期間(2013 年 6 月 28 日~2023 年 9 月
4 日)。
2