よむ、つかう、まなぶ。
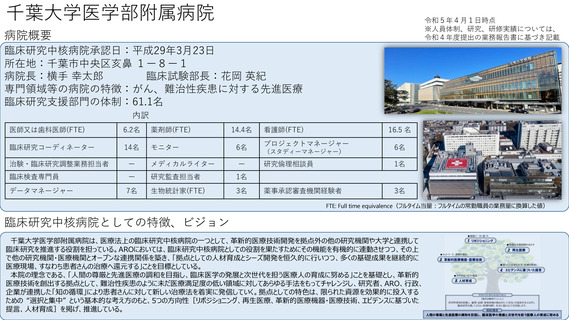
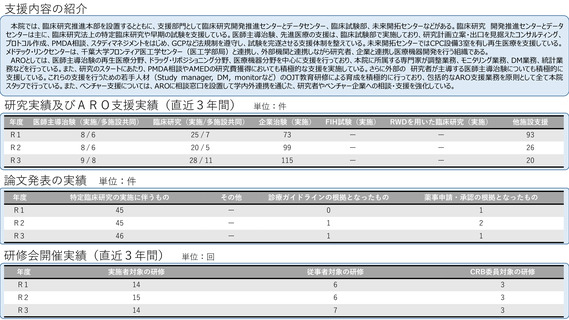
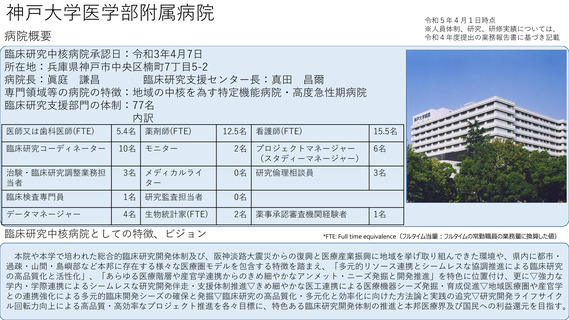
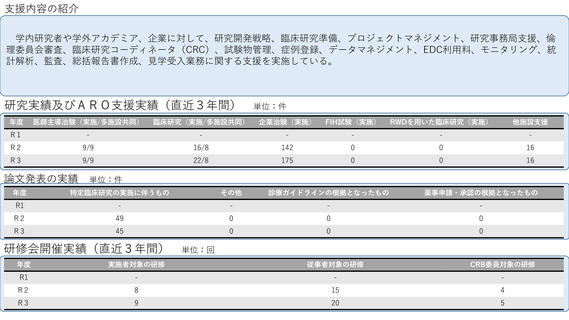
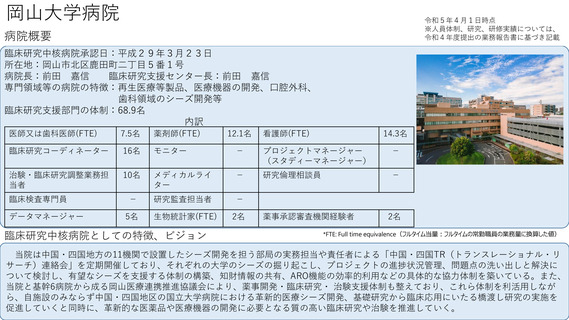
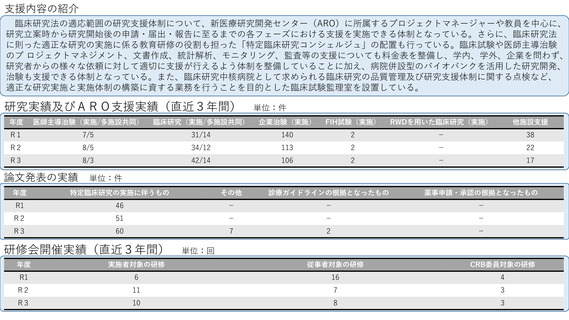
参考資料1:臨床研究中核病院概要表 (56 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_34378.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第33回 8/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
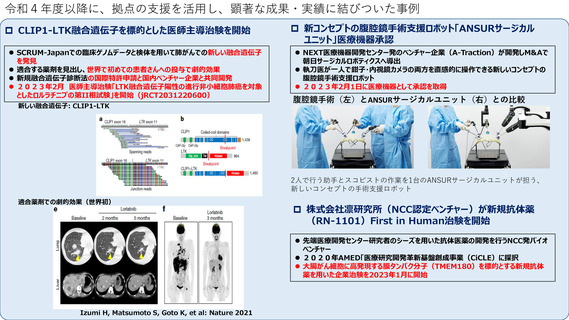
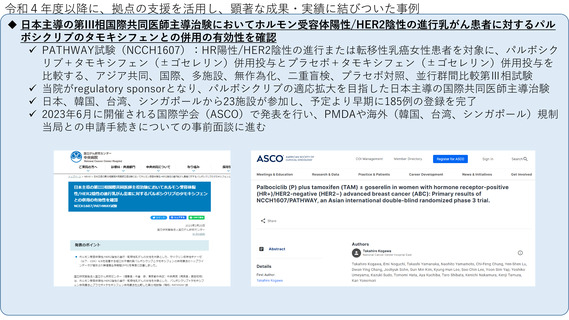
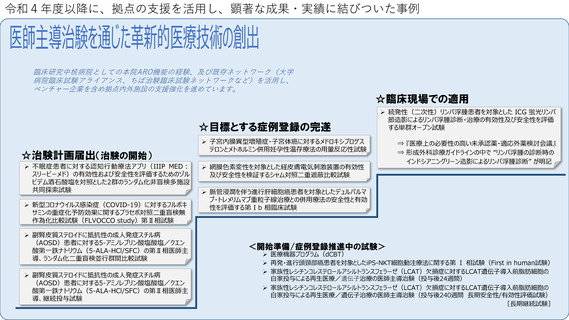
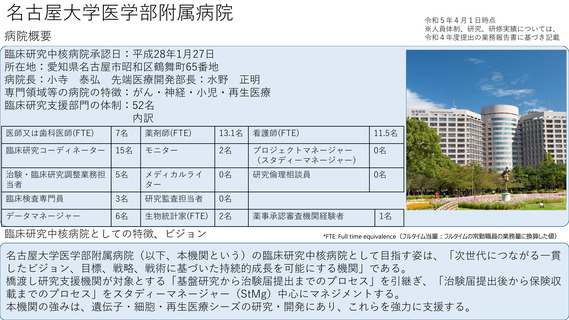
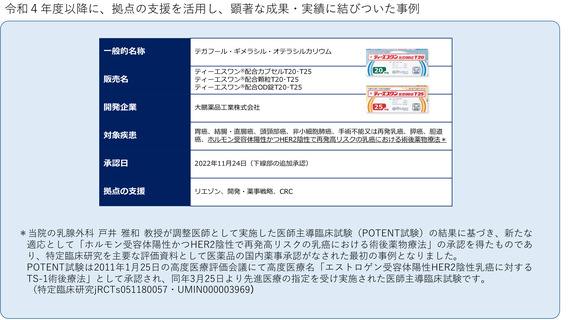
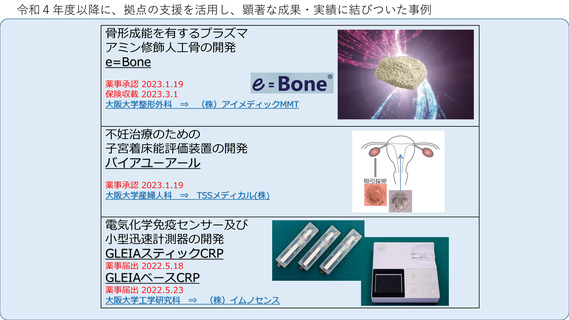
令和4年度以降に、拠点の支援を活用し、顕著な成果・実績に結びついた事例
シーズ名:「ハイリスク症候性人工弁周囲逆流に対する経カテーテル逆流閉鎖術の安全性及び有効性を検討する医師
主導治験」 代表 九州大学病院 有田 武史(日本医師会→AMED 臨床研究・治験推進研究事業 H28-31年)
高度管理医療機器 人工心膜用補綴材 「弁周囲逆流閉鎖セット」 承認番号:30500BZX00101000 R5年5月11日
僧帽弁位及び大動脈弁位の人工弁置換術後の人工弁周囲逆流(PVL, paravalvular leak)のために生じる遷延性溶血性貧血並びに心不全の標準治療
は、再手術が推奨されてきた。しかしながら再手術は再開胸による合併症のリスクを伴い、手術後も再度 PVL を引き起こす可能性が高い。また、
高齢者あるいはその他の合併疾患により複数回の開心術を受けることができない患者も存在する。海外では、再手術による死亡率は6~42% 、周術
期の脳卒中発症率は5.1%、また再手術を受けた患者の25%には胸骨切開創感染による再建が必要であったことが報告されている。そのためPVLの
経皮的閉鎖術が 1992 年に初めて報告された。海外でのカテーテルデバイスの普及と手技の向上により構造的心疾患治療が広まり、ようやく本邦で
も PVL に対する経カテーテル的閉鎖術が少しずつ行われるようになってきたが、適応のない既承認デバイスが治療に使用されている状況である。
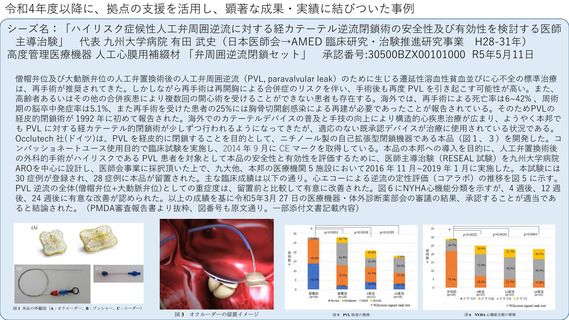
Occlutech 社(ドイツ)は、PVL を経皮的に閉鎖することを目的として、ニチノール製の自己拡張型閉鎖機器である本品(図1、3)を開発した。コ
ンパッショネートユース使用目的で臨床試験を実施し、2014 年 9 月に CE マークを取得している。本品の本邦への導入を目的に、人工弁置換術後
の外科的手術がハイリスクである PVL 患者を対象として本品の安全性と有効性を評価するために、医師主導治験(RESEAL 試験)を九州大学病院
AROを中心に設計し、医師会事業に採択頂いた上で、九大他、本邦の医療機関 5 施設において2016 年 11 月~2019 年 1 月に実施した。本試験には
30 症例が登録され、28 症例に本品が留置された。主な臨床成績は以下の通り。心エコーによる逆流の定性評価(コアラボ)の推移を図 5 に示す。
PVL 逆流の全体(僧帽弁位+大動脈弁位)としての重症度は、留置前と比較して有意に改善された。図6にNYHA心機能分類を示すが、4 週後、12 週
後、24 週後に有意な改善が認められた。以上の成績を基に令和5年3月 27 日の医療機器・体外診断薬部会の審議の結果、承認することが適当であ
ると結論された。(PMDA審査報告書より抜粋、図番号も原文通り。一部添付文書記載内容)
シーズ名:「ハイリスク症候性人工弁周囲逆流に対する経カテーテル逆流閉鎖術の安全性及び有効性を検討する医師
主導治験」 代表 九州大学病院 有田 武史(日本医師会→AMED 臨床研究・治験推進研究事業 H28-31年)
高度管理医療機器 人工心膜用補綴材 「弁周囲逆流閉鎖セット」 承認番号:30500BZX00101000 R5年5月11日
僧帽弁位及び大動脈弁位の人工弁置換術後の人工弁周囲逆流(PVL, paravalvular leak)のために生じる遷延性溶血性貧血並びに心不全の標準治療
は、再手術が推奨されてきた。しかしながら再手術は再開胸による合併症のリスクを伴い、手術後も再度 PVL を引き起こす可能性が高い。また、
高齢者あるいはその他の合併疾患により複数回の開心術を受けることができない患者も存在する。海外では、再手術による死亡率は6~42% 、周術
期の脳卒中発症率は5.1%、また再手術を受けた患者の25%には胸骨切開創感染による再建が必要であったことが報告されている。そのためPVLの
経皮的閉鎖術が 1992 年に初めて報告された。海外でのカテーテルデバイスの普及と手技の向上により構造的心疾患治療が広まり、ようやく本邦で
も PVL に対する経カテーテル的閉鎖術が少しずつ行われるようになってきたが、適応のない既承認デバイスが治療に使用されている状況である。
Occlutech 社(ドイツ)は、PVL を経皮的に閉鎖することを目的として、ニチノール製の自己拡張型閉鎖機器である本品(図1、3)を開発した。コ
ンパッショネートユース使用目的で臨床試験を実施し、2014 年 9 月に CE マークを取得している。本品の本邦への導入を目的に、人工弁置換術後
の外科的手術がハイリスクである PVL 患者を対象として本品の安全性と有効性を評価するために、医師主導治験(RESEAL 試験)を九州大学病院
AROを中心に設計し、医師会事業に採択頂いた上で、九大他、本邦の医療機関 5 施設において2016 年 11 月~2019 年 1 月に実施した。本試験には
30 症例が登録され、28 症例に本品が留置された。主な臨床成績は以下の通り。心エコーによる逆流の定性評価(コアラボ)の推移を図 5 に示す。
PVL 逆流の全体(僧帽弁位+大動脈弁位)としての重症度は、留置前と比較して有意に改善された。図6にNYHA心機能分類を示すが、4 週後、12 週
後、24 週後に有意な改善が認められた。以上の成績を基に令和5年3月 27 日の医療機器・体外診断薬部会の審議の結果、承認することが適当であ
ると結論された。(PMDA審査報告書より抜粋、図番号も原文通り。一部添付文書記載内容)
関連画像
ページ内で利用されている画像ファイルです。
有料会員登録をして頂くことで、このページ内で利用されている画像を個別に閲覧・ダウンロードすることができるようになります。