よむ、つかう、まなぶ。
参考資料1:臨床研究中核病院概要表 (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_34378.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第33回 8/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
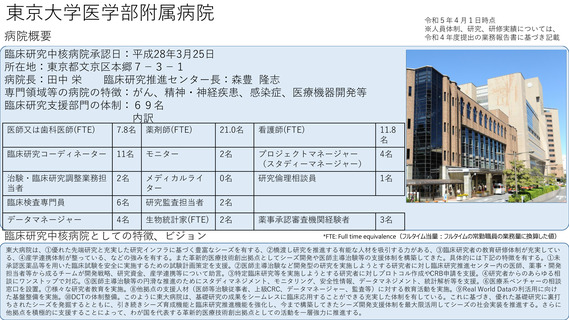
東京大学医学部附属病院
令和5年4月1日時点
※人員体制、研究、研修実績については、
令和4年度提出の業務報告書に基づき記載
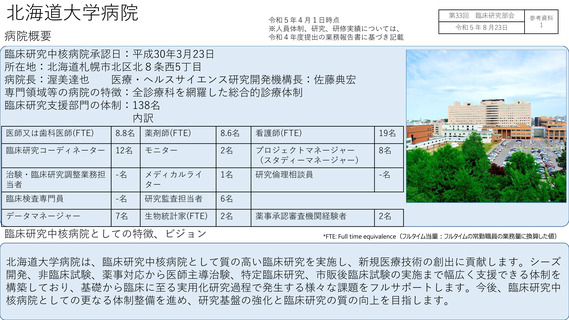
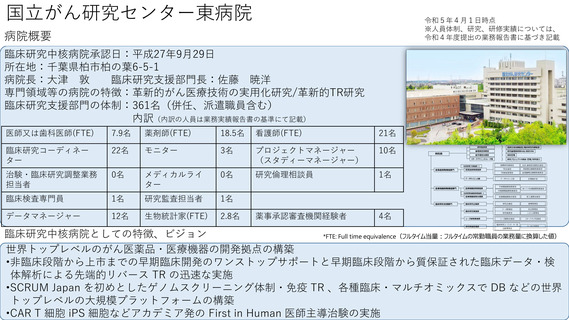
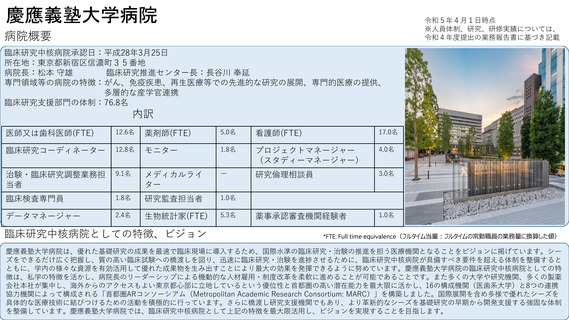
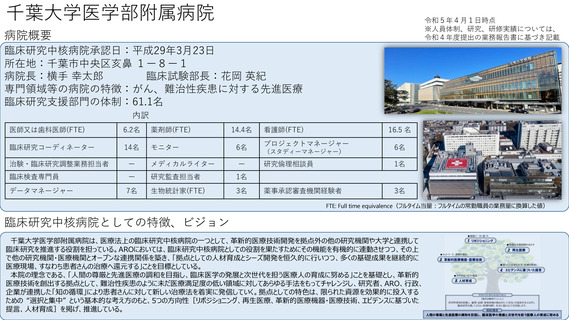
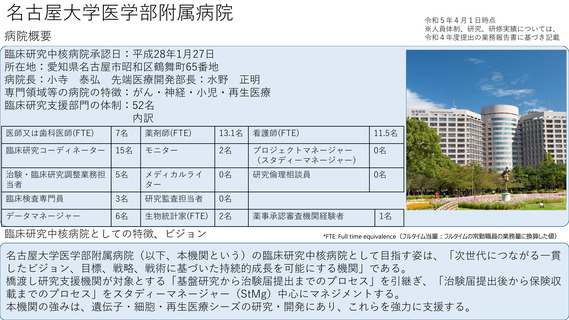
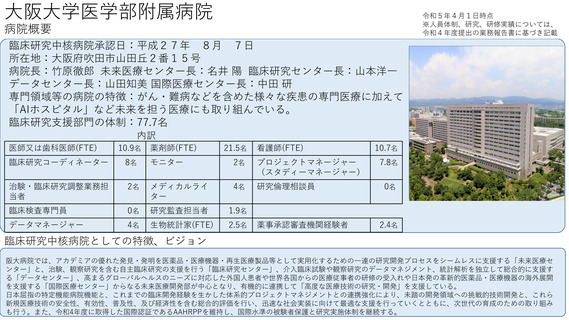
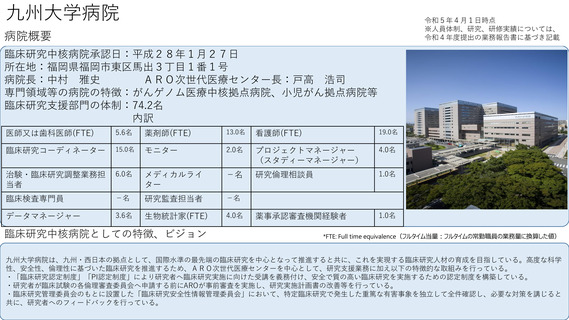
病院概要
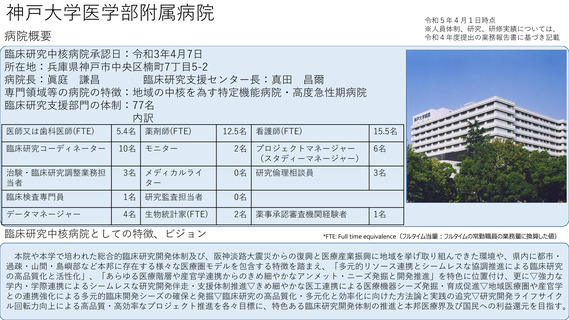
臨床研究中核病院承認日:平成28年3月25日
所在地:東京都文京区本郷7−3−1
病院長:田中 栄
臨床研究推進センター長:森豊 隆志
専門領域等の病院の特徴:がん、精神・神経疾患、感染症、医療機器開発等
臨床研究支援部門の体制:69名
内訳
医師又は歯科医師(FTE)
7.8名
薬剤師(FTE)
21.0名
看護師(FTE)
11.8
名
臨床研究コーディネーター
11名
モニター
2名
プロジェクトマネージャー
(スタディーマネージャー)
4名
治験・臨床研究調整業務担
当者
2名
メディカルライ
ター
0名
研究倫理相談員
1名
臨床検査専門員
6名
研究監査担当者
2名
データマネージャー
4名
生物統計家(FTE)
2名
薬事承認審査機関経験者
3名
臨床研究中核病院としての特徴、ビジョン
病院の画像
*FTE: Full time equivalence(フルタイム当量:フルタイムの常勤職員の業務量に換算した値)
東大病院は、①優れた先端研究と充実した研究インフラに基づく豊富なシーズを有する、②橋渡し研究を推進する有能な人材を吸引する力がある、③臨床研究者の教育研修体制が充実してい
る、④産学連携体制が整っている、などの強みを有する。また革新的医療技術創出拠点としてシーズ開発や医師主導治験等の支援体制を構築してきた。具体的には下記の特徴を有する。①未
承認医薬品等を用いた臨床試験を安全に実施するための試験計画策定を支援。②医師主導治験など開発型の研究を実施しようとする研究者に対し臨床研究推進センター内の医師、薬事・開発
担当者等から成るチームが開発戦略、研究資金、産学連携等について助言。③特定臨床研究等を実施しようとする研究者に対しプロトコル作成やCRB申請を支援。④研究者からのあらゆる相
談にワンストップで対応。⑤医師主導治験等の円滑な推進のためにスタディマネジメント、モニタリング、安全性情報、データマネジメント、統計解析等を支援。⑥医療系ベンチャーの相談
窓口を設置。⑦様々な研究者教育を実施。⑧他拠点の支援人材(医師等治験従事者、上級CRC、データマネージャー、監査等)に対する教育活動を実施。⑨Real World Dataの利活用に向け
た基盤整備を実施。⑩DCTの体制整備。このように東大病院は、基礎研究の成果をシームレスに臨床応用することができる充実した体制を有している。これに基づき、優れた基礎研究に裏打
ちされたシーズを発掘するとともに、引き続きシーズ育成機能と臨床研究推進機能を強化し、今まで構築してきたシーズ開発支援体制を最大限活用してシーズの社会実装を推進する。さらに
他拠点を積極的に支援することによって、わが国を代表する革新的医療技術創出拠点としての活動を一層強力に推進する。
令和5年4月1日時点
※人員体制、研究、研修実績については、
令和4年度提出の業務報告書に基づき記載
病院概要
臨床研究中核病院承認日:平成28年3月25日
所在地:東京都文京区本郷7−3−1
病院長:田中 栄
臨床研究推進センター長:森豊 隆志
専門領域等の病院の特徴:がん、精神・神経疾患、感染症、医療機器開発等
臨床研究支援部門の体制:69名
内訳
医師又は歯科医師(FTE)
7.8名
薬剤師(FTE)
21.0名
看護師(FTE)
11.8
名
臨床研究コーディネーター
11名
モニター
2名
プロジェクトマネージャー
(スタディーマネージャー)
4名
治験・臨床研究調整業務担
当者
2名
メディカルライ
ター
0名
研究倫理相談員
1名
臨床検査専門員
6名
研究監査担当者
2名
データマネージャー
4名
生物統計家(FTE)
2名
薬事承認審査機関経験者
3名
臨床研究中核病院としての特徴、ビジョン
病院の画像
*FTE: Full time equivalence(フルタイム当量:フルタイムの常勤職員の業務量に換算した値)
東大病院は、①優れた先端研究と充実した研究インフラに基づく豊富なシーズを有する、②橋渡し研究を推進する有能な人材を吸引する力がある、③臨床研究者の教育研修体制が充実してい
る、④産学連携体制が整っている、などの強みを有する。また革新的医療技術創出拠点としてシーズ開発や医師主導治験等の支援体制を構築してきた。具体的には下記の特徴を有する。①未
承認医薬品等を用いた臨床試験を安全に実施するための試験計画策定を支援。②医師主導治験など開発型の研究を実施しようとする研究者に対し臨床研究推進センター内の医師、薬事・開発
担当者等から成るチームが開発戦略、研究資金、産学連携等について助言。③特定臨床研究等を実施しようとする研究者に対しプロトコル作成やCRB申請を支援。④研究者からのあらゆる相
談にワンストップで対応。⑤医師主導治験等の円滑な推進のためにスタディマネジメント、モニタリング、安全性情報、データマネジメント、統計解析等を支援。⑥医療系ベンチャーの相談
窓口を設置。⑦様々な研究者教育を実施。⑧他拠点の支援人材(医師等治験従事者、上級CRC、データマネージャー、監査等)に対する教育活動を実施。⑨Real World Dataの利活用に向け
た基盤整備を実施。⑩DCTの体制整備。このように東大病院は、基礎研究の成果をシームレスに臨床応用することができる充実した体制を有している。これに基づき、優れた基礎研究に裏打
ちされたシーズを発掘するとともに、引き続きシーズ育成機能と臨床研究推進機能を強化し、今まで構築してきたシーズ開発支援体制を最大限活用してシーズの社会実装を推進する。さらに
他拠点を積極的に支援することによって、わが国を代表する革新的医療技術創出拠点としての活動を一層強力に推進する。
関連画像
ページ内で利用されている画像ファイルです。
有料会員登録をして頂くことで、このページ内で利用されている画像を個別に閲覧・ダウンロードすることができるようになります。