よむ、つかう、まなぶ。
参考資料1:臨床研究中核病院概要表 (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_34378.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第33回 8/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
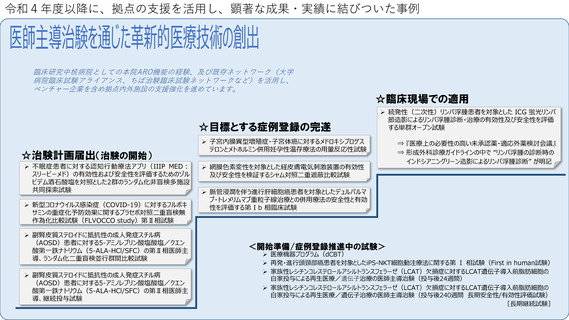
先進医療への対応
・先進医療に関しては、未承認医療機器を用いたFirst in Human の先進医療 B 試験を支援部門が支援し 3 試験実施
・現時点では先進医療B については、 CRC 業務などについては臨床研究コーディネーター室、データセンター機能
などのセントラル機能については臨床研究支援部門もしくは外部CRO などを活用して実施している
患者申出療養への対応
・患者申し出療養の窓口を運営するとともに本制度を活用した他施設主導研究に参加。
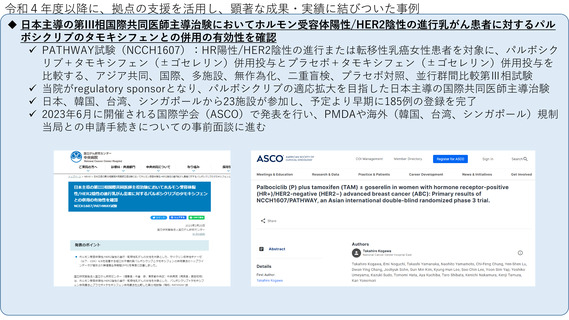
国際共同臨床研究・治験の実施状況
•
SCRUM-Asiaでは、新たにタイ・台湾・マレーシア
の3か国が参加・登録開始
• リキッドバイオプシーによる微小残存腫瘍検出の有
効性評価研究であるCIRCULATE Japanでは観察研究
5,000名、日台共同医師主導治験(ALTAIR)に240名を
超える登録を達成。
(観察研究部分はNature Medicine誌2023に報告)
• 外科切除例の全ゲノム・トランスクリプトーム解析
プロジェクトのTITANIA studyでは目標を超える184
名の登録を実施
• ARCAD-AsiaではARCAD-global(日米仏)と約5万
例の大腸がん比較試験個別データの共有開始
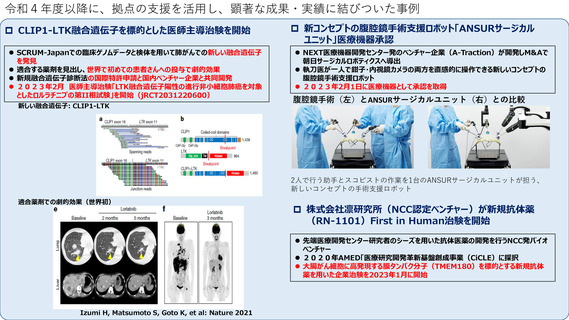
ベンチャー企業への支援実施状況
・NCC発ベンチャー認定制度にて6社が認定ベンチャーとして認定済み
・M&Aで導出した1社の手術支援ロボットが承認取得、1社が新規モノクローナル抗体のFIH治験を開始
・スタートアップ企業を育成するNCC Venture Incubation Program第II期を開始し7チームを支援
・先進医療に関しては、未承認医療機器を用いたFirst in Human の先進医療 B 試験を支援部門が支援し 3 試験実施
・現時点では先進医療B については、 CRC 業務などについては臨床研究コーディネーター室、データセンター機能
などのセントラル機能については臨床研究支援部門もしくは外部CRO などを活用して実施している
患者申出療養への対応
・患者申し出療養の窓口を運営するとともに本制度を活用した他施設主導研究に参加。
国際共同臨床研究・治験の実施状況
•
SCRUM-Asiaでは、新たにタイ・台湾・マレーシア
の3か国が参加・登録開始
• リキッドバイオプシーによる微小残存腫瘍検出の有
効性評価研究であるCIRCULATE Japanでは観察研究
5,000名、日台共同医師主導治験(ALTAIR)に240名を
超える登録を達成。
(観察研究部分はNature Medicine誌2023に報告)
• 外科切除例の全ゲノム・トランスクリプトーム解析
プロジェクトのTITANIA studyでは目標を超える184
名の登録を実施
• ARCAD-AsiaではARCAD-global(日米仏)と約5万
例の大腸がん比較試験個別データの共有開始
ベンチャー企業への支援実施状況
・NCC発ベンチャー認定制度にて6社が認定ベンチャーとして認定済み
・M&Aで導出した1社の手術支援ロボットが承認取得、1社が新規モノクローナル抗体のFIH治験を開始
・スタートアップ企業を育成するNCC Venture Incubation Program第II期を開始し7チームを支援
関連画像
ページ内で利用されている画像ファイルです。
有料会員登録をして頂くことで、このページ内で利用されている画像を個別に閲覧・ダウンロードすることができるようになります。