よむ、つかう、まなぶ。
参考資料1:臨床研究中核病院概要表 (31 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_34378.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第33回 8/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
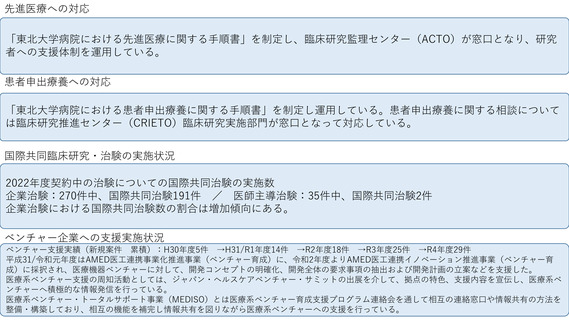
先進医療への対応
先進医療に関する相談窓口を臨床試験部企画調整室に設置し専門職を配置することで、研究者への相談、計画書作成支援など ”ワンストップサービス体制” を構築し、
千葉大学病院および他の医療機関の先進医療実施に向けた、迅速かつ精度の高い支援を提供する体制としている。
種々の先進医療実施に向けた試験実施計画書等の作成は、当院の医師主導治験の支援体制に準じて行っている。骨子作成から段階的にデータマネジメント、統計解
析、品質管理(モニタリング)担当者、臨床研究コーディネーターなどが参加して、試験実施計画書、同意説明文書等の作成を行い、相談窓口では先進医療の開発全般
のロードマップ作成等の支援を行っている。
患者申出療養への対応
患者等からの相談窓口は、患者支援部が対応し、患者申出療養を含めた臨床研究に関する相談については,臨床試験部の担当者と連携し対応している。 患者申出
療養に関する体制の見直しと手順書の整備を令和2年度に行っている。実施についての可否を含めた最終的な検討は,臨床研究に関する病院長のガバナンスを補佐する
臨床研究基盤整備推進・管理委員会で実施している。
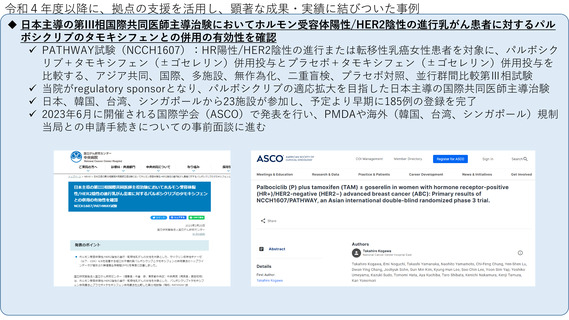
国際共同臨床研究・治験の実施状況
当拠点が支援し、令和2年2月に効能追加の薬事承認を得た「川崎病の急性期(重症であり、冠動脈障害の発生の危険がある場合)に対するシクロスポリン療法」に
ついて、未だ治療適応が未承認のアジア諸国への展開をはかるべく、医療技術実用化総合促進事業/国際共同臨床研究実施推進プログラムを核に、2019年11月当拠
点が主催した “REACTA(日本、マレーシア、台湾、韓国のアカデミアを中心とした国際臨床研究)フォーラム”(※)で培ったアジアの各拠点との連携・活動を通して、
疾病レジストリなどデータの構築、及び臨床上の位置づけについて明確化し、アジア地域での川崎病治療に貢献していくための活動/臨床研究の実施準備を進めている。
※REACTAフォーラム:2019年に引き続き、2023年11月に当拠点が主催して開催することが決定
ベンチャー企業への支援実施状況
臨床研究中核病院として設置する病院内の「ベンチャー支援窓口(相談窓口)」は、学内の「産学連携拠点(IMO)」、「知財」、「臨床評価(薬事、治験)」などの
各組織との仲介役を果たすことで、出口に向けた開発が円滑かつ迅速に進むよう支援している。同時に千葉大亥鼻イノベーションプラザ(中小機構)と連携し、VC情報や
経営に関する人材確保についての情報提供を行い、さらにはMEDISOを始めとする学外の支援基盤を活かすべく、それらとの連携体制を強化している。また、ジャパン・ヘルス
ケアベンチャー・サミットへの出展などを通じ、拠点外からの支援依頼を広く受け付けている。
支援の具体例としては、医学部、看護学部、薬学部の「医療系学部」と「病院」が隣接して存在する亥鼻キャンパスにある “千葉大亥鼻イノベーションプラザ” を核とし、
本学発ベンチャー企業であるセルジェンテック社が実施する医師主導治験の包括的支援を展開している。
先進医療に関する相談窓口を臨床試験部企画調整室に設置し専門職を配置することで、研究者への相談、計画書作成支援など ”ワンストップサービス体制” を構築し、
千葉大学病院および他の医療機関の先進医療実施に向けた、迅速かつ精度の高い支援を提供する体制としている。
種々の先進医療実施に向けた試験実施計画書等の作成は、当院の医師主導治験の支援体制に準じて行っている。骨子作成から段階的にデータマネジメント、統計解
析、品質管理(モニタリング)担当者、臨床研究コーディネーターなどが参加して、試験実施計画書、同意説明文書等の作成を行い、相談窓口では先進医療の開発全般
のロードマップ作成等の支援を行っている。
患者申出療養への対応
患者等からの相談窓口は、患者支援部が対応し、患者申出療養を含めた臨床研究に関する相談については,臨床試験部の担当者と連携し対応している。 患者申出
療養に関する体制の見直しと手順書の整備を令和2年度に行っている。実施についての可否を含めた最終的な検討は,臨床研究に関する病院長のガバナンスを補佐する
臨床研究基盤整備推進・管理委員会で実施している。
国際共同臨床研究・治験の実施状況
当拠点が支援し、令和2年2月に効能追加の薬事承認を得た「川崎病の急性期(重症であり、冠動脈障害の発生の危険がある場合)に対するシクロスポリン療法」に
ついて、未だ治療適応が未承認のアジア諸国への展開をはかるべく、医療技術実用化総合促進事業/国際共同臨床研究実施推進プログラムを核に、2019年11月当拠
点が主催した “REACTA(日本、マレーシア、台湾、韓国のアカデミアを中心とした国際臨床研究)フォーラム”(※)で培ったアジアの各拠点との連携・活動を通して、
疾病レジストリなどデータの構築、及び臨床上の位置づけについて明確化し、アジア地域での川崎病治療に貢献していくための活動/臨床研究の実施準備を進めている。
※REACTAフォーラム:2019年に引き続き、2023年11月に当拠点が主催して開催することが決定
ベンチャー企業への支援実施状況
臨床研究中核病院として設置する病院内の「ベンチャー支援窓口(相談窓口)」は、学内の「産学連携拠点(IMO)」、「知財」、「臨床評価(薬事、治験)」などの
各組織との仲介役を果たすことで、出口に向けた開発が円滑かつ迅速に進むよう支援している。同時に千葉大亥鼻イノベーションプラザ(中小機構)と連携し、VC情報や
経営に関する人材確保についての情報提供を行い、さらにはMEDISOを始めとする学外の支援基盤を活かすべく、それらとの連携体制を強化している。また、ジャパン・ヘルス
ケアベンチャー・サミットへの出展などを通じ、拠点外からの支援依頼を広く受け付けている。
支援の具体例としては、医学部、看護学部、薬学部の「医療系学部」と「病院」が隣接して存在する亥鼻キャンパスにある “千葉大亥鼻イノベーションプラザ” を核とし、
本学発ベンチャー企業であるセルジェンテック社が実施する医師主導治験の包括的支援を展開している。