よむ、つかう、まなぶ。
資料2-1第2 回制度部会資料 (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_30193.html |
| 出典情報 | 厚生科学審議会 医薬品医療機器制度部会(令和4年度第2回 1/12)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
1
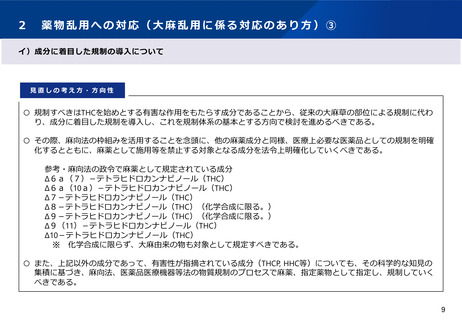
医療ニーズへの対応(大麻由来医薬品に係る取扱い)
見直しの考え方・方向性
○ 国際整合性を図り、医療ニーズに対応する観点から、以下の方向性で見直しを図るべきである。
・大麻から製造された医薬品であって、有効性・安全性が確認され、薬機法に基づく承認を得た医薬品について、
その輸入、製造及び施用を可能とすること
・このため大麻取締法第4条においては、大麻から製造された医薬品の施用・受施用、交付を禁止していることか
ら、当該第4条等の関係条項を改正すること
・他の麻薬成分の医薬品と同様、大麻及び大麻成分についても、麻向法に基づく麻薬製造・製剤、流通、施用に関
する免許制度等の流通管理の仕組みを導入すること
○ その際、「大麻を使用してよい」といった大麻乱用に繋がるような誤った認識が広がらないように留意するととも
に、大麻由来の医薬品を麻向法における麻薬の流通管理に移行していくに当たり、当該医薬品が麻薬となる場合に、
医薬品の製造・販売業者や医療関係者においても、麻薬として適正に管理されるよう薬剤の管理を徹底していくこ
とや、患者にとって負担にならない円滑な施用や薬剤管理のあり方を検討していく必要がある。
○ なお、現行の大麻取締法において実施している大麻から製造された医薬品に係る治験については、治験参加者に対
しても当該医薬品の厳重な管理を求められているが、制度見直し後においては、他の麻薬と同様の水準での管理に
留まる点を含め、円滑な施用が可能となるよう、十分な周知・徹底を図るべきである。
5
医療ニーズへの対応(大麻由来医薬品に係る取扱い)
見直しの考え方・方向性
○ 国際整合性を図り、医療ニーズに対応する観点から、以下の方向性で見直しを図るべきである。
・大麻から製造された医薬品であって、有効性・安全性が確認され、薬機法に基づく承認を得た医薬品について、
その輸入、製造及び施用を可能とすること
・このため大麻取締法第4条においては、大麻から製造された医薬品の施用・受施用、交付を禁止していることか
ら、当該第4条等の関係条項を改正すること
・他の麻薬成分の医薬品と同様、大麻及び大麻成分についても、麻向法に基づく麻薬製造・製剤、流通、施用に関
する免許制度等の流通管理の仕組みを導入すること
○ その際、「大麻を使用してよい」といった大麻乱用に繋がるような誤った認識が広がらないように留意するととも
に、大麻由来の医薬品を麻向法における麻薬の流通管理に移行していくに当たり、当該医薬品が麻薬となる場合に、
医薬品の製造・販売業者や医療関係者においても、麻薬として適正に管理されるよう薬剤の管理を徹底していくこ
とや、患者にとって負担にならない円滑な施用や薬剤管理のあり方を検討していく必要がある。
○ なお、現行の大麻取締法において実施している大麻から製造された医薬品に係る治験については、治験参加者に対
しても当該医薬品の厳重な管理を求められているが、制度見直し後においては、他の麻薬と同様の水準での管理に
留まる点を含め、円滑な施用が可能となるよう、十分な周知・徹底を図るべきである。
5