よむ、つかう、まなぶ。
費-6日本医療機器産業連合会、日本医療機器テクノロジー協会、米国医療機器・IVD工業会、欧州ビジネス協会(EBC)医療機器・IVD委員会 (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_60773.html |
| 出典情報 | 中央社会保険医療協議会 費用対効果評価専門部会(第71回 8/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
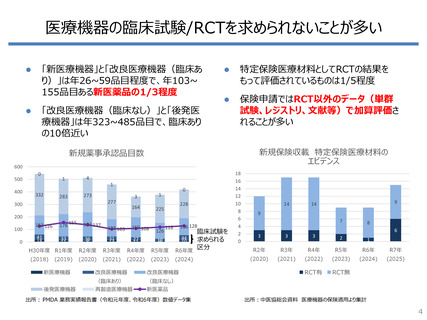
医療機器の臨床試験/RCTを求められないことが多い
「新医療機器」と「改良医療機器(臨床あ
り)」は年26~59品目程度で、年103~
155品目ある新医薬品の1/3程度
⚫
「改良医療機器(臨床なし)」と「後発医
療機器」は年323~485品目で、臨床あり
の10倍近い
⚫
⚫
特定保険医療材料としてRCTの結果を
もって評価されているものは1/5程度
⚫
保険申請ではRCT以外のデータ(単群
試験、レジストリ、文献等)で加算評価さ
れることが多い
新規保険収載 特定保険医療材料の
エビデンス
新規薬事承認品目数
600
500
0
4
1
1
400
332
3
1
164
225
273
283
277
300
0
228
200
153 126
178
155
193 137
159 108
138 103
136 128
118
臨床試験を
44
31
33
36
27
求められる
19
13
11
11
10
8
7
0
区分
H30年度 R1年度 R2年度 R3年度 R4年度 R5年度 R6年度
100
126
41
18
(2018)
(2019)
新医療機器
後発医療機器
(2020)
(2021)
(2022)
(2023)
(2024)
改良医療機器
改良医療機器
(臨床あり)
(臨床なし)
再製造医療機器
新医薬品
出所: PMDA 業務実績報告書(令和元年度、令和6年度)数値データ集
18
16
14
12
10
8
6
4
2
0
14
9
14
9
7
8
6
3
3
3
2
1
R2年
R3年
R4年
R5年
R6年
R7年
(2020)
(2021)
(2022)
(2023)
(2024)
(2025)
RCT有
RCT無
出所:中医協総会資料 医療機器の保険適用より集計
4
「新医療機器」と「改良医療機器(臨床あ
り)」は年26~59品目程度で、年103~
155品目ある新医薬品の1/3程度
⚫
「改良医療機器(臨床なし)」と「後発医
療機器」は年323~485品目で、臨床あり
の10倍近い
⚫
⚫
特定保険医療材料としてRCTの結果を
もって評価されているものは1/5程度
⚫
保険申請ではRCT以外のデータ(単群
試験、レジストリ、文献等)で加算評価さ
れることが多い
新規保険収載 特定保険医療材料の
エビデンス
新規薬事承認品目数
600
500
0
4
1
1
400
332
3
1
164
225
273
283
277
300
0
228
200
153 126
178
155
193 137
159 108
138 103
136 128
118
臨床試験を
44
31
33
36
27
求められる
19
13
11
11
10
8
7
0
区分
H30年度 R1年度 R2年度 R3年度 R4年度 R5年度 R6年度
100
126
41
18
(2018)
(2019)
新医療機器
後発医療機器
(2020)
(2021)
(2022)
(2023)
(2024)
改良医療機器
改良医療機器
(臨床あり)
(臨床なし)
再製造医療機器
新医薬品
出所: PMDA 業務実績報告書(令和元年度、令和6年度)数値データ集
18
16
14
12
10
8
6
4
2
0
14
9
14
9
7
8
6
3
3
3
2
1
R2年
R3年
R4年
R5年
R6年
R7年
(2020)
(2021)
(2022)
(2023)
(2024)
(2025)
RCT有
RCT無
出所:中医協総会資料 医療機器の保険適用より集計
4