よむ、つかう、まなぶ。
費-6日本医療機器産業連合会、日本医療機器テクノロジー協会、米国医療機器・IVD工業会、欧州ビジネス協会(EBC)医療機器・IVD委員会 (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_60773.html |
| 出典情報 | 中央社会保険医療協議会 費用対効果評価専門部会(第71回 8/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
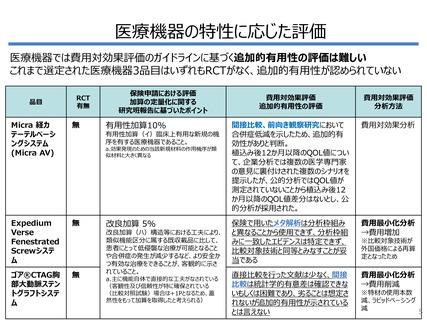
医療機器の特性に応じた評価
■医療機器特有の臨床エビデンス事情
• 比較試験の実施が困難な場合が多い
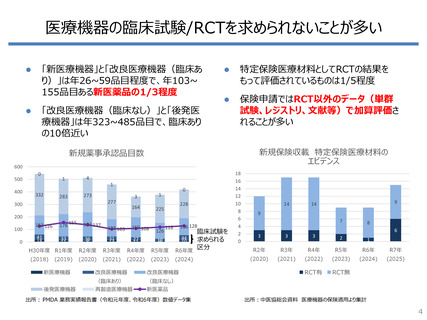
• 薬事承認では臨床試験を求められないことが多く、臨床試験が求められた
場合でもRCTを実施することはかなり少ない
• 保険申請ではRCT以外のデータ(単群試験、レジストリ、文献等)で
加算評価されることが多い
■費用対効果評価制度における課題
• RCT以外のデータによる間接比較では追加的有用性を示すことが困難
– 観察研究やレジストリデータの再解析は患者背景調整が不十分となりやすい
– 単群試験が多く、質の高い間接比較が困難
– 追加的有用性が示せず、費用最小化分析となる事例が続く
•
医療機器は不利な立場に置かれている
■提案
• RCTのような強力なエビデンスがない品目は分析に不向きなため、
費用対効果評価の対象外とする
3
■医療機器特有の臨床エビデンス事情
• 比較試験の実施が困難な場合が多い
• 薬事承認では臨床試験を求められないことが多く、臨床試験が求められた
場合でもRCTを実施することはかなり少ない
• 保険申請ではRCT以外のデータ(単群試験、レジストリ、文献等)で
加算評価されることが多い
■費用対効果評価制度における課題
• RCT以外のデータによる間接比較では追加的有用性を示すことが困難
– 観察研究やレジストリデータの再解析は患者背景調整が不十分となりやすい
– 単群試験が多く、質の高い間接比較が困難
– 追加的有用性が示せず、費用最小化分析となる事例が続く
•
医療機器は不利な立場に置かれている
■提案
• RCTのような強力なエビデンスがない品目は分析に不向きなため、
費用対効果評価の対象外とする
3