よむ、つかう、まなぶ。
07 参考資料2-1 帯状疱疹ワクチン ファクトシート (28 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36248.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会 ワクチン評価に関する小委員会(第21回 11/9)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
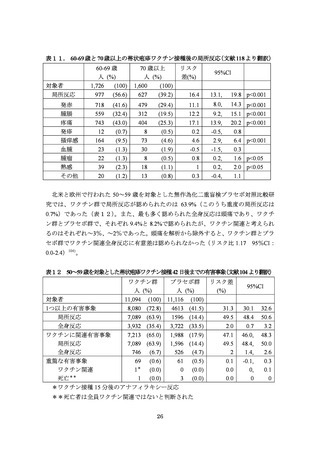
人を対象とした別のプラセボ対照、無作為化二重盲検群間比較研究の報告では、帯状疱疹発症阻止
効果は 69.8%であった 104)。ワクチン効果を年齢別に解析すると、60 代の被接種者における帯状疱疹
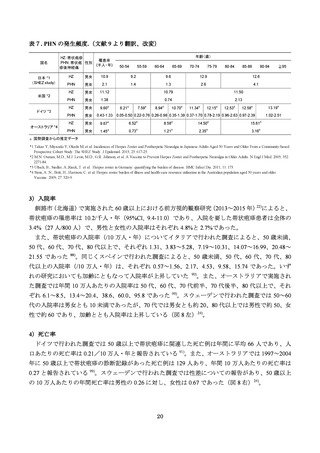
の発症阻止効果は 70 代以上のそれより高かった。一方で PHN 発症阻止効果、及び疾病負荷につい
ては両年齢間に違いはなかった 103)。
③
持続性
ZOSTAVAX®接種後の発症阻止効果の持続性も調べられている。接種後 4~7 年間では帯状疱疹発
症と PHN 発症が、それぞれ 39.6%、60.1%減少し、疾病による死亡や損失した生活の質を示す疾病
負荷は 50.1%減少することが明らかにされた。また、接種後 7~11 年間では、帯状疱疹発症と PHN
発症が、それぞれ 21.1%、35.4%減少し、疾病負荷が 37.3%減少したと報告されている 112,113)。さらに、
60 歳以上の 176,078 人を対象とした研究では、ワクチン接種後 1 年以内の帯状疱疹発症阻止効果は
ワクチン非接種者と比較して 68.7%減少したが、接種 8 年目ではその効果は 4.2%に低下した 114)。
(4)安全性の観点(副反応の頻度、重篤な副反応等)
①
接種に係る安全性
1)国内臨床治験 115-117)
帯状疱疹の予防を目的に、50 歳以上の健康成人 259 人に対して国内臨床試験が実施された(阪大微
研乾燥弱毒生水痘ワクチン国内臨床試験:CTD5.3.5.2-1:BKHZ1 試験)
。接種から 6~8 週後までに発
現した有害事象の発現割合は 56.0%(145/259 人)で、副反応は 50.6%(131/259 人)に認められた 117)。
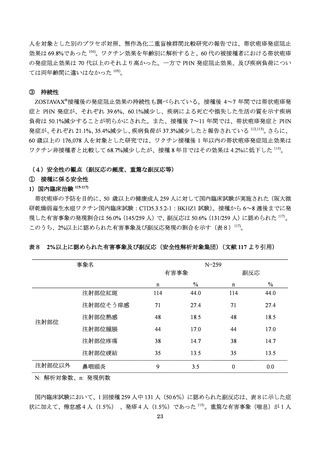
このうち、2%以上に認められた有害事象及び副反応発現の割合を示す(表8)117)。
表8
2%以上に認められた有害事象及び副反応(安全性解析対象集団)(文献 117 より引用)
N=259
事象名
有害事象
注射部位
注射部位以外
副反応
注射部位紅斑
n
114
%
44.0
n
114
%
44.0
注射部位そう痒感
71
27.4
71
27.4
注射部位熱感
48
18.5
48
18.5
注射部位腫脹
44
17.0
44
17.0
注射部位疼痛
38
14.7
38
14.7
注射部位硬結
35
13.5
35
13.5
鼻咽頭炎
9
3.5
0
0.0
N: 解析対象数、n: 発現例数
国内臨床試験において、1 回接種 259 人中 131 人(50.6%)に認められた副反応は、表8に示した症
状に加えて、倦怠感 4 人(1.5%) 、発疹 4 人(1.5%)であった 115)。重篤な有害事象(喘息)が 1 人
23
効果は 69.8%であった 104)。ワクチン効果を年齢別に解析すると、60 代の被接種者における帯状疱疹
の発症阻止効果は 70 代以上のそれより高かった。一方で PHN 発症阻止効果、及び疾病負荷につい
ては両年齢間に違いはなかった 103)。
③
持続性
ZOSTAVAX®接種後の発症阻止効果の持続性も調べられている。接種後 4~7 年間では帯状疱疹発
症と PHN 発症が、それぞれ 39.6%、60.1%減少し、疾病による死亡や損失した生活の質を示す疾病
負荷は 50.1%減少することが明らかにされた。また、接種後 7~11 年間では、帯状疱疹発症と PHN
発症が、それぞれ 21.1%、35.4%減少し、疾病負荷が 37.3%減少したと報告されている 112,113)。さらに、
60 歳以上の 176,078 人を対象とした研究では、ワクチン接種後 1 年以内の帯状疱疹発症阻止効果は
ワクチン非接種者と比較して 68.7%減少したが、接種 8 年目ではその効果は 4.2%に低下した 114)。
(4)安全性の観点(副反応の頻度、重篤な副反応等)
①
接種に係る安全性
1)国内臨床治験 115-117)
帯状疱疹の予防を目的に、50 歳以上の健康成人 259 人に対して国内臨床試験が実施された(阪大微
研乾燥弱毒生水痘ワクチン国内臨床試験:CTD5.3.5.2-1:BKHZ1 試験)
。接種から 6~8 週後までに発
現した有害事象の発現割合は 56.0%(145/259 人)で、副反応は 50.6%(131/259 人)に認められた 117)。
このうち、2%以上に認められた有害事象及び副反応発現の割合を示す(表8)117)。
表8
2%以上に認められた有害事象及び副反応(安全性解析対象集団)(文献 117 より引用)
N=259
事象名
有害事象
注射部位
注射部位以外
副反応
注射部位紅斑
n
114
%
44.0
n
114
%
44.0
注射部位そう痒感
71
27.4
71
27.4
注射部位熱感
48
18.5
48
18.5
注射部位腫脹
44
17.0
44
17.0
注射部位疼痛
38
14.7
38
14.7
注射部位硬結
35
13.5
35
13.5
鼻咽頭炎
9
3.5
0
0.0
N: 解析対象数、n: 発現例数
国内臨床試験において、1 回接種 259 人中 131 人(50.6%)に認められた副反応は、表8に示した症
状に加えて、倦怠感 4 人(1.5%) 、発疹 4 人(1.5%)であった 115)。重篤な有害事象(喘息)が 1 人
23