よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況 (55 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26332.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第1回 6/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
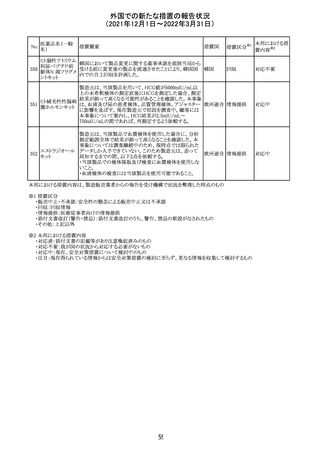
外国での新たな措置の報告状況
(2021年12月1日~2022年3月31日)
No.
医薬品名(一般
名)
前立腺特異抗原
キット
血液検査用卵胞
刺激ホルモンキッ
ト
甲状腺刺激ホル
330 モンキット
ベータ2-マイクロ
グロブリンキット
プロラクチンキット
癌胎児性抗原
キット
前立腺特異抗原
キット
血液検査用卵胞
刺激ホルモンキッ
ト
甲状腺刺激ホル
331 モンキット
ベータ2-マイクロ
グロブリンキット
プロラクチンキット
癌胎児性抗原
キット
エストラジオール
キット
遊離サイロキシン
キット
血液検査用黄体
形成ホルモンキッ
ト
ムンプスウイルス
キット
麻疹ウイルス免疫
グロブリンG抗体
キット
風疹ウイルス免疫
332
グロブリンGキット
遊離トリヨードサイ
ロニンキット
トリヨードサイロニ
ンキット
サイロキシンキット
フェリチンキット
アルファーフェト
プロテインキット
血液検査用テスト
ステロンキット
抗ミュラー管ホル
モンキット
※1
本邦における措
置内容※2
措置概要
措置国
【第1報】【第2報】
使用者からの報告を受けて、製造元が調査したところ、
2021年2月以降に製造されたキットの試薬ストリップに含ま
れる蛍光基質のバッチが通常よりも早く劣化したことによっ
て、基質エラーの発生頻度が通常のレベルを超えて増加
し、臨床検体を用いた試験の結果報告が遅延する可能性
があることがわかった。これにより、当該ロットの納品先に、
対象製品の使用を中止し、廃棄するよう依頼する。なお、製
造元でのリスク分析の結果、本製品において、結果報告の
遅延によって患者へ影響が生じるリスクはないことがわかっ
た。
【第3報】
原料供給元と協力して蛍光基質原料の管理方法を改め、
製造に使用する前に劣化速度を確認し、異常の無い蛍光
基質原料のみを製造に使用する手順に変更した。これによ
り、対象製品を納品した医療機関等に、本事象の特定され
た原因及び講じられた再発防止策とともに、本事象が発生
しない製品の製造が開始されたことを情報提供する。
フランス、
オーストラ
リア、
情報提供
イギリス、
ドイツ
対応中
【第1報】【第2報】
使用者からの報告を受けて、製造元が調査したところ、
2021年2月以降に製造されたキットの試薬ストリップに含ま
れる蛍光基質のバッチが通常よりも早く劣化したことによっ
て、基質エラーの発生頻度が通常のレベルを超えて増加
し、臨床検体を用いた試験の結果報告が遅延する可能性
があることがわかった。これにより、暫定措置として、使用者
に本事象が発生しない使用期限(推奨使用期限)内に製品
をご使用いただくように注意喚起する。なお、製造元でのリ
スク分析の結果、本製品において、結果報告の遅延によっ
て患者へ影響が生じるリスクはないことがわかった。
【第3報】
原料供給元と協力して蛍光基質原料の管理方法を改め、
製造に使用する前に劣化速度を確認し、異常の無い蛍光
基質原料のみを製造に使用する手順に変更した。これによ
り、対象製品を納品した医療機関等に、本事象の特定され
た原因及び講じられた再発防止策とともに、本事象が発生
しない製品の製造が開始されたことを情報提供する。
フランス、
オーストラ
リア、
情報提供
イギリス、
ドイツ
対応中
【第1報】
使用者からの報告を受けて、製造元が調査したところ、
2021年2月以降に製造されたキットの試薬ストリップに含ま
れる蛍光基質のバッチが通常よりも早く劣化したことによっ
て、基質エラーの発生頻度が通常のレベルを超えて増加
し、臨床検体を用いた試験の結果報告が遅延する可能性
があることがわかった。これにより、暫定措置として、使用者
に本事象が発生しない使用期限(推奨使用期限)内に製品
をご使用いただくように注意喚起する。なお、製造元でのリ
スク分析の結果、本製品において、結果報告の遅延によっ
て患者へ影響が生じるリスクはないことがわかった。
【第2報】
原料供給元と協力して蛍光基質原料の管理方法を改め、
製造に使用する前に劣化速度を確認し、異常の無い蛍光
基質原料のみを製造に使用する手順に変更した。これによ
り、対象製品を納品した医療機関等に、本事象の特定され
た原因及び講じられた再発防止策とともに、本事象が発生
しない製品の製造が開始されたことを情報提供する。
フランス、
オーストラ
リア、
情報提供
イギリス、
ドイツ
対応中
55
措置区分
(2021年12月1日~2022年3月31日)
No.
医薬品名(一般
名)
前立腺特異抗原
キット
血液検査用卵胞
刺激ホルモンキッ
ト
甲状腺刺激ホル
330 モンキット
ベータ2-マイクロ
グロブリンキット
プロラクチンキット
癌胎児性抗原
キット
前立腺特異抗原
キット
血液検査用卵胞
刺激ホルモンキッ
ト
甲状腺刺激ホル
331 モンキット
ベータ2-マイクロ
グロブリンキット
プロラクチンキット
癌胎児性抗原
キット
エストラジオール
キット
遊離サイロキシン
キット
血液検査用黄体
形成ホルモンキッ
ト
ムンプスウイルス
キット
麻疹ウイルス免疫
グロブリンG抗体
キット
風疹ウイルス免疫
332
グロブリンGキット
遊離トリヨードサイ
ロニンキット
トリヨードサイロニ
ンキット
サイロキシンキット
フェリチンキット
アルファーフェト
プロテインキット
血液検査用テスト
ステロンキット
抗ミュラー管ホル
モンキット
※1
本邦における措
置内容※2
措置概要
措置国
【第1報】【第2報】
使用者からの報告を受けて、製造元が調査したところ、
2021年2月以降に製造されたキットの試薬ストリップに含ま
れる蛍光基質のバッチが通常よりも早く劣化したことによっ
て、基質エラーの発生頻度が通常のレベルを超えて増加
し、臨床検体を用いた試験の結果報告が遅延する可能性
があることがわかった。これにより、当該ロットの納品先に、
対象製品の使用を中止し、廃棄するよう依頼する。なお、製
造元でのリスク分析の結果、本製品において、結果報告の
遅延によって患者へ影響が生じるリスクはないことがわかっ
た。
【第3報】
原料供給元と協力して蛍光基質原料の管理方法を改め、
製造に使用する前に劣化速度を確認し、異常の無い蛍光
基質原料のみを製造に使用する手順に変更した。これによ
り、対象製品を納品した医療機関等に、本事象の特定され
た原因及び講じられた再発防止策とともに、本事象が発生
しない製品の製造が開始されたことを情報提供する。
フランス、
オーストラ
リア、
情報提供
イギリス、
ドイツ
対応中
【第1報】【第2報】
使用者からの報告を受けて、製造元が調査したところ、
2021年2月以降に製造されたキットの試薬ストリップに含ま
れる蛍光基質のバッチが通常よりも早く劣化したことによっ
て、基質エラーの発生頻度が通常のレベルを超えて増加
し、臨床検体を用いた試験の結果報告が遅延する可能性
があることがわかった。これにより、暫定措置として、使用者
に本事象が発生しない使用期限(推奨使用期限)内に製品
をご使用いただくように注意喚起する。なお、製造元でのリ
スク分析の結果、本製品において、結果報告の遅延によっ
て患者へ影響が生じるリスクはないことがわかった。
【第3報】
原料供給元と協力して蛍光基質原料の管理方法を改め、
製造に使用する前に劣化速度を確認し、異常の無い蛍光
基質原料のみを製造に使用する手順に変更した。これによ
り、対象製品を納品した医療機関等に、本事象の特定され
た原因及び講じられた再発防止策とともに、本事象が発生
しない製品の製造が開始されたことを情報提供する。
フランス、
オーストラ
リア、
情報提供
イギリス、
ドイツ
対応中
【第1報】
使用者からの報告を受けて、製造元が調査したところ、
2021年2月以降に製造されたキットの試薬ストリップに含ま
れる蛍光基質のバッチが通常よりも早く劣化したことによっ
て、基質エラーの発生頻度が通常のレベルを超えて増加
し、臨床検体を用いた試験の結果報告が遅延する可能性
があることがわかった。これにより、暫定措置として、使用者
に本事象が発生しない使用期限(推奨使用期限)内に製品
をご使用いただくように注意喚起する。なお、製造元でのリ
スク分析の結果、本製品において、結果報告の遅延によっ
て患者へ影響が生じるリスクはないことがわかった。
【第2報】
原料供給元と協力して蛍光基質原料の管理方法を改め、
製造に使用する前に劣化速度を確認し、異常の無い蛍光
基質原料のみを製造に使用する手順に変更した。これによ
り、対象製品を納品した医療機関等に、本事象の特定され
た原因及び講じられた再発防止策とともに、本事象が発生
しない製品の製造が開始されたことを情報提供する。
フランス、
オーストラ
リア、
情報提供
イギリス、
ドイツ
対応中
55
措置区分