よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況 (25 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26332.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第1回 6/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
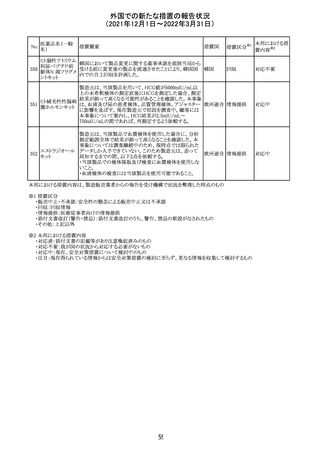
外国での新たな措置の報告状況
(2021年12月1日~2022年3月31日)
No.
医薬品名(一般
名)
措置概要
措置国
措置区分
※1
本邦における措
置内容※2
【第1報、第2報】
欧州EMAのPRACは、2022年1月10日~13日に開催された
会合にて、本剤接種後の非常にまれな横断性脊髄炎に関
する警告を含め、頻度不明の副反応として追加するよう欧
州添付文書の改訂を勧告した。
PRACは、本剤について、欧州の副作用報告データベース
(EudraVigilance)に登録されている症例や科学文献からの
データなど、世界中で報告されている入手可能な情報を検
討し、本剤と横断性脊髄炎との因果関係について少なくと
も合理的な可能性があると結論付けた。本剤のベネフィッ
ト・リスクプロファイルに変更はないとしている。
コロナウイルス(S
ARS-CoV-
2)ワクチン(遺伝
138
子組換えサルア
デノウイルスベク
ター)
【第3報、第4報】
PRACの勧告に基づき欧州製品情報の改訂が実施され、
2022年2月7日付で改訂版が欧州EMAのウェブサイトに掲 欧州連
載された。
合、
改訂内容は以下のとおり。
イギリス
・「Special warnings and precautions for use」の項の神経学
的事象に関する記載に横断性脊髄炎を追加。
・「Undesirable effects」の項に、副反応として「神経系障害:
横断性脊髄炎(頻度不明)」を追加。
その他
注目
その他
注目
また英国においても2022年1月26日付で製品情報が改訂さ
れた。
改訂内容は以下のとおり。
・「Special warnings and precautions for use」の神経学的事
象の項に横断性脊髄炎に関する注意喚起を追加。
・「Undesirable effects」の項に、副反応として「神経系障害:
横断性脊髄炎(頻度不明)」を追加。
なお、欧州および英国ともにPackage leafletも改訂された。
【第1報、第2報】
英国において顔面麻痺に関する製品情報の改訂が実施さ
れ、改訂版が英国政府のウェブサイトに掲載された(改訂
日:2022年1月4日)。
コロナウイルス(S
改訂内容は以下のとおり。
ARS-CoV-
・Undesirable effectsの項に、まれな神経系障害として「顔
2)ワクチン(遺伝
139
面麻痺」を追加。
イギリス
子組換えサルア
当該改訂情報はPackage Leafletにも反映された。
デノウイルスベク
なお、改訂根拠となった症例は、米国、ペルーおよびチリ
ター)
で実施された臨床試験のデータに基づいており、2021年3
月5日までの安全性追跡期間において、本剤接種群の5例
に顔面麻痺(または顔面神経麻痺)が発現したが、いずれ
も非重篤と報告された。
ポリエチレングリ
コール処理人免
疫グロブリン
ポリエチレングリ
コール処理人免
140 疫グロブリン
pH4処理酸性人
免疫グロブリン
pH4処理酸性人
免疫グロブリン
人免疫グロブリン
【第1報及び第2報】
フランス及び英国において、Gammagard(人免疫グロブリン
フランス、
製剤)のバイアルバックに付いている輸液セットの品質に問
回収
イギリス
題が生じたため、一部のロット(5g製剤:12ロット、10g製剤:
18ロット)が自主回収された。
25
対応不要
(2021年12月1日~2022年3月31日)
No.
医薬品名(一般
名)
措置概要
措置国
措置区分
※1
本邦における措
置内容※2
【第1報、第2報】
欧州EMAのPRACは、2022年1月10日~13日に開催された
会合にて、本剤接種後の非常にまれな横断性脊髄炎に関
する警告を含め、頻度不明の副反応として追加するよう欧
州添付文書の改訂を勧告した。
PRACは、本剤について、欧州の副作用報告データベース
(EudraVigilance)に登録されている症例や科学文献からの
データなど、世界中で報告されている入手可能な情報を検
討し、本剤と横断性脊髄炎との因果関係について少なくと
も合理的な可能性があると結論付けた。本剤のベネフィッ
ト・リスクプロファイルに変更はないとしている。
コロナウイルス(S
ARS-CoV-
2)ワクチン(遺伝
138
子組換えサルア
デノウイルスベク
ター)
【第3報、第4報】
PRACの勧告に基づき欧州製品情報の改訂が実施され、
2022年2月7日付で改訂版が欧州EMAのウェブサイトに掲 欧州連
載された。
合、
改訂内容は以下のとおり。
イギリス
・「Special warnings and precautions for use」の項の神経学
的事象に関する記載に横断性脊髄炎を追加。
・「Undesirable effects」の項に、副反応として「神経系障害:
横断性脊髄炎(頻度不明)」を追加。
その他
注目
その他
注目
また英国においても2022年1月26日付で製品情報が改訂さ
れた。
改訂内容は以下のとおり。
・「Special warnings and precautions for use」の神経学的事
象の項に横断性脊髄炎に関する注意喚起を追加。
・「Undesirable effects」の項に、副反応として「神経系障害:
横断性脊髄炎(頻度不明)」を追加。
なお、欧州および英国ともにPackage leafletも改訂された。
【第1報、第2報】
英国において顔面麻痺に関する製品情報の改訂が実施さ
れ、改訂版が英国政府のウェブサイトに掲載された(改訂
日:2022年1月4日)。
コロナウイルス(S
改訂内容は以下のとおり。
ARS-CoV-
・Undesirable effectsの項に、まれな神経系障害として「顔
2)ワクチン(遺伝
139
面麻痺」を追加。
イギリス
子組換えサルア
当該改訂情報はPackage Leafletにも反映された。
デノウイルスベク
なお、改訂根拠となった症例は、米国、ペルーおよびチリ
ター)
で実施された臨床試験のデータに基づいており、2021年3
月5日までの安全性追跡期間において、本剤接種群の5例
に顔面麻痺(または顔面神経麻痺)が発現したが、いずれ
も非重篤と報告された。
ポリエチレングリ
コール処理人免
疫グロブリン
ポリエチレングリ
コール処理人免
140 疫グロブリン
pH4処理酸性人
免疫グロブリン
pH4処理酸性人
免疫グロブリン
人免疫グロブリン
【第1報及び第2報】
フランス及び英国において、Gammagard(人免疫グロブリン
フランス、
製剤)のバイアルバックに付いている輸液セットの品質に問
回収
イギリス
題が生じたため、一部のロット(5g製剤:12ロット、10g製剤:
18ロット)が自主回収された。
25
対応不要