よむ、つかう、まなぶ。
総-6-2最適使用推進ガイドライン(アムシェプリ) (8 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_73124.html |
| 出典情報 | 中央社会保険医療協議会 総会(第650回 5/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
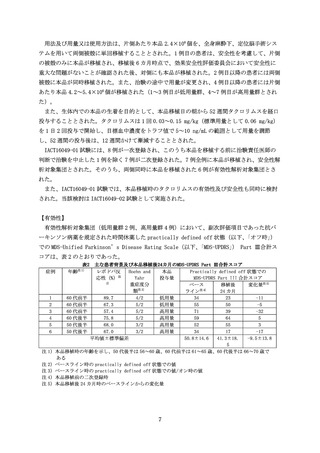
(1) オフ時 MDS-UPDRS Part III 合計スコア
オフ時の MDS-UPDRS Part Ⅲ合計スコアについて、有効性解析対象集団の 6 例中 4 例で著効3)
と判断された。移植後 24 カ月に著効とならなかった 2 例(高用量群:症例 4、症例 5)のうち 1
例(症例 5)は、移植後 18 カ月まで改善が認められていたが、移植後 24 カ月に+3 となり悪化
した。もう 1 例(症例 4)は移植後 4 週にスコアが上昇し、以降は移植後 24 カ月まで低下した
が、ベースラインからの変化量は+5 となり悪化した。
(2) 移植細胞の生着及び機能評価
有効性解析対象集団 6 例における[18F]FDOPA の集積が本品の移植部位である被殻に定性的に
確認された。移植後 24 カ月において、被殻での Ki 値は 6 例中 5 例でベースラインから増加し
ており、また、被殻/尾状核比4)は 6 例全例でベースラインから増加した。
また、生着の判定は、IACT16049-02 試験において移植後 12 カ月及び 24 カ月時点で行われ
た。客観性を担保するため、評価時期までに得られた MRI 画像及び PET 画像([18F]FDOPA 及び
[18F]GE1805))を用いて、被殻での生着の有無を脳神経内科医及び放射線科医による合議の上
で判定された。有効性解析対象集団 6 例全例で、移植後 12 カ月及び 24 カ月のいずれの時点で
も被殻に生着ありと判定された。
(3) 累積拒絶反応抑制率(非発現率)
IACT16049-02 試験における主要評価項目とされた本品移植後 12 週及び 12 カ月の累積拒絶反
応抑制率(非発現率)6)について、いずれの時点においても累積拒絶反応抑制率(非発現率)は
100%(6/6 例)であり、有効性解析対象の 6 例全例で拒絶反応なしと判定された。
【安全性】
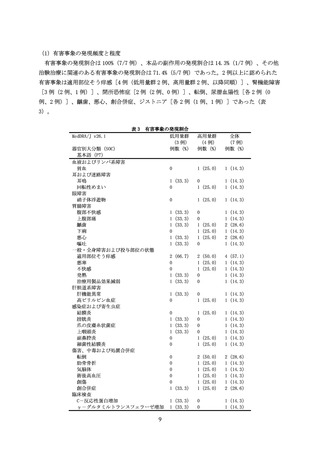
IACT16049-01 試験の主要評価項目は、(1)有害事象の発現頻度と程度及び(2)移植後 24 カ
月における脳内の移植片増大(3 cm3 を超える)7)の有無(MRI)とされた。主要評価項目の結果
は、以下のとおりであった。
3)
事前に治験実施計画書において、偽手術又は標準治療でのオフ時の MDS-UPDRS Part Ⅲの 1~2 年間の推移に
係る以下の報告に基づき、ベースラインから移植後 24 カ月にオフ時の MDS-UPDRS Part Ⅲ合計スコアの 5 点
以上の改善を著効、0~4 点の改善を有効と定義した。
・ドパミン神経細胞移植を検討した臨床試験(Ann Neurol. 2003; 54: 403-14、N Engl J Med 2001; 8;
344: 710-9)では変化なし又は悪化。
・DBS を検討した臨床試験(Lancet Neurol 2010; 9: 581-91)では変化なし。
4)
本品を移植していない尾状核に対する本品を移植した被殻での Ki 値の比。
5)
活性化ミクログリアに発現するとされる translocator protein に対するアンタゴニスト。神経炎症反応の
評価に使用された。
6)
本品移植後 12 週間及び 12 カ月間に拒絶反応が一度もなかった症例の割合。
7)
日本脳神経外科学会のガイドライン(脳卒中合同ガイドライン委員会. 脳卒中治療ガイドライン 2009)で被
殻出血の手術適応となる血腫量は 31 cm3 以上とされていることを踏まえ、移植片が直線的に増大すると仮定
しても 20 年後に移植片が 31 cm3 を超えないよう、2 年後では 3.1 cm3 を限界点とする基準が設定された。
8
オフ時の MDS-UPDRS Part Ⅲ合計スコアについて、有効性解析対象集団の 6 例中 4 例で著効3)
と判断された。移植後 24 カ月に著効とならなかった 2 例(高用量群:症例 4、症例 5)のうち 1
例(症例 5)は、移植後 18 カ月まで改善が認められていたが、移植後 24 カ月に+3 となり悪化
した。もう 1 例(症例 4)は移植後 4 週にスコアが上昇し、以降は移植後 24 カ月まで低下した
が、ベースラインからの変化量は+5 となり悪化した。
(2) 移植細胞の生着及び機能評価
有効性解析対象集団 6 例における[18F]FDOPA の集積が本品の移植部位である被殻に定性的に
確認された。移植後 24 カ月において、被殻での Ki 値は 6 例中 5 例でベースラインから増加し
ており、また、被殻/尾状核比4)は 6 例全例でベースラインから増加した。
また、生着の判定は、IACT16049-02 試験において移植後 12 カ月及び 24 カ月時点で行われ
た。客観性を担保するため、評価時期までに得られた MRI 画像及び PET 画像([18F]FDOPA 及び
[18F]GE1805))を用いて、被殻での生着の有無を脳神経内科医及び放射線科医による合議の上
で判定された。有効性解析対象集団 6 例全例で、移植後 12 カ月及び 24 カ月のいずれの時点で
も被殻に生着ありと判定された。
(3) 累積拒絶反応抑制率(非発現率)
IACT16049-02 試験における主要評価項目とされた本品移植後 12 週及び 12 カ月の累積拒絶反
応抑制率(非発現率)6)について、いずれの時点においても累積拒絶反応抑制率(非発現率)は
100%(6/6 例)であり、有効性解析対象の 6 例全例で拒絶反応なしと判定された。
【安全性】
IACT16049-01 試験の主要評価項目は、(1)有害事象の発現頻度と程度及び(2)移植後 24 カ
月における脳内の移植片増大(3 cm3 を超える)7)の有無(MRI)とされた。主要評価項目の結果
は、以下のとおりであった。
3)
事前に治験実施計画書において、偽手術又は標準治療でのオフ時の MDS-UPDRS Part Ⅲの 1~2 年間の推移に
係る以下の報告に基づき、ベースラインから移植後 24 カ月にオフ時の MDS-UPDRS Part Ⅲ合計スコアの 5 点
以上の改善を著効、0~4 点の改善を有効と定義した。
・ドパミン神経細胞移植を検討した臨床試験(Ann Neurol. 2003; 54: 403-14、N Engl J Med 2001; 8;
344: 710-9)では変化なし又は悪化。
・DBS を検討した臨床試験(Lancet Neurol 2010; 9: 581-91)では変化なし。
4)
本品を移植していない尾状核に対する本品を移植した被殻での Ki 値の比。
5)
活性化ミクログリアに発現するとされる translocator protein に対するアンタゴニスト。神経炎症反応の
評価に使用された。
6)
本品移植後 12 週間及び 12 カ月間に拒絶反応が一度もなかった症例の割合。
7)
日本脳神経外科学会のガイドライン(脳卒中合同ガイドライン委員会. 脳卒中治療ガイドライン 2009)で被
殻出血の手術適応となる血腫量は 31 cm3 以上とされていることを踏まえ、移植片が直線的に増大すると仮定
しても 20 年後に移植片が 31 cm3 を超えないよう、2 年後では 3.1 cm3 を限界点とする基準が設定された。
8