よむ、つかう、まなぶ。
総-6-2最適使用推進ガイドライン(アムシェプリ) (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_73124.html |
| 出典情報 | 中央社会保険医療協議会 総会(第650回 5/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
用法及び用量又は使用方法は、片側あたり本品 2.4×106 個を、全身麻酔下、定位脳手術シス
テムを用いて両側被殻に単回移植することとされた。1 例目の患者は、安全性を考慮して、片側
の被殻のみに本品が移植され、移植後 6 カ月時点で、効果安全性評価委員会において安全性に
重大な問題がないことが確認された後、対側にも本品が移植された。2 例目以降の患者には両側
被殻に本品が同時移植された。また、治験の途中で用量が変更され、4 例目以降の患者には片側
あたり本品 4.2~5.4×106 個が移植された(1~3 例目が低用量群、4~7 例目が高用量群とされ
た)。
また、生体内での本品の生着を目的として、本品移植日の朝から 52 週間タクロリムスを経口
投与することとされた。タクロリムスは 1 回 0.03~0.15 mg/kg(標準用量として 0.06 mg/kg)
を 1 日 2 回投与で開始し、目標血中濃度をトラフ値で 5~10 ng/mL の範囲として用量を調節
し、52 週間の投与後は、12 週間かけて漸減することとされた。
IACT16049-01 試験には、8 例が一次登録され、このうち本品を移植する前に治験責任医師の
判断で治験を中止した 1 例を除く 7 例が二次登録された。7 例全例に本品が移植され、安全性解
析対象集団とされた。そのうち、両側同時に本品を移植された 6 例が有効性解析対象集団とさ
れた。
また、IACT16049-01 試験では、本品移植時のタクロリムスの有効性及び安全性も同時に検討
された。当該検討は IACT16049-02 試験として実施された。
【有効性】
有効性解析対象集団(低用量群 2 例、高用量群 4 例)において、副次評価項目であった抗パ
ーキンソン病薬を規定された時間休薬した practically defined off 状態(以下、「オフ時」)
での MDS-Unified Parkinson’s Disease Rating Scale(以下、「MDS-UPDRS」
) Part Ⅲ合計ス
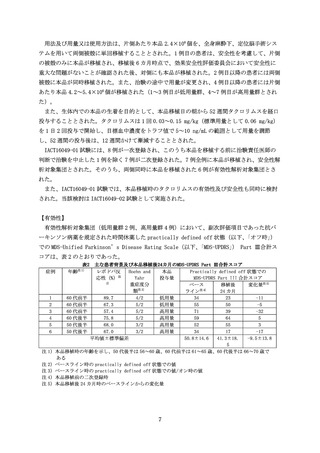
コアは、表 2 のとおりであった。
主な患者背景及び本品移植後24カ月のMDS-UPDRS Part Ⅲ合計スコア
レボドパ反
Hoehn and
本品
Practically defined off 状態での
応性(%)注
Yahr
投与量
MDS-UPDRS Part III 合計スコア
2)
重症度分
ベース
移植後
変化量注 5)
注 4)
類注 3)
ライン
24 カ月
1
60 代前半
89.7
4/2
低用量
34
23
−11
2
60 代前半
67.3
5/2
低用量
55
50
−5
3
60 代前半
57.4
5/2
高用量
71
39
−32
4
60 代後半
75.8
5/2
高用量
59
64
5
5
50 代後半
68.0
3/2
高用量
52
55
3
6
50 代後半
67.0
3/2
高用量
34
17
−17
平均値±標準偏差
50.8±14.6
41.3±18.
−9.5±13.8
5
注 1)本品移植時の年齢を示し、50 代後半は 56~60 歳、60 代前半は 61~65 歳、60 代後半は 66~70 歳で
ある
注 2)ベースライン時の practically defined off 状態での値
注 3)ベースライン時の practically defined off 状態での値/オン時の値
注 4)本品移植前の二次登録時
注 5)本品移植後 24 カ月時のベースラインからの変化量
症例
表2
年齢注 1)
7
テムを用いて両側被殻に単回移植することとされた。1 例目の患者は、安全性を考慮して、片側
の被殻のみに本品が移植され、移植後 6 カ月時点で、効果安全性評価委員会において安全性に
重大な問題がないことが確認された後、対側にも本品が移植された。2 例目以降の患者には両側
被殻に本品が同時移植された。また、治験の途中で用量が変更され、4 例目以降の患者には片側
あたり本品 4.2~5.4×106 個が移植された(1~3 例目が低用量群、4~7 例目が高用量群とされ
た)。
また、生体内での本品の生着を目的として、本品移植日の朝から 52 週間タクロリムスを経口
投与することとされた。タクロリムスは 1 回 0.03~0.15 mg/kg(標準用量として 0.06 mg/kg)
を 1 日 2 回投与で開始し、目標血中濃度をトラフ値で 5~10 ng/mL の範囲として用量を調節
し、52 週間の投与後は、12 週間かけて漸減することとされた。
IACT16049-01 試験には、8 例が一次登録され、このうち本品を移植する前に治験責任医師の
判断で治験を中止した 1 例を除く 7 例が二次登録された。7 例全例に本品が移植され、安全性解
析対象集団とされた。そのうち、両側同時に本品を移植された 6 例が有効性解析対象集団とさ
れた。
また、IACT16049-01 試験では、本品移植時のタクロリムスの有効性及び安全性も同時に検討
された。当該検討は IACT16049-02 試験として実施された。
【有効性】
有効性解析対象集団(低用量群 2 例、高用量群 4 例)において、副次評価項目であった抗パ
ーキンソン病薬を規定された時間休薬した practically defined off 状態(以下、「オフ時」)
での MDS-Unified Parkinson’s Disease Rating Scale(以下、「MDS-UPDRS」
) Part Ⅲ合計ス
コアは、表 2 のとおりであった。
主な患者背景及び本品移植後24カ月のMDS-UPDRS Part Ⅲ合計スコア
レボドパ反
Hoehn and
本品
Practically defined off 状態での
応性(%)注
Yahr
投与量
MDS-UPDRS Part III 合計スコア
2)
重症度分
ベース
移植後
変化量注 5)
注 4)
類注 3)
ライン
24 カ月
1
60 代前半
89.7
4/2
低用量
34
23
−11
2
60 代前半
67.3
5/2
低用量
55
50
−5
3
60 代前半
57.4
5/2
高用量
71
39
−32
4
60 代後半
75.8
5/2
高用量
59
64
5
5
50 代後半
68.0
3/2
高用量
52
55
3
6
50 代後半
67.0
3/2
高用量
34
17
−17
平均値±標準偏差
50.8±14.6
41.3±18.
−9.5±13.8
5
注 1)本品移植時の年齢を示し、50 代後半は 56~60 歳、60 代前半は 61~65 歳、60 代後半は 66~70 歳で
ある
注 2)ベースライン時の practically defined off 状態での値
注 3)ベースライン時の practically defined off 状態での値/オン時の値
注 4)本品移植前の二次登録時
注 5)本品移植後 24 カ月時のベースラインからの変化量
症例
表2
年齢注 1)
7