よむ、つかう、まなぶ。
総-6-2最適使用推進ガイドライン(アムシェプリ) (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_73124.html |
| 出典情報 | 中央社会保険医療協議会 総会(第650回 5/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
3.臨床成績
レボドパ含有製剤を含む既存の薬物療法で十分な効果が得られないパーキンソン病患者の運
動症状の改善について、承認時に評価を行った臨床試験の成績を示す。
3.1 第Ⅱ相試験(IACT16049-01 試験)
薬物治療のみでは症状のコントロールが困難になっているが、レボドパ製剤に対する反応性
が完全には失われていない PD 患者(目標症例数 7 例)を対象に、本品の安全性及び有効性を検
討することを目的とした非盲検非対照国内試験(IACT16049-01 試験)が、1 施設で実施され
た。主な選択・除外基準は表 1 のとおりであった。
選択基
準
除外基
準
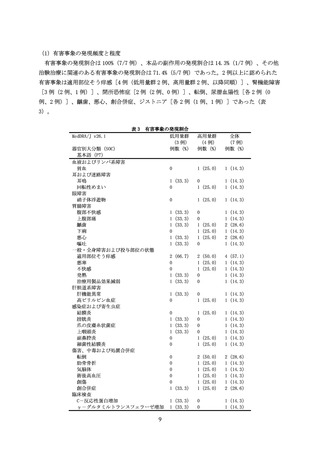
表 1 主な選択・除外基準
MDS PD の臨床診断基準(Mov Disord 2015; 30: 1591-601)に準じて、PD(臨床的確定例又
は臨床的ほぼ確実例)と診断されている
既存の薬物治療では症状のコントロールが十分に得られていない
同意取得時の年齢が 50 歳以上 70 歳未満である
PD の罹病期間が 5 年以上である
オンとオフの状態を有する(MDS-UPDRS Part Ⅲ及び症状日誌の評価より確認する)
オフ時の H&Y 重症度分類が 3 度以上である
オン時の H&Y 重症度分類が 3 度以下である
抗 PD 薬休薬時の L-dopa 反応性が 30%以上である
DAT スキャンにおいて、基底核領域で PD に特徴的な低下パターンを認める
登録前 7 日以内の臨床検査にて、以下の臓器機能を有する
好中球:2,000/μL 以上
血小板:5.0×104/μL 以上
AST、ALT:施設基準上限値の 3.0 倍以下
総ビリルビン:施設基準上限値の 1.5 倍以下
eGFR:60 mL/min/1.73 m2 以上
頭部 MRI において、症候性の器質的病変が認められる
認知症又は認知症のリスクが高いと判断される
以下のいずれかの合併症を有する
悪性新生物
てんかん
精神疾患(鬱病、双極性障害、統合失調症等)
その他、重篤な合併症(脳血管障害、心疾患、慢性呼吸器疾患、コントロール不良の
高血圧、糖尿病等)
以下のいずれかの既往を有する
悪性新生物
てんかん
脳出血
精神疾患(鬱病、双極性障害、統合失調症等)
淡蒼球手術、視床手術、脳深部刺激手術
IACT16049-01 試験における各患者の治験期間は、一次登録1)から最終観察日までとされた。
二次登録 1)からタクロリムスの投与終了日又は治験中止判定日までが治験治療期間とされ、本
品移植から 24 カ月まで2)が観察期間とされた。
1)
スクリーニングを実施し適格性が確認されたときが一次登録、再度の検査、観察及び調査を行い適格性が確認
されたときが二次登録とされた。本品は二次登録から 28 日以内に移植された。
2)
1 例目については両側移植後 24 カ月までが観察期間とされた。
6
レボドパ含有製剤を含む既存の薬物療法で十分な効果が得られないパーキンソン病患者の運
動症状の改善について、承認時に評価を行った臨床試験の成績を示す。
3.1 第Ⅱ相試験(IACT16049-01 試験)
薬物治療のみでは症状のコントロールが困難になっているが、レボドパ製剤に対する反応性
が完全には失われていない PD 患者(目標症例数 7 例)を対象に、本品の安全性及び有効性を検
討することを目的とした非盲検非対照国内試験(IACT16049-01 試験)が、1 施設で実施され
た。主な選択・除外基準は表 1 のとおりであった。
選択基
準
除外基
準
表 1 主な選択・除外基準
MDS PD の臨床診断基準(Mov Disord 2015; 30: 1591-601)に準じて、PD(臨床的確定例又
は臨床的ほぼ確実例)と診断されている
既存の薬物治療では症状のコントロールが十分に得られていない
同意取得時の年齢が 50 歳以上 70 歳未満である
PD の罹病期間が 5 年以上である
オンとオフの状態を有する(MDS-UPDRS Part Ⅲ及び症状日誌の評価より確認する)
オフ時の H&Y 重症度分類が 3 度以上である
オン時の H&Y 重症度分類が 3 度以下である
抗 PD 薬休薬時の L-dopa 反応性が 30%以上である
DAT スキャンにおいて、基底核領域で PD に特徴的な低下パターンを認める
登録前 7 日以内の臨床検査にて、以下の臓器機能を有する
好中球:2,000/μL 以上
血小板:5.0×104/μL 以上
AST、ALT:施設基準上限値の 3.0 倍以下
総ビリルビン:施設基準上限値の 1.5 倍以下
eGFR:60 mL/min/1.73 m2 以上
頭部 MRI において、症候性の器質的病変が認められる
認知症又は認知症のリスクが高いと判断される
以下のいずれかの合併症を有する
悪性新生物
てんかん
精神疾患(鬱病、双極性障害、統合失調症等)
その他、重篤な合併症(脳血管障害、心疾患、慢性呼吸器疾患、コントロール不良の
高血圧、糖尿病等)
以下のいずれかの既往を有する
悪性新生物
てんかん
脳出血
精神疾患(鬱病、双極性障害、統合失調症等)
淡蒼球手術、視床手術、脳深部刺激手術
IACT16049-01 試験における各患者の治験期間は、一次登録1)から最終観察日までとされた。
二次登録 1)からタクロリムスの投与終了日又は治験中止判定日までが治験治療期間とされ、本
品移植から 24 カ月まで2)が観察期間とされた。
1)
スクリーニングを実施し適格性が確認されたときが一次登録、再度の検査、観察及び調査を行い適格性が確認
されたときが二次登録とされた。本品は二次登録から 28 日以内に移植された。
2)
1 例目については両側移植後 24 カ月までが観察期間とされた。
6