よむ、つかう、まなぶ。
総-6-2最適使用推進ガイドライン(アムシェプリ) (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_73124.html |
| 出典情報 | 中央社会保険医療協議会 総会(第650回 5/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
2.本品の特徴、作用機序
アムシェプリ(一般名:ラグネプロセル、以下「本品」
)は非自己 iPS 細胞由来ドパミン神経前
駆細胞(以下「本細胞」
)を構成細胞(有効成分)とする再生医療等製品である。
本品は、線条体の被殻に移植された後、DA を合成・分泌する DA 神経細胞に分化・成熟する。
失われた DA 神経細胞が補充されることで、移植部位近傍の DA 量が増加する。また、補充された
DA 神経細胞により、移植されたレボドパの取込み・代謝能力が回復し DA 量が増加する。このよ
うな本品の原理・メカニズムを踏まえ、本品が DA 神経として機能することで PD 患者の運動症状
の改善が期待される。
パーキンソン病モデルラットである 6-ヒドロキシドパミン傷害免疫不全ラットの線条体に本
細胞を移植したところ、病態の指標であるメタンフェタミン誘発異常回転行動が改善した。また、
移植した細胞が脳内で生着し、DA 神経細胞に分化していることが確認された。非臨床安全性試験
として実施した一般毒性試験(観察期間 26 週間)
、造腫瘍性試験(観察期間 39 週間)
、一般毒性
及び造腫瘍性複合型試験(観察期間 52 週間)及び奇形腫形成試験(観察期間 26 週間)では、本
細胞に関連した毒性変化及び造腫瘍性は認められなかった。
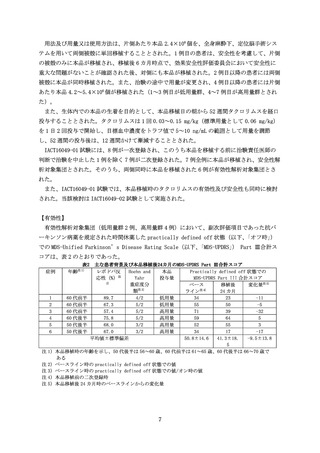
上記の知見を踏まえ、薬物治療のみでは症状のコントロールが困難になっているが、レボドパ
製剤に対する反応性が完全には失われていない PD 患者を対象に臨床試験を実施した結果、一定
の有効性が示唆され、安全性及び忍容性が確認された。ただし、現時点で得られている本品の有
効性及び安全性に関するデータは限られており、再生医療等製品の条件及び期限付承認制度に基
づいて承認が得られる段階である。本品の有効性の検証及びさらなる安全性の確認のため、製造
販売後承認条件評価として製造販売後臨床試験及び全例を対象とした使用成績調査を実施し、製
造販売後も継続して評価を行う。
5
アムシェプリ(一般名:ラグネプロセル、以下「本品」
)は非自己 iPS 細胞由来ドパミン神経前
駆細胞(以下「本細胞」
)を構成細胞(有効成分)とする再生医療等製品である。
本品は、線条体の被殻に移植された後、DA を合成・分泌する DA 神経細胞に分化・成熟する。
失われた DA 神経細胞が補充されることで、移植部位近傍の DA 量が増加する。また、補充された
DA 神経細胞により、移植されたレボドパの取込み・代謝能力が回復し DA 量が増加する。このよ
うな本品の原理・メカニズムを踏まえ、本品が DA 神経として機能することで PD 患者の運動症状
の改善が期待される。
パーキンソン病モデルラットである 6-ヒドロキシドパミン傷害免疫不全ラットの線条体に本
細胞を移植したところ、病態の指標であるメタンフェタミン誘発異常回転行動が改善した。また、
移植した細胞が脳内で生着し、DA 神経細胞に分化していることが確認された。非臨床安全性試験
として実施した一般毒性試験(観察期間 26 週間)
、造腫瘍性試験(観察期間 39 週間)
、一般毒性
及び造腫瘍性複合型試験(観察期間 52 週間)及び奇形腫形成試験(観察期間 26 週間)では、本
細胞に関連した毒性変化及び造腫瘍性は認められなかった。
上記の知見を踏まえ、薬物治療のみでは症状のコントロールが困難になっているが、レボドパ
製剤に対する反応性が完全には失われていない PD 患者を対象に臨床試験を実施した結果、一定
の有効性が示唆され、安全性及び忍容性が確認された。ただし、現時点で得られている本品の有
効性及び安全性に関するデータは限られており、再生医療等製品の条件及び期限付承認制度に基
づいて承認が得られる段階である。本品の有効性の検証及びさらなる安全性の確認のため、製造
販売後承認条件評価として製造販売後臨床試験及び全例を対象とした使用成績調査を実施し、製
造販売後も継続して評価を行う。
5