よむ、つかう、まなぶ。
総-6-2最適使用推進ガイドライン(アムシェプリ) (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_73124.html |
| 出典情報 | 中央社会保険医療協議会 総会(第650回 5/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
MedDRA/J v26.1
器官別大分類(SOC)
基本語(PT)
体重減少
尿潜血陽性
頭部磁気共鳴画像
筋骨格系および結合組織障害
関節痛
背部痛
腰部脊柱管狭窄症
筋緊張
神経系障害
ジスキネジア
ジストニア
頭痛
感覚鈍麻
精神障害
不安
閉所恐怖症
幻嗅
腎および尿路障害
緊張性膀胱
頻尿
腎機能障害
呼吸器、胸郭および縦隔障害
鼻漏
皮膚および皮下組織障害
脱毛症
湿疹
血管障害
起立性低血圧
末梢冷感
製品の問題
医療機器破損
低用量群
(3 例)
例数(%)
高用量群
(4 例)
例数(%)
全体
(7 例)
例数(%)
0
0
0
1(25.0)
2(50.0)
1(25.0)
1(14.3)
2(28.6)
1(14.3)
1(33.3)
1(33.3)
0
1(33.3)
0
0
1(25.0)
0
1(14.3)
1(14.3)
1(14.3)
1(14.3)
0
1(33.3)
1(33.3)
0
1(25.0)
1(25.0)
0
1(25.0)
1(14.3)
2(28.6)
1(14.3)
1(14.3)
0
2(66.7)
0
1(25.0)
0
1(25.0)
1(14.3)
2(28.6)
1(14.3)
0
0
2(66.7)
1(25.0)
1(25.0)
1(25.0)
1(14.3)
1(14.3)
3(42.9)
1(33.3)
0
1(14.3)
0
1(33.3)
1(25.0)
0
1(14.3)
1(14.3)
0
0
1(25.0)
1(25.0)
1(14.3)
1(14.3)
1(33.3)
0
1(14.3)
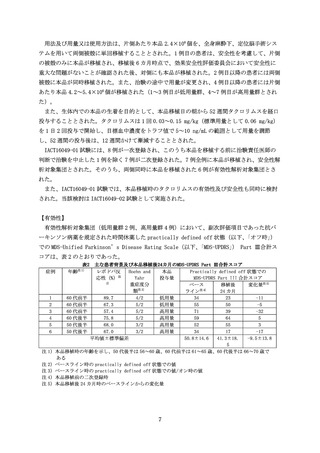
高度の有害事象は認められず、中等度のジスキネジアが 1 例(高用量群の症例 F)に発現し
た。本事象の転帰は未回復であったが、本品とは関連なしと判断された。その他の事象はいず
れも軽度であった。死亡、重篤な有害事象及び移植片摘除に至った有害事象は認められなかっ
た。
タクロリムスの副作用の発現割合は 42.9%(3/7 例)であった。2 例以上に認められた副作用
は、腎機能障害 2 例であった。その他は、肝機能異常、γ-グルタミルトランスフェラーゼ増
加、爪の皮膚糸状菌症、膀胱炎各 1 例であった。重症度はいずれも軽度で、腎機能障害及び爪
の皮膚糸状菌症の各 1 例が未回復であった以外は回復であった。死亡、重篤な有害事象及び投
与中止に至った有害事象はなかった。投与量の減量に至った有害事象は腎機能障害の 1 例で、
投与開始後 243 日に発現し、転帰は未回復であった。
(2)移植後 24 カ月における脳内の移植片増大(3 cm3 を超える)の有無(MRI)
本品移植後の移植片体積について、7 例全例で本品移植後 24 カ月に左右それぞれで 3 cm3 超え
る脳内の移植片の増大は認められなかった。
10
器官別大分類(SOC)
基本語(PT)
体重減少
尿潜血陽性
頭部磁気共鳴画像
筋骨格系および結合組織障害
関節痛
背部痛
腰部脊柱管狭窄症
筋緊張
神経系障害
ジスキネジア
ジストニア
頭痛
感覚鈍麻
精神障害
不安
閉所恐怖症
幻嗅
腎および尿路障害
緊張性膀胱
頻尿
腎機能障害
呼吸器、胸郭および縦隔障害
鼻漏
皮膚および皮下組織障害
脱毛症
湿疹
血管障害
起立性低血圧
末梢冷感
製品の問題
医療機器破損
低用量群
(3 例)
例数(%)
高用量群
(4 例)
例数(%)
全体
(7 例)
例数(%)
0
0
0
1(25.0)
2(50.0)
1(25.0)
1(14.3)
2(28.6)
1(14.3)
1(33.3)
1(33.3)
0
1(33.3)
0
0
1(25.0)
0
1(14.3)
1(14.3)
1(14.3)
1(14.3)
0
1(33.3)
1(33.3)
0
1(25.0)
1(25.0)
0
1(25.0)
1(14.3)
2(28.6)
1(14.3)
1(14.3)
0
2(66.7)
0
1(25.0)
0
1(25.0)
1(14.3)
2(28.6)
1(14.3)
0
0
2(66.7)
1(25.0)
1(25.0)
1(25.0)
1(14.3)
1(14.3)
3(42.9)
1(33.3)
0
1(14.3)
0
1(33.3)
1(25.0)
0
1(14.3)
1(14.3)
0
0
1(25.0)
1(25.0)
1(14.3)
1(14.3)
1(33.3)
0
1(14.3)
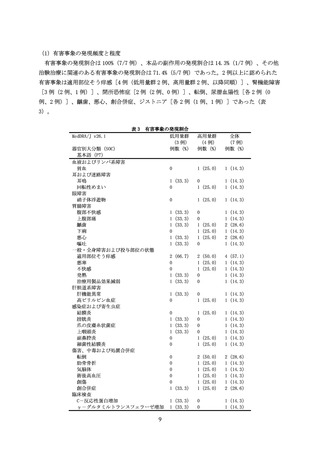
高度の有害事象は認められず、中等度のジスキネジアが 1 例(高用量群の症例 F)に発現し
た。本事象の転帰は未回復であったが、本品とは関連なしと判断された。その他の事象はいず
れも軽度であった。死亡、重篤な有害事象及び移植片摘除に至った有害事象は認められなかっ
た。
タクロリムスの副作用の発現割合は 42.9%(3/7 例)であった。2 例以上に認められた副作用
は、腎機能障害 2 例であった。その他は、肝機能異常、γ-グルタミルトランスフェラーゼ増
加、爪の皮膚糸状菌症、膀胱炎各 1 例であった。重症度はいずれも軽度で、腎機能障害及び爪
の皮膚糸状菌症の各 1 例が未回復であった以外は回復であった。死亡、重篤な有害事象及び投
与中止に至った有害事象はなかった。投与量の減量に至った有害事象は腎機能障害の 1 例で、
投与開始後 243 日に発現し、転帰は未回復であった。
(2)移植後 24 カ月における脳内の移植片増大(3 cm3 を超える)の有無(MRI)
本品移植後の移植片体積について、7 例全例で本品移植後 24 カ月に左右それぞれで 3 cm3 超え
る脳内の移植片の増大は認められなかった。
10