よむ、つかう、まなぶ。
総-7参考2 (9 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71462.html |
| 出典情報 | 中央社会保険医療協議会 総会(第648回 3/11)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
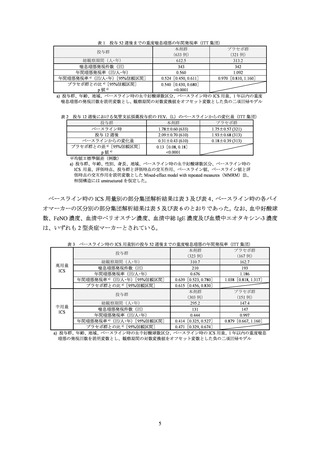
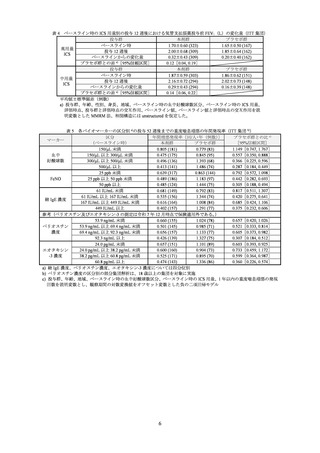
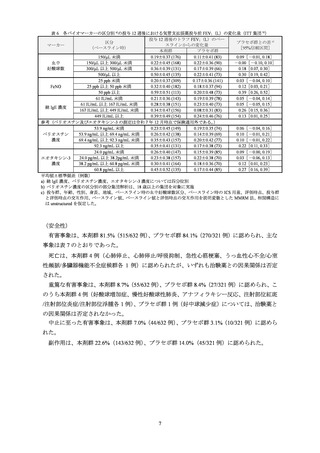
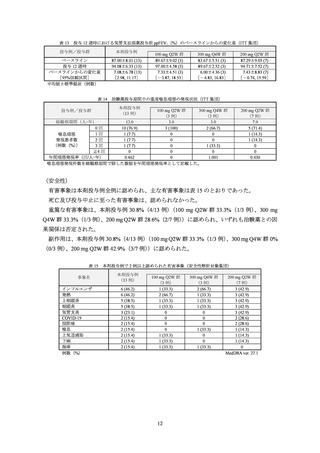
表 7 いずれかの群で 3%以上認められた有害事象(安全性解析対象集団)
本剤群
プラセボ群
事象名
(632 例)
(321 例)
ウイルス性上気道感染
111 (17.6)
64 (19.9)
注射部位紅斑
98 (15.5)
22 (6.9)
上気道感染
77 (12.2)
49 (15.3)
気管支炎
71 (11.2)
42 (13.1)
頭痛
40 (6.3)
25 (7.8)
注射部位浮腫
40 (6.3)
5 (1.6)
インフルエンザ
38 (6.0)
22 (6.9)
偶発的過量投与
33 (5.2)
16 (5.0)
注射部位そう痒感
31 (4.9)
3 (0.9)
副鼻腔炎
26 (4.1)
29 (9.0)
胃腸炎
25 (4.0)
15 (4.7)
背部痛
25 (4.0)
7 (2.2)
咽頭炎
24 (3.8)
16 (5.0)
尿路感染
19 (3.0)
12 (3.7)
関節痛
19 (3.0)
11 (3.4)
アレルギー性鼻炎
18 (2.8)
15 (4.7)
悪心
13 (2.1)
10 (3.1)
急性副鼻腔炎
10 (1.6)
15 (4.7)
例数(%)
MedDRA ver. 20.0
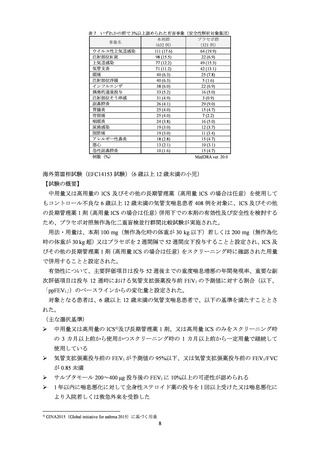
海外第Ⅲ相試験(EFC14153 試験)
(6 歳以上 12 歳未満の小児)
【試験の概要】
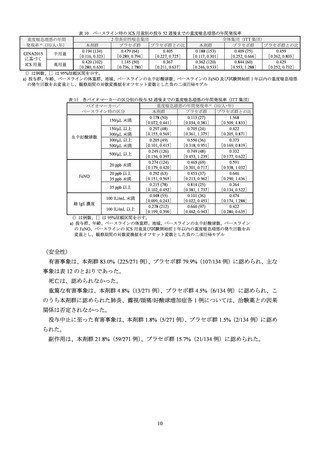
中用量又は高用量の ICS 及びその他の長期管理薬(高用量 ICS の場合は任意)を使用して
もコントロール不良な 6 歳以上 12 歳未満の気管支喘息患者 408 例を対象に、ICS 及びその他
の長期管理薬 1 剤(高用量 ICS の場合は任意)併用下での本剤の有効性及び安全性を検討する
ため、プラセボ対照無作為化二重盲検並行群間比較試験が実施された。
用法・用量は、本剤 100 mg(無作為化時の体重が 30 kg 以下)若しくは 200 mg(無作為化
時の体重が 30 kg 超)又はプラセボを 2 週間隔で 52 週間皮下投与することと設定され、ICS 及
びその他の長期管理薬 1 剤(高用量 ICS の場合は任意)をスクリーニング時に確認された用量
で併用することと設定された。
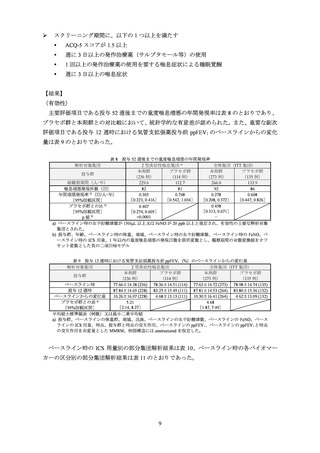
有効性について、主要評価項目は投与 52 週後までの重度喘息増悪の年間発現率、重要な副
次評価項目は投与 12 週時における気管支拡張薬投与前 FEV1 の予測値に対する割合(以下、
「ppFEV1」
)のベースラインからの変化量と設定された。
対象となる患者は、6 歳以上 12 歳未満の気管支喘息患者で、以下の基準を満たすこととさ
れた。
(主な選択基準)
➢
中用量又は高用量の ICS4)及び長期管理薬 1 剤、又は高用量 ICS のみをスクリーニング時
の 3 カ月以上前から使用かつスクリーニング時の 1 カ月以上前から一定用量で継続して
使用している
➢
気管支拡張薬投与前の FEV1 が予測値の 95%以下、又は気管支拡張薬投与前の FEV1/FVC
が 0.85 未満
➢
サルブタモール 200~400 μg 投与後の FEV1 に 10%以上の可逆性が認められる
➢
1 年以内に喘息悪化に対して全身性ステロイド薬の投与を 1 回以上受けた又は喘息悪化に
より入院若しくは救急外来を受診した
4)
GINA2015(Global initiative for asthma 2015)に基づく用量
8
本剤群
プラセボ群
事象名
(632 例)
(321 例)
ウイルス性上気道感染
111 (17.6)
64 (19.9)
注射部位紅斑
98 (15.5)
22 (6.9)
上気道感染
77 (12.2)
49 (15.3)
気管支炎
71 (11.2)
42 (13.1)
頭痛
40 (6.3)
25 (7.8)
注射部位浮腫
40 (6.3)
5 (1.6)
インフルエンザ
38 (6.0)
22 (6.9)
偶発的過量投与
33 (5.2)
16 (5.0)
注射部位そう痒感
31 (4.9)
3 (0.9)
副鼻腔炎
26 (4.1)
29 (9.0)
胃腸炎
25 (4.0)
15 (4.7)
背部痛
25 (4.0)
7 (2.2)
咽頭炎
24 (3.8)
16 (5.0)
尿路感染
19 (3.0)
12 (3.7)
関節痛
19 (3.0)
11 (3.4)
アレルギー性鼻炎
18 (2.8)
15 (4.7)
悪心
13 (2.1)
10 (3.1)
急性副鼻腔炎
10 (1.6)
15 (4.7)
例数(%)
MedDRA ver. 20.0
海外第Ⅲ相試験(EFC14153 試験)
(6 歳以上 12 歳未満の小児)
【試験の概要】
中用量又は高用量の ICS 及びその他の長期管理薬(高用量 ICS の場合は任意)を使用して
もコントロール不良な 6 歳以上 12 歳未満の気管支喘息患者 408 例を対象に、ICS 及びその他
の長期管理薬 1 剤(高用量 ICS の場合は任意)併用下での本剤の有効性及び安全性を検討する
ため、プラセボ対照無作為化二重盲検並行群間比較試験が実施された。
用法・用量は、本剤 100 mg(無作為化時の体重が 30 kg 以下)若しくは 200 mg(無作為化
時の体重が 30 kg 超)又はプラセボを 2 週間隔で 52 週間皮下投与することと設定され、ICS 及
びその他の長期管理薬 1 剤(高用量 ICS の場合は任意)をスクリーニング時に確認された用量
で併用することと設定された。
有効性について、主要評価項目は投与 52 週後までの重度喘息増悪の年間発現率、重要な副
次評価項目は投与 12 週時における気管支拡張薬投与前 FEV1 の予測値に対する割合(以下、
「ppFEV1」
)のベースラインからの変化量と設定された。
対象となる患者は、6 歳以上 12 歳未満の気管支喘息患者で、以下の基準を満たすこととさ
れた。
(主な選択基準)
➢
中用量又は高用量の ICS4)及び長期管理薬 1 剤、又は高用量 ICS のみをスクリーニング時
の 3 カ月以上前から使用かつスクリーニング時の 1 カ月以上前から一定用量で継続して
使用している
➢
気管支拡張薬投与前の FEV1 が予測値の 95%以下、又は気管支拡張薬投与前の FEV1/FVC
が 0.85 未満
➢
サルブタモール 200~400 μg 投与後の FEV1 に 10%以上の可逆性が認められる
➢
1 年以内に喘息悪化に対して全身性ステロイド薬の投与を 1 回以上受けた又は喘息悪化に
より入院若しくは救急外来を受診した
4)
GINA2015(Global initiative for asthma 2015)に基づく用量
8