よむ、つかう、まなぶ。
総-7参考2 (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71462.html |
| 出典情報 | 中央社会保険医療協議会 総会(第648回 3/11)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
➢
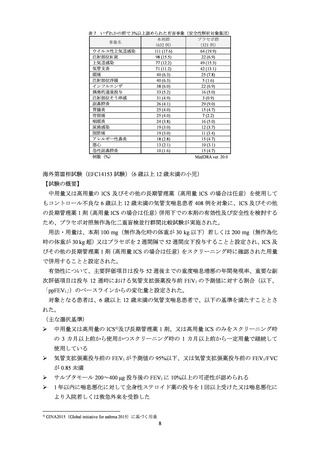
スクリーニング期間に、以下の 1 つ以上を満たす
ACQ-5 スコアが 1.5 以上
週に 3 日以上の発作治療薬(サルブタモール等)の使用
1 回以上の発作治療薬の使用を要する喘息症状による睡眠覚醒
週に 3 日以上の喘息症状
【結果】
(有効性)
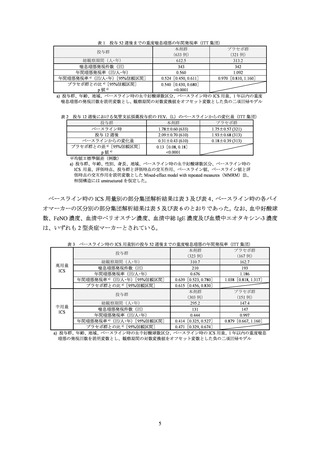
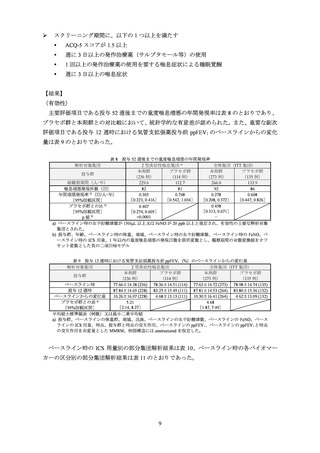
主要評価項目である投与 52 週後までの重度喘息増悪の年間発現率は表 8 のとおりであり、
プラセボ群と本剤群との対比較において、統計学的な有意差が認められた。また、重要な副次
評価項目である投与 12 週時における気管支拡張薬投与前 ppFEV1 のベースラインからの変化
量は表 9 のとおりであった。
表 8 投与 52 週後までの重度喘息増悪の年間発現率
2 型炎症性喘息集団 a)
全体集団(ITT 集団)
本剤群
プラセボ群
本剤群
プラセボ群
投与群
(236 例)
(114 例)
(273 例)
(135 例)
総観察期間(人・年)
229.6
112.7
266.0
133.9
喘息増悪発現件数(回)
82
81
92
86
年間増悪発現率 b)(回/人・年)
0.305
0.748
0.278
0.608
[0.223, 0.416] [0.542, 1.034] [0.208, 0.372] [0.447, 0.826]
[95%信頼区間]
プラセボ群との比 b)
0.458
0.407
[0.313, 0.671]
[95%信頼区間]
[0.274, 0.605]
<0.0001
-
p 値 b)
a) ベースライン時の血中好酸球数が 150/μL 以上又は FeNO が 20 ppb 以上と規定され、有効性の主要な解析対象
集団とされた。
b) 投与群、年齢、ベースライン時の体重、地域、ベースライン時の血中好酸球数、ベースライン時の FeNO、ベ
ースライン時の ICS 用量、1 年以内の重度喘息増悪の発現回数を説明変数とし、観察期間の対数変換値をオフ
セット変数とした負の二項回帰モデル
解析対象集団
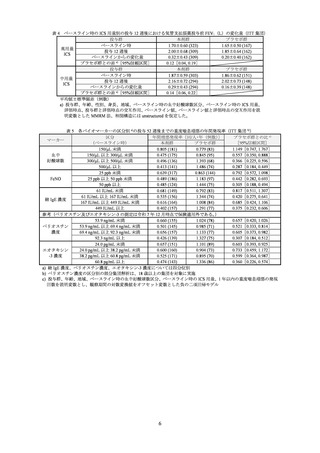
表 9 投与 12 週時における気管支拡張薬投与前 ppFEV1(%)のベースラインからの変化量
解析対象集団
2 型炎症性喘息集団
全体集団(ITT 集団)
本剤群
プラセボ群
本剤群
プラセボ群
投与群
(236 例)
(114 例)
(273 例)
(135 例)
ベースライン時
77.66±14.38 (236) 78.36±14.51 (114) 77.63±14.72 (273) 78.98±14.74 (135)
投与 12 週時
87.84±14.65 (228) 83.25±15.49 (111) 87.81±14.53 (264) 83.80±15.36 (132)
ベースラインからの変化量
10.26±16.07 (228)
4.68±13.13 (111) 10.30±16.41 (264)
4.62±13.09 (132)
プラセボ群との差 a)
5.21
4.68
[2.14, 8.27]
[1.87, 7.49]
[95%信頼区間]
平均値±標準偏差(例数)又は最小二乗平均値
a) 投与群、ベースラインの体重群、地域、民族、ベースラインの血中好酸球数、ベースラインの FeNO、ベース
ラインの ICS 用量、時点、投与群と時点の交互作用、ベースラインの ppFEV1、ベースラインの ppFEV1 と時点
の交互作用を共変量とした MMRM、相関構造には unstructured を仮定した。
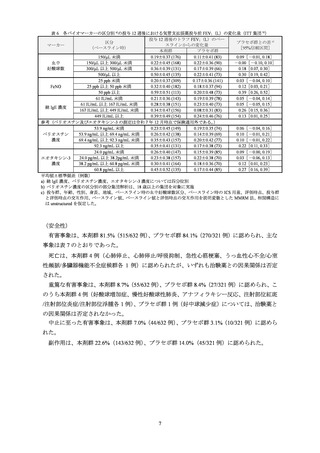
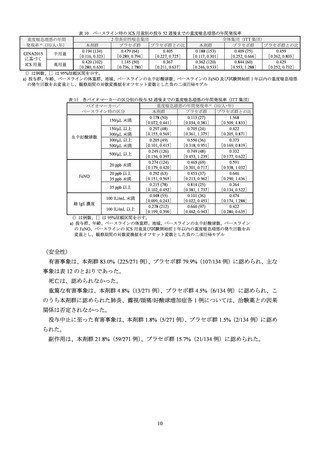
ベースライン時の ICS 用量別の部分集団解析結果は表 10、ベースライン時の各バイオマー
カーの区分別の部分集団解析結果は表 11 のとおりであった。
9
スクリーニング期間に、以下の 1 つ以上を満たす
ACQ-5 スコアが 1.5 以上
週に 3 日以上の発作治療薬(サルブタモール等)の使用
1 回以上の発作治療薬の使用を要する喘息症状による睡眠覚醒
週に 3 日以上の喘息症状
【結果】
(有効性)
主要評価項目である投与 52 週後までの重度喘息増悪の年間発現率は表 8 のとおりであり、
プラセボ群と本剤群との対比較において、統計学的な有意差が認められた。また、重要な副次
評価項目である投与 12 週時における気管支拡張薬投与前 ppFEV1 のベースラインからの変化
量は表 9 のとおりであった。
表 8 投与 52 週後までの重度喘息増悪の年間発現率
2 型炎症性喘息集団 a)
全体集団(ITT 集団)
本剤群
プラセボ群
本剤群
プラセボ群
投与群
(236 例)
(114 例)
(273 例)
(135 例)
総観察期間(人・年)
229.6
112.7
266.0
133.9
喘息増悪発現件数(回)
82
81
92
86
年間増悪発現率 b)(回/人・年)
0.305
0.748
0.278
0.608
[0.223, 0.416] [0.542, 1.034] [0.208, 0.372] [0.447, 0.826]
[95%信頼区間]
プラセボ群との比 b)
0.458
0.407
[0.313, 0.671]
[95%信頼区間]
[0.274, 0.605]
<0.0001
-
p 値 b)
a) ベースライン時の血中好酸球数が 150/μL 以上又は FeNO が 20 ppb 以上と規定され、有効性の主要な解析対象
集団とされた。
b) 投与群、年齢、ベースライン時の体重、地域、ベースライン時の血中好酸球数、ベースライン時の FeNO、ベ
ースライン時の ICS 用量、1 年以内の重度喘息増悪の発現回数を説明変数とし、観察期間の対数変換値をオフ
セット変数とした負の二項回帰モデル
解析対象集団
表 9 投与 12 週時における気管支拡張薬投与前 ppFEV1(%)のベースラインからの変化量
解析対象集団
2 型炎症性喘息集団
全体集団(ITT 集団)
本剤群
プラセボ群
本剤群
プラセボ群
投与群
(236 例)
(114 例)
(273 例)
(135 例)
ベースライン時
77.66±14.38 (236) 78.36±14.51 (114) 77.63±14.72 (273) 78.98±14.74 (135)
投与 12 週時
87.84±14.65 (228) 83.25±15.49 (111) 87.81±14.53 (264) 83.80±15.36 (132)
ベースラインからの変化量
10.26±16.07 (228)
4.68±13.13 (111) 10.30±16.41 (264)
4.62±13.09 (132)
プラセボ群との差 a)
5.21
4.68
[2.14, 8.27]
[1.87, 7.49]
[95%信頼区間]
平均値±標準偏差(例数)又は最小二乗平均値
a) 投与群、ベースラインの体重群、地域、民族、ベースラインの血中好酸球数、ベースラインの FeNO、ベース
ラインの ICS 用量、時点、投与群と時点の交互作用、ベースラインの ppFEV1、ベースラインの ppFEV1 と時点
の交互作用を共変量とした MMRM、相関構造には unstructured を仮定した。
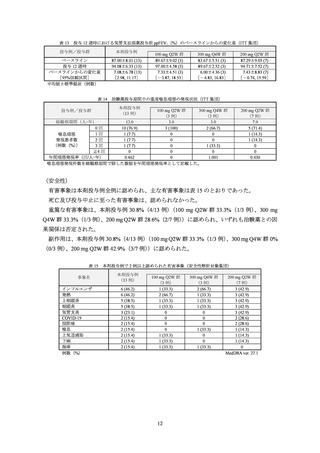
ベースライン時の ICS 用量別の部分集団解析結果は表 10、ベースライン時の各バイオマー
カーの区分別の部分集団解析結果は表 11 のとおりであった。
9