よむ、つかう、まなぶ。
総-7参考2 (8 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71462.html |
| 出典情報 | 中央社会保険医療協議会 総会(第648回 3/11)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
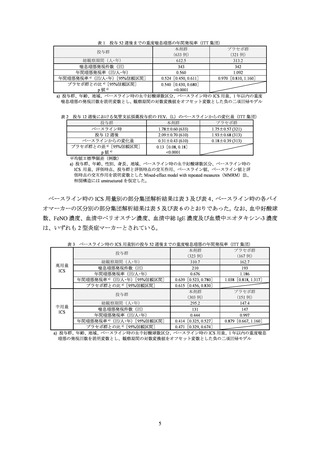
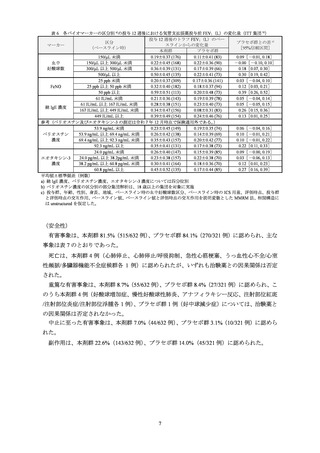
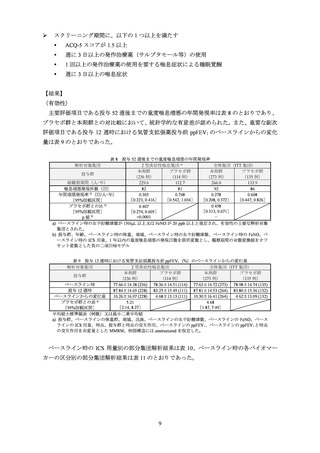
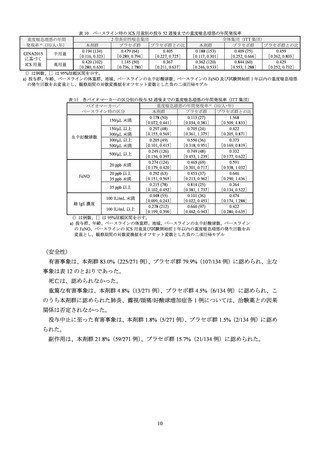
表 6 各バイオマーカーの区分別 a)の投与 12 週後における気管支拡張薬投与前 FEV1(L)の変化量(ITT 集団 b))
投与 12 週後のトラフ FEV1(L)のベー
区分
プラセボ群との差 c)
スラインからの変化量
マーカー
(ベースライン時)
[95%信頼区間]
本剤群
プラセボ群
150/μL 未満
0.19±0.37 (176)
0.11±0.41 (83)
0.09[-0.01, 0.18]
150/μL 以上 300/μL 未満
0.22±0.45 (168)
0.22±0.36 (90)
-0.00[-0.10, 0.10]
血中
好酸球数
300/μL 以上 500/μL 未満
0.36±0.39 (131)
0.17±0.39 (66)
0.18[0.07, 0.30]
500/μL 以上
0.50±0.45 (135)
0.22±0.41 (73)
0.30[0.19, 0.42]
25 ppb 未満
0.20±0.37 (309)
0.17±0.36 (141)
0.03[-0.04, 0.10]
25 ppb 以上 50 ppb 未満
0.32±0.40 (182)
0.18±0.37 (94)
0.12[0.03, 0.21]
FeNO
50 ppb 以上
0.59±0.51 (113)
0.20±0.48 (73)
0.39[0.26, 0.52]
61 IU/mL 未満
0.21±0.36 (143)
0.19±0.39 (78)
0.05[-0.04, 0.14]
61 IU/mL 以上 167 IU/mL 未満
0.28±0.38 (151)
0.23±0.40 (73)
0.05[-0.05, 0.15]
総 IgE 濃度
167 IU/mL 以上 449 IU/mL 未満
0.34±0.47 (156)
0.08±0.31 (83)
0.26[0.15, 0.36]
449 IU/mL 以上
0.39±0.49 (154)
0.24±0.46 (76)
0.13[0.01, 0.25]
参考(ペリオスチン及びエオタキシン-3 の測定は令和 7 年 12 月時点で保険適用外である。)
53.9 ng/mL 未満
0.23±0.45 (149)
0.19±0.35 (74)
0.06[-0.04, 0.16]
53.9 ng/mL 以上 69.4 ng/mL 未満
0.26±0.42 (138)
0.14±0.39 (69)
0.10[-0.01, 0.21]
ペリオスチン
濃度
69.4 ng/mL 以上 92.3 ng/mL 未満
0.35±0.43 (157)
0.20±0.42 (77)
0.10[-0.01, 0.22]
92.3 ng/mL 以上
0.35±0.41 (131)
0.17±0.38 (73)
0.22[0.11, 0.33]
24.0 pg/mL 未満
0.26±0.40 (147)
0.15±0.39 (85)
0.09[-0.00, 0.19]
24.0 pg/mL 以上 38.2pg/mL 未満
0.23±0.38 (157)
0.22±0.38 (70)
0.03[-0.06, 0.13]
エオタキシン-3
濃度
38.2 pg/mL 以上 60.8 pg/mL 未満
0.30±0.41 (164)
0.18±0.36 (70)
0.12[0.01, 0.23]
60.8 pg/mL 以上
0.45±0.52 (135)
0.17±0.44 (85)
0.27[0.16, 0.39]
平均値±標準偏差(例数)
a) 総 IgE 濃度、ペリオスチン濃度、エオタキシン-3 濃度については四分位別
b) ペリオスチン濃度の区分別の部分集団解析は、18 歳以上の集団を対象に実施
c) 投与群、年齢、性別、身長、地域、ベースライン時の血中好酸球数区分、ベースライン時の ICS 用量、評価時点、投与群
と評価時点の交互作用、ベースライン値、ベースライン値と評価時点の交互作用を説明変数とした MMRM 法、相関構造に
は unstructured を仮定した。
(安全性)
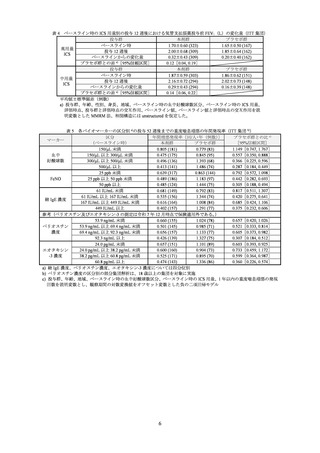
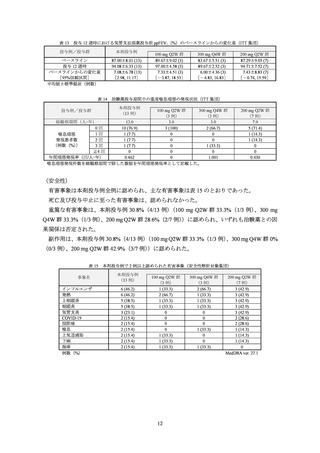
有害事象は、本剤群 81.5%(515/632 例)
、プラセボ群 84.1%(270/321 例)に認められ、主な
事象は表 7 のとおりであった。
死亡は、本剤群 4 例(心肺停止、心肺停止/呼吸抑制、急性心筋梗塞、うっ血性心不全/心室
性頻脈/多臓器機能不全症候群各 1 例)に認められたが、いずれも治験薬との因果関係は否定
された。
重篤な有害事象は、本剤群 8.7%(55/632 例)
、プラセボ群 8.4%(27/321 例)に認められ、こ
のうち本剤群 4 例(好酸球増加症、慢性好酸球性肺炎、アナフィラキシー反応、注射部位紅斑
/注射部位炎症/注射部位浮腫各 1 例)
、プラセボ群 1 例(好中球減少症)については、治験薬と
の因果関係は否定されなかった。
中止に至った有害事象は、本剤群 7.0%(44/632 例)
、プラセボ群 3.1%(10/321 例)に認めら
れた。
副作用は、本剤群 22.6%(143/632 例)、プラセボ群 14.0%(45/321 例)に認められた。
7
投与 12 週後のトラフ FEV1(L)のベー
区分
プラセボ群との差 c)
スラインからの変化量
マーカー
(ベースライン時)
[95%信頼区間]
本剤群
プラセボ群
150/μL 未満
0.19±0.37 (176)
0.11±0.41 (83)
0.09[-0.01, 0.18]
150/μL 以上 300/μL 未満
0.22±0.45 (168)
0.22±0.36 (90)
-0.00[-0.10, 0.10]
血中
好酸球数
300/μL 以上 500/μL 未満
0.36±0.39 (131)
0.17±0.39 (66)
0.18[0.07, 0.30]
500/μL 以上
0.50±0.45 (135)
0.22±0.41 (73)
0.30[0.19, 0.42]
25 ppb 未満
0.20±0.37 (309)
0.17±0.36 (141)
0.03[-0.04, 0.10]
25 ppb 以上 50 ppb 未満
0.32±0.40 (182)
0.18±0.37 (94)
0.12[0.03, 0.21]
FeNO
50 ppb 以上
0.59±0.51 (113)
0.20±0.48 (73)
0.39[0.26, 0.52]
61 IU/mL 未満
0.21±0.36 (143)
0.19±0.39 (78)
0.05[-0.04, 0.14]
61 IU/mL 以上 167 IU/mL 未満
0.28±0.38 (151)
0.23±0.40 (73)
0.05[-0.05, 0.15]
総 IgE 濃度
167 IU/mL 以上 449 IU/mL 未満
0.34±0.47 (156)
0.08±0.31 (83)
0.26[0.15, 0.36]
449 IU/mL 以上
0.39±0.49 (154)
0.24±0.46 (76)
0.13[0.01, 0.25]
参考(ペリオスチン及びエオタキシン-3 の測定は令和 7 年 12 月時点で保険適用外である。)
53.9 ng/mL 未満
0.23±0.45 (149)
0.19±0.35 (74)
0.06[-0.04, 0.16]
53.9 ng/mL 以上 69.4 ng/mL 未満
0.26±0.42 (138)
0.14±0.39 (69)
0.10[-0.01, 0.21]
ペリオスチン
濃度
69.4 ng/mL 以上 92.3 ng/mL 未満
0.35±0.43 (157)
0.20±0.42 (77)
0.10[-0.01, 0.22]
92.3 ng/mL 以上
0.35±0.41 (131)
0.17±0.38 (73)
0.22[0.11, 0.33]
24.0 pg/mL 未満
0.26±0.40 (147)
0.15±0.39 (85)
0.09[-0.00, 0.19]
24.0 pg/mL 以上 38.2pg/mL 未満
0.23±0.38 (157)
0.22±0.38 (70)
0.03[-0.06, 0.13]
エオタキシン-3
濃度
38.2 pg/mL 以上 60.8 pg/mL 未満
0.30±0.41 (164)
0.18±0.36 (70)
0.12[0.01, 0.23]
60.8 pg/mL 以上
0.45±0.52 (135)
0.17±0.44 (85)
0.27[0.16, 0.39]
平均値±標準偏差(例数)
a) 総 IgE 濃度、ペリオスチン濃度、エオタキシン-3 濃度については四分位別
b) ペリオスチン濃度の区分別の部分集団解析は、18 歳以上の集団を対象に実施
c) 投与群、年齢、性別、身長、地域、ベースライン時の血中好酸球数区分、ベースライン時の ICS 用量、評価時点、投与群
と評価時点の交互作用、ベースライン値、ベースライン値と評価時点の交互作用を説明変数とした MMRM 法、相関構造に
は unstructured を仮定した。
(安全性)
有害事象は、本剤群 81.5%(515/632 例)
、プラセボ群 84.1%(270/321 例)に認められ、主な
事象は表 7 のとおりであった。
死亡は、本剤群 4 例(心肺停止、心肺停止/呼吸抑制、急性心筋梗塞、うっ血性心不全/心室
性頻脈/多臓器機能不全症候群各 1 例)に認められたが、いずれも治験薬との因果関係は否定
された。
重篤な有害事象は、本剤群 8.7%(55/632 例)
、プラセボ群 8.4%(27/321 例)に認められ、こ
のうち本剤群 4 例(好酸球増加症、慢性好酸球性肺炎、アナフィラキシー反応、注射部位紅斑
/注射部位炎症/注射部位浮腫各 1 例)
、プラセボ群 1 例(好中球減少症)については、治験薬と
の因果関係は否定されなかった。
中止に至った有害事象は、本剤群 7.0%(44/632 例)
、プラセボ群 3.1%(10/321 例)に認めら
れた。
副作用は、本剤群 22.6%(143/632 例)、プラセボ群 14.0%(45/321 例)に認められた。
7