よむ、つかう、まなぶ。
総-7参考2 (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71462.html |
| 出典情報 | 中央社会保険医療協議会 総会(第648回 3/11)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
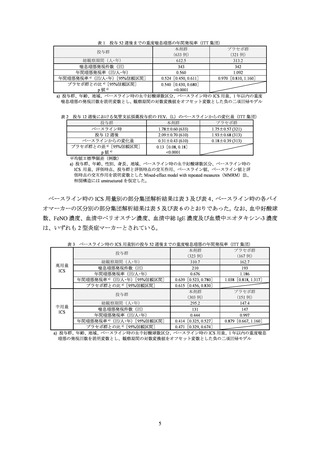
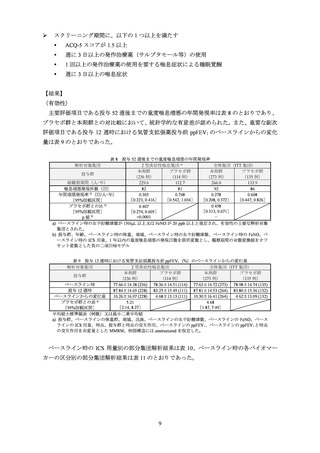
表 10 ベースライン時の ICS 用量別の投与 52 週後までの重度喘息増悪の年間発現率
2 型炎症性喘息集団
全体集団(ITT 集団)
本剤群
プラセボ群
プラセボ群との比
本剤群
プラセボ群
プラセボ群との比
0.194 (134)
0.479 (64)
0.405
0.188 (153)
0.409 (75)
0.459
GINA2015
中用量
[0.116, 0.323]
[0.289, 0.794]
[0.227, 0.725]
[0.117, 0.301]
[0.252, 0.666]
[0.262, 0.803]
に基づく
0.420 (102)
1.145 (50)
0.367
0.362 (120)
0.844 (60)
0.429
ICS 用量
高用量
[0.280, 0.630]
[0.736, 1.780]
[0.211, 0.637]
[0.246, 0.533]
[0.553, 1.288]
[0.252, 0.732]
()は例数、
[]は 95%信頼区間を示す。
a) 投与群、年齢、ベースラインの体重群、地域、ベースラインの血中好酸球数、ベースラインの FeNO 及び試験開始前 1 年以内の重度喘息増悪
の発生回数を共変量とし、観察期間の対数変換値をオフセット変数とした負の二項回帰モデル
重度喘息増悪の年間
発現率 a)(回/人・年)
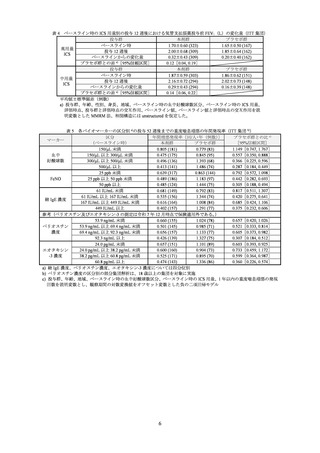
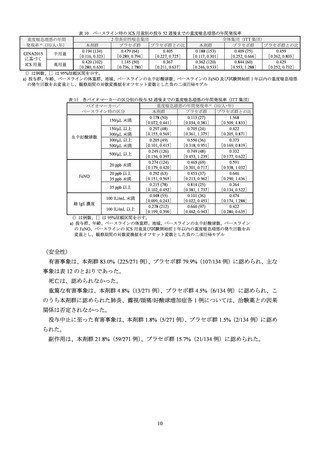
表 11 各バイオマーカーの区分別の投与 52 週後までの重度喘息増悪の年間発現率(ITT 集団)
重度喘息増悪の年間発現率 a)(回/人・年)
バイオマーカー/
ベースライン時の区分
本剤群
プラセボ群
プラセボ群との比
0.178 (50)
0.113 (27)
1.568
150/µL 未満
[0.072, 0.441]
[0.034, 0.381]
[0.509, 4.833]
150/µL 以上
0.297 (48)
0.705 (24)
0.422
[0.155, 0.569]
[0.361, 1.375]
[0.205, 0.871]
300/µL 未満
血中好酸球数
300/µL 以上
0.205 (49)
0.550 (36)
0.373
[0.101, 0.415]
[0.318, 0.951]
[0.169, 0.819]
500/µL 未満
0.249 (126)
0.749 (48)
0.332
500/µL 以上
[0.156, 0.397]
[0.453, 1.239]
[0.177, 0.622]
0.274 (124)
0.465 (69)
0.591
20 ppb 未満
[0.179, 0.420]
[0.301, 0.717]
[0.338, 1.032]
20 ppb 以上
0.292 (63)
0.453 (37)
0.646
FeNO
[0.151, 0.565]
[0.213, 0.962]
[0.290, 1.436]
35 ppb 未満
0.215 (78)
0.814 (25)
0.264
35 ppb 以上
[0.102, 0.452]
[0.381, 1.737]
[0.134, 0.522]
0.048 (55)
0.101 (36)
0.474
100 IU/mL 未満
[0.009, 0.243]
[0.022, 0.453]
[0.174, 1.288]
総 IgE 濃度
0.278 (212)
0.660 (97)
0.422
100 IU/mL 以上
[0.199, 0.390]
[0.462, 0.943]
[0.280, 0.635]
()は例数、
[]は 95%信頼区間を示す。
a) 投与群、年齢、ベースラインの体重群、地域、ベースラインの血中好酸球数、ベースライン
の FeNO、ベースラインの ICS 用量及び試験開始前 1 年以内の重度喘息増悪の発生回数を共
変量とし、観察期間の対数変換値をオフセット変数とした負の二項回帰モデル
(安全性)
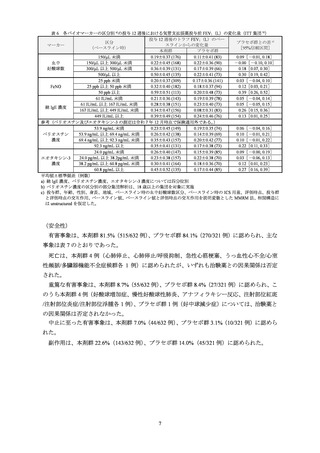
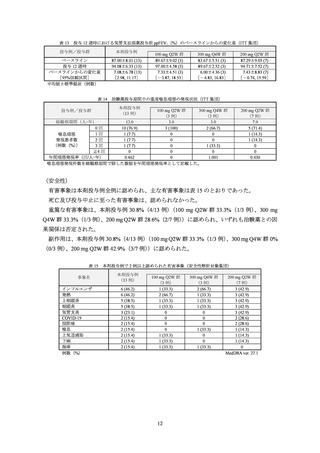
有害事象は、本剤群 83.0%(225/271 例)
、プラセボ群 79.9%(107/134 例)に認められ、主な
事象は表 12 のとおりであった。
死亡は、認められなかった。
重篤な有害事象は、本剤群 4.8%(13/271 例)、プラセボ群 4.5%(6/134 例)に認められ、こ
のうち本剤群に認められた肺炎、霧視/頭痛/好酸球増加症各 1 例については、治験薬との因果
関係は否定されなかった。
投与中止に至った有害事象は、本剤群 1.8%(5/271 例)
、プラセボ群 1.5%(2/134 例)に認め
られた。
副作用は、本剤群 21.8%(59/271 例)
、プラセボ群 15.7%(21/134 例)に認められた。
10
2 型炎症性喘息集団
全体集団(ITT 集団)
本剤群
プラセボ群
プラセボ群との比
本剤群
プラセボ群
プラセボ群との比
0.194 (134)
0.479 (64)
0.405
0.188 (153)
0.409 (75)
0.459
GINA2015
中用量
[0.116, 0.323]
[0.289, 0.794]
[0.227, 0.725]
[0.117, 0.301]
[0.252, 0.666]
[0.262, 0.803]
に基づく
0.420 (102)
1.145 (50)
0.367
0.362 (120)
0.844 (60)
0.429
ICS 用量
高用量
[0.280, 0.630]
[0.736, 1.780]
[0.211, 0.637]
[0.246, 0.533]
[0.553, 1.288]
[0.252, 0.732]
()は例数、
[]は 95%信頼区間を示す。
a) 投与群、年齢、ベースラインの体重群、地域、ベースラインの血中好酸球数、ベースラインの FeNO 及び試験開始前 1 年以内の重度喘息増悪
の発生回数を共変量とし、観察期間の対数変換値をオフセット変数とした負の二項回帰モデル
重度喘息増悪の年間
発現率 a)(回/人・年)
表 11 各バイオマーカーの区分別の投与 52 週後までの重度喘息増悪の年間発現率(ITT 集団)
重度喘息増悪の年間発現率 a)(回/人・年)
バイオマーカー/
ベースライン時の区分
本剤群
プラセボ群
プラセボ群との比
0.178 (50)
0.113 (27)
1.568
150/µL 未満
[0.072, 0.441]
[0.034, 0.381]
[0.509, 4.833]
150/µL 以上
0.297 (48)
0.705 (24)
0.422
[0.155, 0.569]
[0.361, 1.375]
[0.205, 0.871]
300/µL 未満
血中好酸球数
300/µL 以上
0.205 (49)
0.550 (36)
0.373
[0.101, 0.415]
[0.318, 0.951]
[0.169, 0.819]
500/µL 未満
0.249 (126)
0.749 (48)
0.332
500/µL 以上
[0.156, 0.397]
[0.453, 1.239]
[0.177, 0.622]
0.274 (124)
0.465 (69)
0.591
20 ppb 未満
[0.179, 0.420]
[0.301, 0.717]
[0.338, 1.032]
20 ppb 以上
0.292 (63)
0.453 (37)
0.646
FeNO
[0.151, 0.565]
[0.213, 0.962]
[0.290, 1.436]
35 ppb 未満
0.215 (78)
0.814 (25)
0.264
35 ppb 以上
[0.102, 0.452]
[0.381, 1.737]
[0.134, 0.522]
0.048 (55)
0.101 (36)
0.474
100 IU/mL 未満
[0.009, 0.243]
[0.022, 0.453]
[0.174, 1.288]
総 IgE 濃度
0.278 (212)
0.660 (97)
0.422
100 IU/mL 以上
[0.199, 0.390]
[0.462, 0.943]
[0.280, 0.635]
()は例数、
[]は 95%信頼区間を示す。
a) 投与群、年齢、ベースラインの体重群、地域、ベースラインの血中好酸球数、ベースライン
の FeNO、ベースラインの ICS 用量及び試験開始前 1 年以内の重度喘息増悪の発生回数を共
変量とし、観察期間の対数変換値をオフセット変数とした負の二項回帰モデル
(安全性)
有害事象は、本剤群 83.0%(225/271 例)
、プラセボ群 79.9%(107/134 例)に認められ、主な
事象は表 12 のとおりであった。
死亡は、認められなかった。
重篤な有害事象は、本剤群 4.8%(13/271 例)、プラセボ群 4.5%(6/134 例)に認められ、こ
のうち本剤群に認められた肺炎、霧視/頭痛/好酸球増加症各 1 例については、治験薬との因果
関係は否定されなかった。
投与中止に至った有害事象は、本剤群 1.8%(5/271 例)
、プラセボ群 1.5%(2/134 例)に認め
られた。
副作用は、本剤群 21.8%(59/271 例)
、プラセボ群 15.7%(21/134 例)に認められた。
10