よむ、つかう、まなぶ。
【資料1-1】成分情報等 (17 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_70651.html |
| 出典情報 | 医療用から要指導・一般用への転用に関する評価検討会議(第35回 2/20)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
*19. 有効成分に関する理化学的知見
8)Rosenborg J, et al. Drug Metab Dispos. 1999;27:1104-16
9)社内資料:ホルモテロールのシトクロムP450阻害作用の検討
(843-RD0395)
(2009年10月16日承認、
CTD2.7.2.2)
10)
社内資料:シムビコートと各単剤の血漿中濃度の比較(SD-039-0259)
(2009年10月16日承認、
CTD2.7.1.2)
11)
Seidegård J. Clin Pharmacol Ther. 2000;68:13-7
12)
Raaska K, et al. Clin Pharmacol Ther. 2002;72:362-9
13)
大田 健 他:アレルギー・免疫, 2010;17(4):624-38
14)
足立 満:アレルギー・免疫, 2010;17(2):266-82
15)
Atienza T, et al. Respirology. 2013;18(2):354-63
16)
Rabe KF, et al. Lancet. 2006;368:744-53
17)
Kuna P, et al. Int J Clin Pract. 2007;61:725-36
18)
Bousquet J, et al. Respir Med. 2007;101:2437-46
19)
社内資料:シムビコートの慢性閉塞性肺疾患患者における国際共同第III相
比較試験
(2012年8月10日承認、
CTD2.7.3.3)
20)
社内資料:シムビコートの日本人慢性閉塞性肺疾患患者における第III相長
期投与試験
(2012年8月10日承認、
CTD2.7.3.3)
21)
Calverley PM, et al. Eur Respir J. 2003;22:912-9
22)
Szafranski W, et al. Eur Respir J. 2003;21:74-81
23)
Brattsand R, et al. Clin Ther. 2003;25(Suppl C):C28
24)
Edsbäcker S, et al. Annals of Allergy Asthma & Immunology.
2002;88(6):609-16
25)
Ullman A, et al. Allergy. 1992;47:384-7
26)
Barnes PJ. Eur Respir J. 2002;19:182-91
27)
Roth M, et al. The Lancet. 2002;360:1293-9
28)
Linden M, et al. Pulm Pharmacol. 1994;7:43-7
29)
Woolley MJ, et al. J Appl Physiol. 1994;77:1303-8
30)
社内資料:呼吸困難症SD系ラットにおける卵白アルブミン誘発気道/肺過
敏反応及び炎症細胞に対する作用, 1995
31)
Svensjö E, et al. Prog Resp Res. 1985;19:173-80
32)
Brattsand R, et al. Amsterdam, Excerpta Medica. Proceeding from
a Symposium in Basel. 1984;145-53
33)
O' Riordan TG, et al. J Appl Physiol. 1998;85(3):1086-91
34)
Abraham WM, et al. Bull Eur Physiopathol Respir. 1986;22:38792
35)
Ida H. Arzneimittelforschung. 1976;26(7):1337-40
36)
Selroos O. et al. Pulm Pharmacol Ther. 2002;15:175-83
37)
Korn SH, et al. Eur Respir J. 2001;17:1070-7
38)
社内資料:アレルギーラットモデルの気道過敏性及び炎症に及ぼす影響
(2009年10月16日承認、
CTD2.6.2.2)
19.1 ブデソニド
*一般的名称
ブデソニド
(Budesonide)
(JAN)
(日局)
*化学名
16α,17-[(1RS )-Butylidenebis(oxy)]-11β,21-dihydroxypregna-1,4-diene3,20-dione
分子式
C25H34O6
分子量
430.53
*性状
ブデソニドは白色~微黄白色の結晶又は結晶性の粉末である。
ブデソニドはメタノールにやや溶けやすく、
アセトニトリル又はエタノール
(99.5)
にやや溶けにくく、
水にほとんど溶けない。
*化学構造式
融点
約240℃
(分解)
19.2ホルモテロールフマル酸塩水和物
一般的名称
ホルモテロールフマル酸塩水和物
(Formoterol Fumarate Hydrate)
(JAN)
(日局)
*化学名
N -(2-Hydroxy-5-{(1RS )-1-hydroxy-2-[(2RS )-1-(4-methoxyphenyl)
propan-2-ylamino]ethyl}phenyl)formamide hemifumarate monohydrate
分子式
(C19H24N2O4)2・C4H4O4・2H2O
分子量
840.91
性状
ホルモテロールフマル酸塩水和物は白色~帯黄白色の結晶性の粉末である。
酢
酸
(100)
に溶けやすく、
メタノールにやや溶けやすく、
水又はエタノール
(95)
に極めて溶けにくく、
ジエチルエーテルにほとんど溶けない。
本品のメタノー
ル溶液
(1→100)
は旋光性を示さない。
化学構造式
24. 文献請求先及び問い合わせ先
アストラゼネカ株式会社 メディカルインフォメーションセンター
〒530-0011 大阪市北区大深町3番1号
TEL 0120-189-115
https://www.astrazeneca.co.jp
26. 製造販売業者等
26.1 製造販売元
融点
約138℃
(分解)
【参考】
22. 包装
本剤のブデソニド用量は、
容器
(タービュヘイラー)
から放出される薬剤量として表記してお
り、
パルミコートタービュヘイラーのブデソニド用量は容器
(タービュヘイラー)
内で量り取ら
れる薬剤量として表記している。
両薬剤の用量対応は、
以下のとおりである。
〈シムビコートタービュヘイラー30吸入〉
[1本、
乾燥剤入り]
〈シムビコートタービュヘイラー60吸入〉
[1本、
乾燥剤入り]
[10本、
乾燥剤入り]
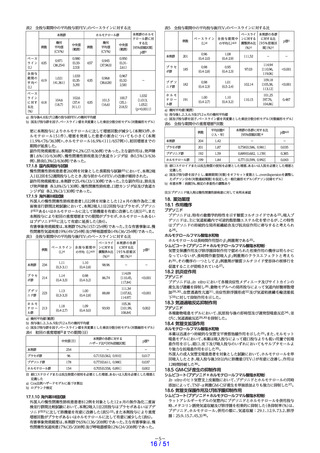
シムビコートタービュヘイラーとパルミコートタービュヘイラーの
ブデソニドに関する用量対応表
ブデソニドの用量
23. 主要文献
1)深瀬広幸 他:アレルギー・免疫, 2009;16(10):1586-602
社内資料:ブデソニドのin vitro 血漿蛋白結合, 1995
2)
社内資料:ホルモテロールフマル酸塩のin vitro 血漿蛋白結合
3)
(843-RD0354)
(2009年10月16日承認、
CTD2.7.2.2)
4)宮本昭正 他:アレルギーの領域, 1997;4(S-1):18-25
5)社内資料:ホルモテロール吸入投与時の肺内到達率
(SD-037-0602)
(2009
年10月16日承認、
CTD2.7.2.2)
6)社内資料:ブデソニドのヒトにおける代謝排泄, 1984
7)Jönsson G, et al. Drug Metab Dispos. 1995;23:137-42
PI370@B
シムビコート
タービュヘイラー
容器から放出される量
(delivered dose)
パルミコート200µg
タービュヘイラー
容器内で量り取られる量
(metered dose)
1回吸入
160µg
200µg
2回吸入
320µg
400µg
4回吸入
640µg
800µg
8回吸入
1280µg
1600µg
SYM
-6-
17 / 51
8)Rosenborg J, et al. Drug Metab Dispos. 1999;27:1104-16
9)社内資料:ホルモテロールのシトクロムP450阻害作用の検討
(843-RD0395)
(2009年10月16日承認、
CTD2.7.2.2)
10)
社内資料:シムビコートと各単剤の血漿中濃度の比較(SD-039-0259)
(2009年10月16日承認、
CTD2.7.1.2)
11)
Seidegård J. Clin Pharmacol Ther. 2000;68:13-7
12)
Raaska K, et al. Clin Pharmacol Ther. 2002;72:362-9
13)
大田 健 他:アレルギー・免疫, 2010;17(4):624-38
14)
足立 満:アレルギー・免疫, 2010;17(2):266-82
15)
Atienza T, et al. Respirology. 2013;18(2):354-63
16)
Rabe KF, et al. Lancet. 2006;368:744-53
17)
Kuna P, et al. Int J Clin Pract. 2007;61:725-36
18)
Bousquet J, et al. Respir Med. 2007;101:2437-46
19)
社内資料:シムビコートの慢性閉塞性肺疾患患者における国際共同第III相
比較試験
(2012年8月10日承認、
CTD2.7.3.3)
20)
社内資料:シムビコートの日本人慢性閉塞性肺疾患患者における第III相長
期投与試験
(2012年8月10日承認、
CTD2.7.3.3)
21)
Calverley PM, et al. Eur Respir J. 2003;22:912-9
22)
Szafranski W, et al. Eur Respir J. 2003;21:74-81
23)
Brattsand R, et al. Clin Ther. 2003;25(Suppl C):C28
24)
Edsbäcker S, et al. Annals of Allergy Asthma & Immunology.
2002;88(6):609-16
25)
Ullman A, et al. Allergy. 1992;47:384-7
26)
Barnes PJ. Eur Respir J. 2002;19:182-91
27)
Roth M, et al. The Lancet. 2002;360:1293-9
28)
Linden M, et al. Pulm Pharmacol. 1994;7:43-7
29)
Woolley MJ, et al. J Appl Physiol. 1994;77:1303-8
30)
社内資料:呼吸困難症SD系ラットにおける卵白アルブミン誘発気道/肺過
敏反応及び炎症細胞に対する作用, 1995
31)
Svensjö E, et al. Prog Resp Res. 1985;19:173-80
32)
Brattsand R, et al. Amsterdam, Excerpta Medica. Proceeding from
a Symposium in Basel. 1984;145-53
33)
O' Riordan TG, et al. J Appl Physiol. 1998;85(3):1086-91
34)
Abraham WM, et al. Bull Eur Physiopathol Respir. 1986;22:38792
35)
Ida H. Arzneimittelforschung. 1976;26(7):1337-40
36)
Selroos O. et al. Pulm Pharmacol Ther. 2002;15:175-83
37)
Korn SH, et al. Eur Respir J. 2001;17:1070-7
38)
社内資料:アレルギーラットモデルの気道過敏性及び炎症に及ぼす影響
(2009年10月16日承認、
CTD2.6.2.2)
19.1 ブデソニド
*一般的名称
ブデソニド
(Budesonide)
(JAN)
(日局)
*化学名
16α,17-[(1RS )-Butylidenebis(oxy)]-11β,21-dihydroxypregna-1,4-diene3,20-dione
分子式
C25H34O6
分子量
430.53
*性状
ブデソニドは白色~微黄白色の結晶又は結晶性の粉末である。
ブデソニドはメタノールにやや溶けやすく、
アセトニトリル又はエタノール
(99.5)
にやや溶けにくく、
水にほとんど溶けない。
*化学構造式
融点
約240℃
(分解)
19.2ホルモテロールフマル酸塩水和物
一般的名称
ホルモテロールフマル酸塩水和物
(Formoterol Fumarate Hydrate)
(JAN)
(日局)
*化学名
N -(2-Hydroxy-5-{(1RS )-1-hydroxy-2-[(2RS )-1-(4-methoxyphenyl)
propan-2-ylamino]ethyl}phenyl)formamide hemifumarate monohydrate
分子式
(C19H24N2O4)2・C4H4O4・2H2O
分子量
840.91
性状
ホルモテロールフマル酸塩水和物は白色~帯黄白色の結晶性の粉末である。
酢
酸
(100)
に溶けやすく、
メタノールにやや溶けやすく、
水又はエタノール
(95)
に極めて溶けにくく、
ジエチルエーテルにほとんど溶けない。
本品のメタノー
ル溶液
(1→100)
は旋光性を示さない。
化学構造式
24. 文献請求先及び問い合わせ先
アストラゼネカ株式会社 メディカルインフォメーションセンター
〒530-0011 大阪市北区大深町3番1号
TEL 0120-189-115
https://www.astrazeneca.co.jp
26. 製造販売業者等
26.1 製造販売元
融点
約138℃
(分解)
【参考】
22. 包装
本剤のブデソニド用量は、
容器
(タービュヘイラー)
から放出される薬剤量として表記してお
り、
パルミコートタービュヘイラーのブデソニド用量は容器
(タービュヘイラー)
内で量り取ら
れる薬剤量として表記している。
両薬剤の用量対応は、
以下のとおりである。
〈シムビコートタービュヘイラー30吸入〉
[1本、
乾燥剤入り]
〈シムビコートタービュヘイラー60吸入〉
[1本、
乾燥剤入り]
[10本、
乾燥剤入り]
シムビコートタービュヘイラーとパルミコートタービュヘイラーの
ブデソニドに関する用量対応表
ブデソニドの用量
23. 主要文献
1)深瀬広幸 他:アレルギー・免疫, 2009;16(10):1586-602
社内資料:ブデソニドのin vitro 血漿蛋白結合, 1995
2)
社内資料:ホルモテロールフマル酸塩のin vitro 血漿蛋白結合
3)
(843-RD0354)
(2009年10月16日承認、
CTD2.7.2.2)
4)宮本昭正 他:アレルギーの領域, 1997;4(S-1):18-25
5)社内資料:ホルモテロール吸入投与時の肺内到達率
(SD-037-0602)
(2009
年10月16日承認、
CTD2.7.2.2)
6)社内資料:ブデソニドのヒトにおける代謝排泄, 1984
7)Jönsson G, et al. Drug Metab Dispos. 1995;23:137-42
PI370@B
シムビコート
タービュヘイラー
容器から放出される量
(delivered dose)
パルミコート200µg
タービュヘイラー
容器内で量り取られる量
(metered dose)
1回吸入
160µg
200µg
2回吸入
320µg
400µg
4回吸入
640µg
800µg
8回吸入
1280µg
1600µg
SYM
-6-
17 / 51